Clear Sky Science · it
Analisi di concordanza tra profili di DNA e RNA: lo studio IMPACT2 del MD Anderson in oncologia di precisione
Perché questa ricerca conta per i pazienti oncologici
Il trattamento del cancro è sempre più guidato dal patrimonio genetico del tumore di ciascun paziente. I medici usano già test sul DNA per identificare mutazioni bersagliabili con farmaci specifici, ma questi test non raccontano l'intera storia su come si comporti un tumore. Questo studio del MD Anderson Cancer Center pone una domanda pratica: se guardiamo anche all'RNA — le “copie operative” dei geni che indicano quali geni sono effettivamente attivi o inattivi — possiamo comprendere meglio il cancro di un paziente e le sue probabilità di sopravvivenza?
Due livelli di informazione: DNA e RNA
Ogni cellula tumorale porta modifiche nel DNA, ma il DNA è per lo più una planimetria statica. L'RNA, al contrario, cattura ciò che la cellula sta effettivamente facendo in un dato momento. Nell'ambito della sperimentazione IMPACT2, più di 800 pazienti con tumori avanzati hanno effettuato un profilo genetico del loro tumore. Per 253 di loro i ricercatori disponevano di dati sia sul DNA sia sull'RNA. Hanno confrontato quali geni risultavano alterati a livello di DNA (come mutazioni o copie extra) e quali mostravano livelli di RNA insolitamente alti o bassi, verificando quanto spesso questi due livelli raccontassero la stessa storia e se tali informazioni fossero correlate alla sopravvivenza dei pazienti.
Quando le modifiche geniche e l'attività coincidono
Il gruppo ha prima cercato eventi “concordanti” — casi in cui lo stesso gene risultava anomalo sia nel DNA sia nell'RNA. Tra i 253 pazienti, 50 avevano almeno una corrispondenza di questo tipo, per un totale di 58 eventi distribuiti su 23 geni. La maggior parte di questi coinvolgeva copie in eccesso o mancanti di un gene che mostrava anche livelli di RNA più alti o più bassi, e questa corrispondenza era più marcata per oncogeni noti come CDKN2A, AR, ESR1, KRAS, PIK3CA, AKT2, TP53 e CCND1. Questi riscontri supportano l'idea che, per alcuni geni chiave del cancro, le modifiche strutturali del DNA si traducano effettivamente in un aumento o diminuzione dell'attività genica, rafforzandone l'importanza come bersagli terapeutici.
Relazioni nascoste rivelate dai segnali dell'RNA
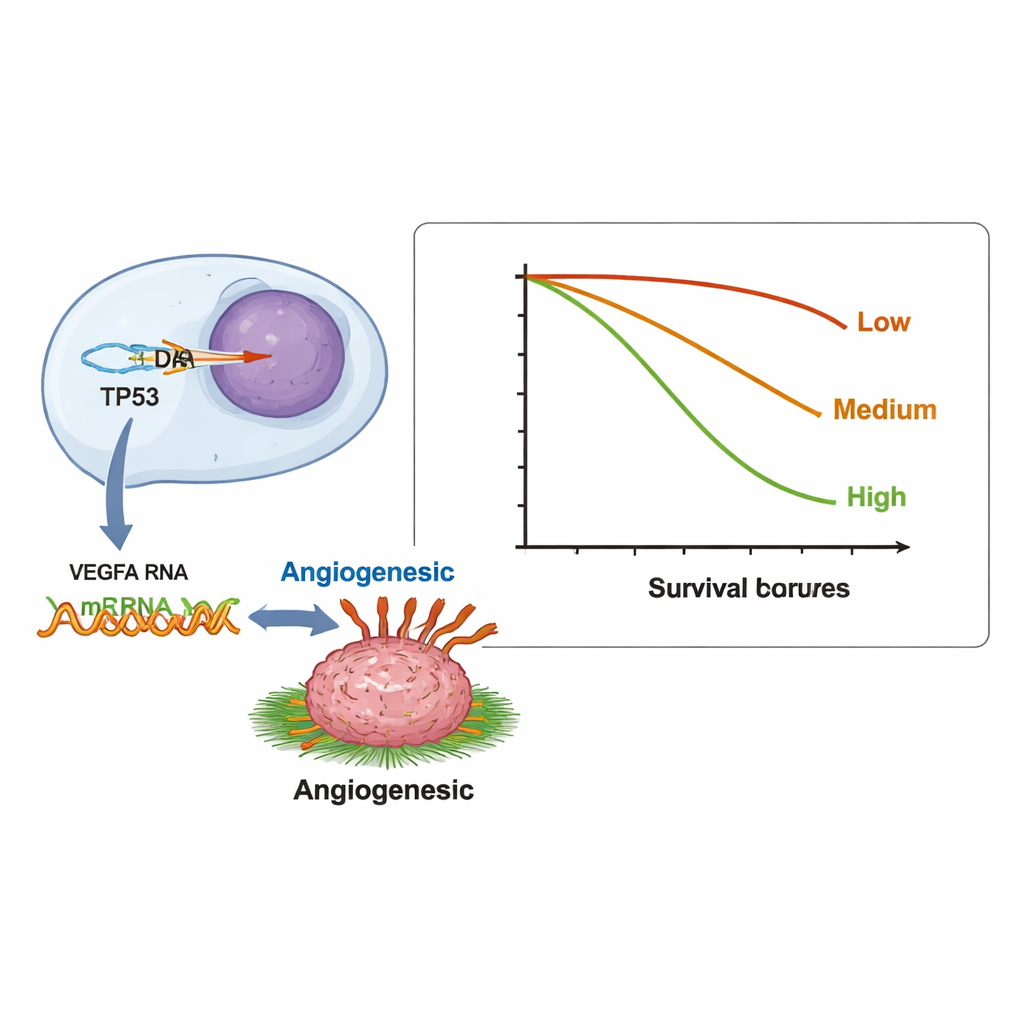
Oltre alle corrispondenze uno a uno, i ricercatori hanno analizzato più di 12.000 coppie di geni per verificare se una variazione del DNA in un gene fosse sistematicamente legata a livelli anomali di RNA in un altro. Hanno trovato 123 coppie significative. Molte di queste si raggruppavano in una grande rete di crescita e sopravvivenza nota come via PI3K/AKT, spesso al centro di terapie mirate. Un pattern particolarmente notevole collegava alterazioni nel gene oncosoppressore TP53 a segnali di RNA iperattivi di VEGFA, un gene che aiuta i tumori a formare nuovi vasi sanguigni. Questa relazione potrebbe contribuire a spiegare perché alcuni pazienti con alterazioni di TP53 rispondono al bevacizumab, un farmaco che blocca la formazione di vasi, e illustra come i dati sull'RNA possano mettere in luce interazioni gene–gene clinicamente rilevanti che il DNA da solo potrebbe non evidenziare.
Carico di attività genica e sopravvivenza dei pazienti
I ricercatori hanno poi valutato se la quantità complessiva di attività genica anomala in un tumore — ciò che hanno definito carico trascrizionale tumorale, o TTB — fosse collegata alla durata della sopravvivenza. Hanno contato quanti geni mostravano livelli di RNA alterati in ciascun paziente e li hanno raggruppati in basso (0–2 geni), intermedio (3–5) e alto (6 o più). I pazienti nel gruppo ad alto TTB hanno vissuto una mediana di 6,7 mesi, rispetto a 9,8 e 11,9 mesi nei gruppi inferiori. In altre parole, i tumori con molti geni “malfunzionanti” a livello di RNA tendevano a essere più aggressivi. I tumori privi di PD-L1, un marcatore spesso usato per selezionare i pazienti per l'immunoterapia, tendevano inoltre ad avere un numero maggiore di geni con espressione anomala, suggerendo un possibile legame tra ampia disfunzione genica e un ambiente tumorale resistente all'attacco immunitario.
Cosa significa per la cura del cancro in futuro
Questo studio dimostra che la profilazione dell'RNA aggiunge informazioni utili e complementari ai test sul DNA in pazienti reali con tumori avanzati. In alcuni geni, le modifiche del DNA e l'attività dell'RNA coincidono e rafforzano i bersagli terapeutici noti; in altri casi, i modelli trascrizionali rivelano nuove relazioni che potrebbero guidare la scelta dei farmaci, come il legame tra TP53 e VEGFA. Soprattutto per i pazienti, un elevato carico di attività genica anomala è stato associato a una sopravvivenza più breve, suggerendo che misure basate sull'RNA potrebbero aiutare i medici a valutare l'aggressività di un tumore e affinare la prognosi. Sebbene il testing dell'RNA non sia ancora impiegato di routine per selezionare le terapie, questi risultati ne supportano il potenziale come passo successivo nell'oncologia di precisione, soprattutto man mano che studi più ampi e strumenti analitici migliori facilitano l'integrazione della profilazione trascrittomica nella pratica clinica quotidiana.
Citazione: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
Parole chiave: oncologia di precisione, profilazione dell'RNA, sequenziamento del DNA, carico trascrizionale tumorale, biomarcatori del cancro