Clear Sky Science · it
La iperglutaminolisi guida la senescenza e l’invecchiamento attraverso l’attivazione dell’asse arginina-mTORC1
Perché questa ricerca è importante per un invecchiamento sano
L’invecchiamento non riguarda solo rughe e capelli grigi: riguarda cellule in tutto il corpo che perdono gradualmente la capacità di ripararsi e rigenerarsi. Questo studio pone una domanda apparentemente semplice ma di grande portata: il modo in cui le nostre cellule bruciano l’amminoacido glutamina può effettivamente spingerle verso l’età avanzata? Gli autori scoprono una catena metabolica prima nascosta che collega il processamento della glutamina a un interruttore di crescita potente chiamato mTORC1, e dimostrano che l’eccessiva attivazione di questa via può accelerare attivamente l’invecchiamento cellulare in moscerini e topi.
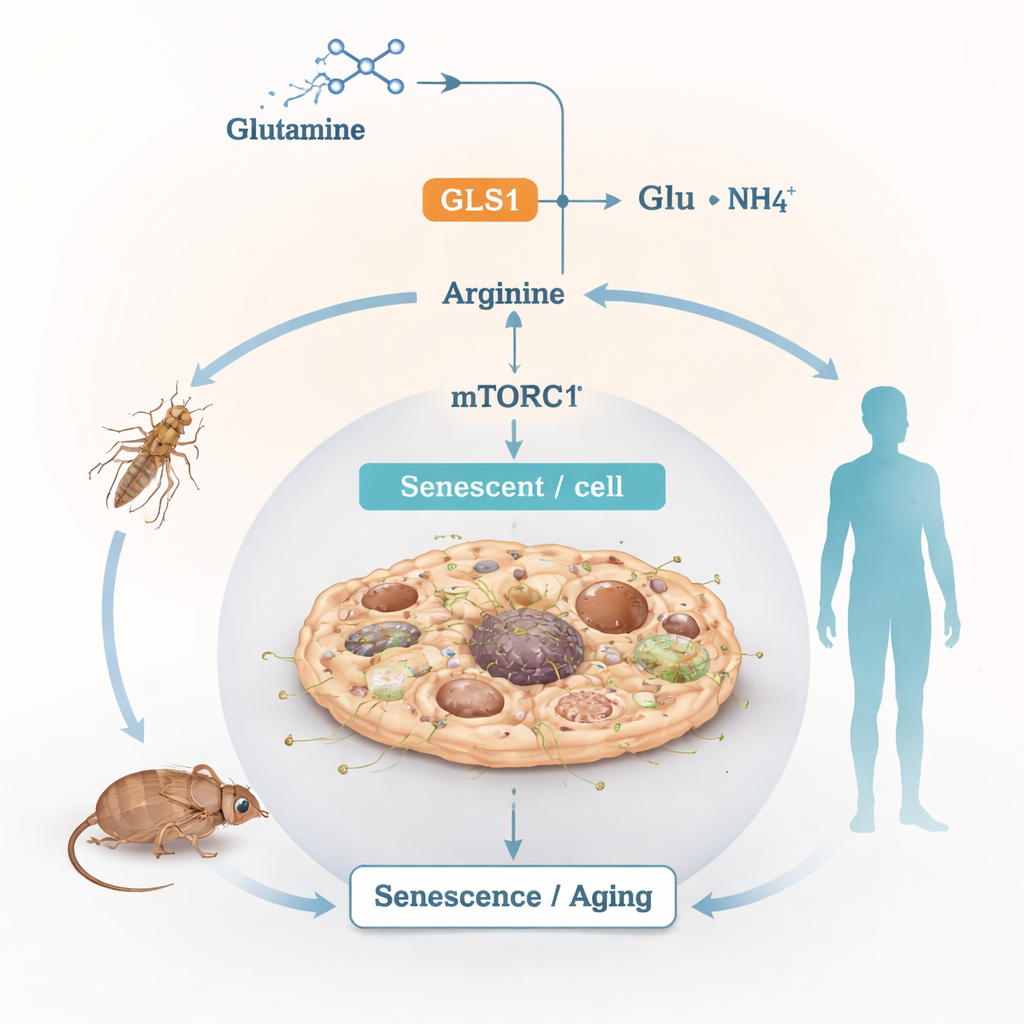
Una linea di carburante che corre troppo calda
La glutamina è l’amminoacido libero più abbondante nel sangue e nei tessuti. Le cellule la usano come combustibile versatile e come mattone per la sintesi, degradandola tramite un processo chiamato glutaminolisi. Il primo passaggio è catalizzato da un enzima chiamato GLS1, che converte la glutamina in glutammato e ammonio; da lì i prodotti confluiscono nella produzione di energia, nelle difese antiossidanti e nella sintesi di altri amminoacidi. Pur essendo questa degradazione cruciale per la vita normale, gli autori si sono chiesti cosa accada quando diventa cronicamente iperattiva nel contesto dell’invecchiamento e dello stress.
Scoprire la “iperglutaminolisi” in cellule e animali vecchi
Utilizzando un profilo avanzato dei metaboliti, il gruppo ha confrontato cellule giovani e in divisione con cellule senescenti—cellule più vecchie che hanno cessato di dividersi e secernono fattori infiammatori. Hanno riscontrato che molti amminoacidi aumentavano, con la glutamina al centro della rete riorganizzata. Le cellule senescenti consumavano più glutamina, presentavano livelli e attività di GLS1 più elevati e accumulavano più glutammato e ammonio. Cambiamenti simili sono apparsi nell’organismo intero: moscerini invecchiati e topi anziani mostravano attività di GLS elevata in più tessuti. Gli autori hanno definito questo stato condiviso di aumentata degradazione della glutamina “iperglutaminolisi”, suggerendo che sia una caratteristica conservata dell’invecchiamento piuttosto che un effetto collaterale marginale.
Abbassare la degradazione della glutamina rallenta i segni dell’invecchiamento
Se l’iperglutaminolisi accompagna l’invecchiamento, contribuisce davvero a guidarlo? Per testarlo, i ricercatori hanno bloccato la glutaminolisi in diversi modi: riducendo la glutamina nel mezzo di coltura, inibendo GLS con farmaci o riducendo geneticamente GLS1. In cellule stressate o replicativamente invecchiate, questi interventi hanno ridotto marcatori classici di senescenza come la colorazione SA-β-gal, l’inibitore del ciclo cellulare p16 e i segnali infiammatori del “SASP”. Nei moscerini, sia la riduzione genetica di GLS sia dosi basse di farmaci bloccanti GLS hanno prolungato la durata di vita, migliorato la capacità di arrampicata (un test di vigore) e ridotto la perdita di integrità intestinale legata all’età. È importante che, quando la glutaminolisi è stata limitata fin dall’inizio dell’esposizione allo stress, l’effetto non dipendeva principalmente dall’eliminazione delle cellule vecchie, ma dal prevenire che diventassero senescenti in primo luogo.
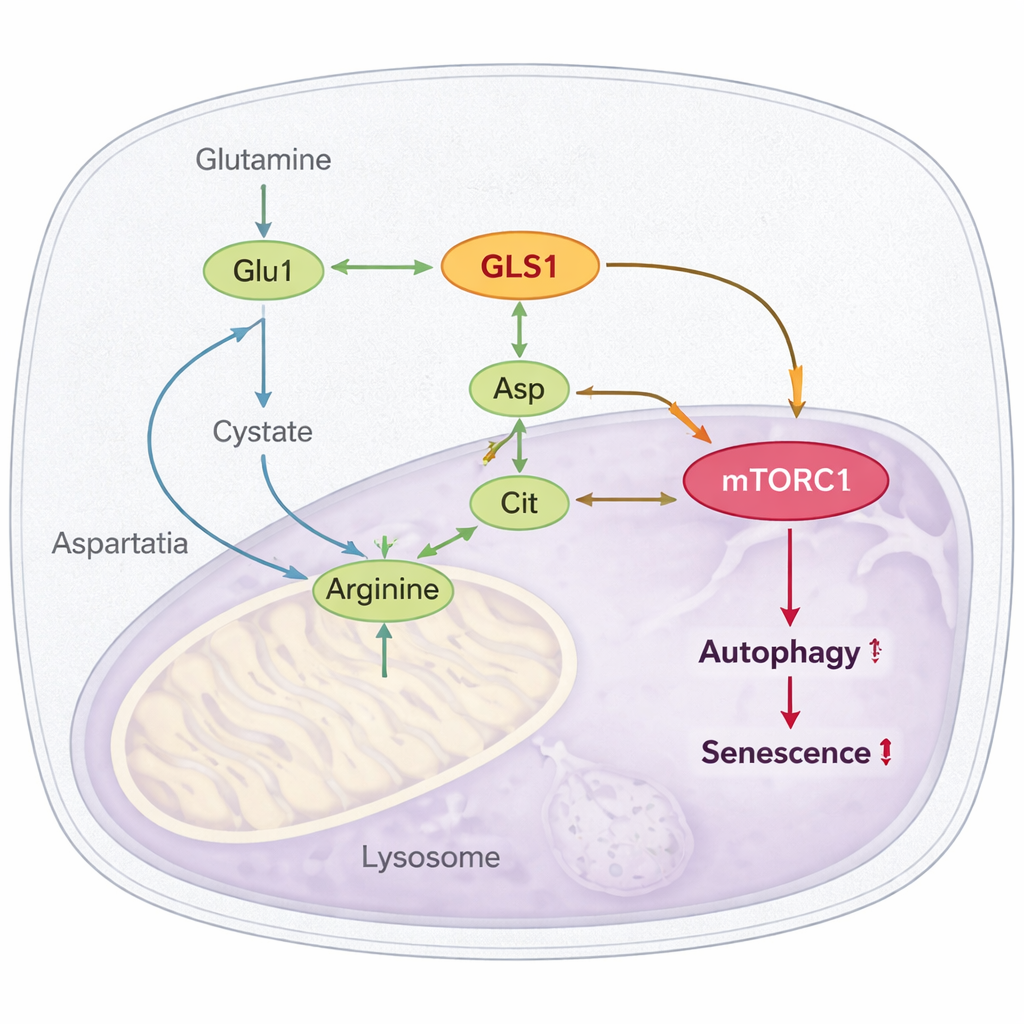
Un circuito nascosto: dalla glutamina all’arginina fino a mTORC1
La scoperta più sorprendente è come questa via iperattiva si colleghi a mTORC1, un regolatore principale che, quando rimane acceso in modo persistente, è noto per promuovere l’invecchiamento e bloccare il riciclaggio cellulare (autofagia). Gli autori mostrano che l’iperglutaminolisi potenzia la produzione di arginina, un altro amminoacido che attiva direttamente mTORC1. Glutammato e ammonio generati dalla glutamina confluiscono nella sintesi di aspartato e citrullina, che vengono poi combinati in arginina. In cellule e moscerini anziani, i livelli di arginina e dei suoi precursori aumentano; bloccare GLS o abbassare l’espressione di un enzima chiave della sintesi dell’arginina (ASL) riduce l’arginina e attenua l’attività di mTORC1. Dimostrano inoltre che la proteina sensore dell’arginina CASTOR1 è necessaria per questo effetto: quando CASTOR1 è disabilitata, bloccare la glutaminolisi non silenzia più mTORC1 né migliora l’autofagia, e il beneficio sulla senescenza viene perso.
Quando troppo di qualcosa di buono accelera l’invecchiamento
Per verificare se spingere semplicemente più forte questa via potesse accelerare l’invecchiamento cellulare, il team ha sovraccaricato cellule altrimenti sane con glutamina, arginina o combinazioni dei metaboliti intermedi per settimane. Il risultato è stato un chiaro aumento dei marcatori di senescenza e dei geni infiammatori. Nei moscerini, la supplementazione a lungo termine con glutamina o arginina in eccesso ha ridotto la durata mediana e massima della vita. Nel complesso, il lavoro delinea una cascata completa: l’eccessiva degradazione della glutamina (iperglutaminolisi) amplifica la produzione di arginina, che viene rilevata da CASTOR1, mantiene mTORC1 anormalmente attivo, sopprime il riciclo cellulare e promuove la senescenza e l’invecchiamento dell’organismo.
Cosa significa questo per le future strategie anti-età
Per i non specialisti, questo studio ricolloca il metabolismo della glutamina come una spada a doppio taglio: necessario per la salute, ma potenzialmente dannoso quando cronicamente iperattivato nella mezza-età e oltre. Mappando una via concreta dalla catabolizzazione della glutamina alla sovraattivazione di mTORC1, gli autori evidenziano nuovi punti di intervento—come gli enzimi GLS1 e ASL o il passo di sensori dell’arginina—che potrebbero essere modulati per rallentare il declino legato all’età senza spegnere completamente il metabolismo vitale. Sebbene sia ancora troppo presto per tradurre questi risultati in consigli dietetici o trattamenti, il lavoro aggiunge un tassello importante al puzzle di come il metabolismo quotidiano dei nutrienti possa spingere le nostre cellule verso la resilienza o verso un invecchiamento accelerato.
Citazione: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
Parole chiave: metabolismo del glutamine, senescenza cellulare, segnalazione mTORC1, biosintesi dell’arginina, interventi sull’invecchiamento