Clear Sky Science · it
L’antigene nucleare 1 esogeno del virus Epstein–Barr induce una resistenza ai tumori guidata da ADAR1 contro l’immunoterapia
Perché un virus comune conta per il trattamento del cancro
Molti tumori vengono oggi trattati con farmaci immunoterapici che liberano il sistema immunitario dell’organismo. Tuttavia la maggior parte dei pazienti non ne trae beneficio, perché i loro tumori imparano a nascondersi dall’attacco immunitario. Questo studio rivela come un virus molto comune, il virus di Epstein–Barr (EBV), aiuti i tumori a disattivare le difese immunitarie e a resistere a questi potenti farmaci — e come un nuovo tipo di molecola progettata possa riattivare quelle difese.
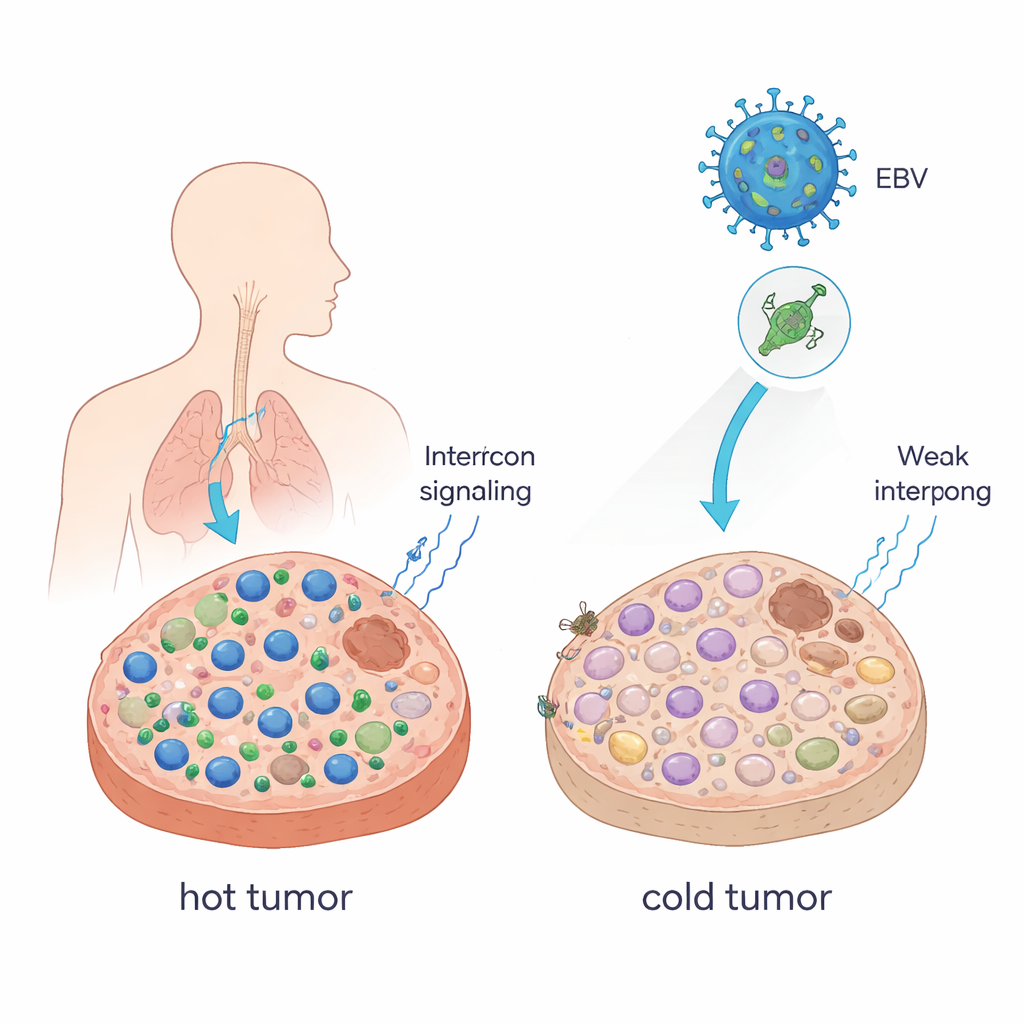
Trasformare tumori “caldi” in tumori “freddi”
I medici descrivono spesso i tumori come “caldi” quando sono pieni di cellule T che uccidono il cancro, e “freddi” quando queste cellule scarseggiano. I tumori caldi rispondono di solito bene agli inibitori dei checkpoint immunitari (ICB) come gli anticorpi anti–PD-1; i tumori freddi spesso no. Gli autori hanno mostrato che una singola proteina dell’EBV, chiamata EBNA1, può spingere i tumori verso questo stato più freddo ed elusivo. Quando hanno costretto cellule tumorali murine a produrre EBNA1 e le hanno impiantate in topi con sistema immunitario integro, i tumori sono diventati più grandi, contenevano meno cellule CD8+ T e cellule natural killer, e avevano più macrofagi immunosoppressivi. Anche i segnali detti interferoni — messaggeri chiave che aiutano a radunare le cellule immunitarie — risultavano fortemente ridotti. In campioni di pazienti con carcinoma nasofaringeo, un tumore strettamente legato all’EBV, i tumori che esprimevano EBNA1 mostravano analogamente meno cellule CD8+ rispetto al tessuto normale.
Una scorciatoia virale nel macchinario di controllo dell’RNA della cellula
Per capire come EBNA1 rimodelli l’ambiente tumorale, i ricercatori hanno cercato proteine umane che interagissero fisicamente con essa. Si sono concentrati su una proteina chiamata IGF2BP3, che legge piccole modifiche chimiche (m6A) sugli mRNA e può aumentarne la stabilità o la traduzione in proteina. EBNA1 si legava saldamente a IGF2BP3 in diversi tipi cellulari, incluse cellule tumorali EBV-positive. I dati dai tumori dei pazienti hanno mostrato che livelli elevati di IGF2BP3 andavano di pari passo con una debole attività dei geni legati agli interferoni e con una minore infiltrazione di cellule T CD8+, suggerendo che questa alleanza virus-ospite potrebbe attenuare l’immunità anti-tumorale.
Potenziare un editor dell’RNA che silenzia i segnali di pericolo
Un’analisi più approfondita ha evidenziato un bersaglio chiave di questa interazione: ADAR1, un enzima che modifica l’RNA a doppio filamento cambiando certe lettere “A” in “I”. Questo editing può far apparire meno pericoloso l’RNA simile a quello virale all’interno delle cellule agli sensori interni, riducendo le risposte interferoniche. Gli autori hanno scoperto che EBNA1, IGF2BP3 e un fattore di traduzione chiamato EIF4G1 formano un complesso a tre sulla molecola di mRNA di ADAR1. Questo complesso aumenta il marchio m6A, recluta il macchinario di traduzione e potenzia selettivamente la produzione della proteina ADAR1 senza aumentare i suoi livelli di RNA. Di conseguenza, le cellule tumorali eseguono più editing dell’RNA in elementi genetici ripetuti posti vicino ai geni correlati agli interferoni. Queste modifiche riducono la quantità di RNA doppio filamento non editato che normalmente allerterebbe sensori come MDA5 e PKR, attenuando la produzione di interferoni e aiutando i tumori a nascondersi dall’attacco immunitario.
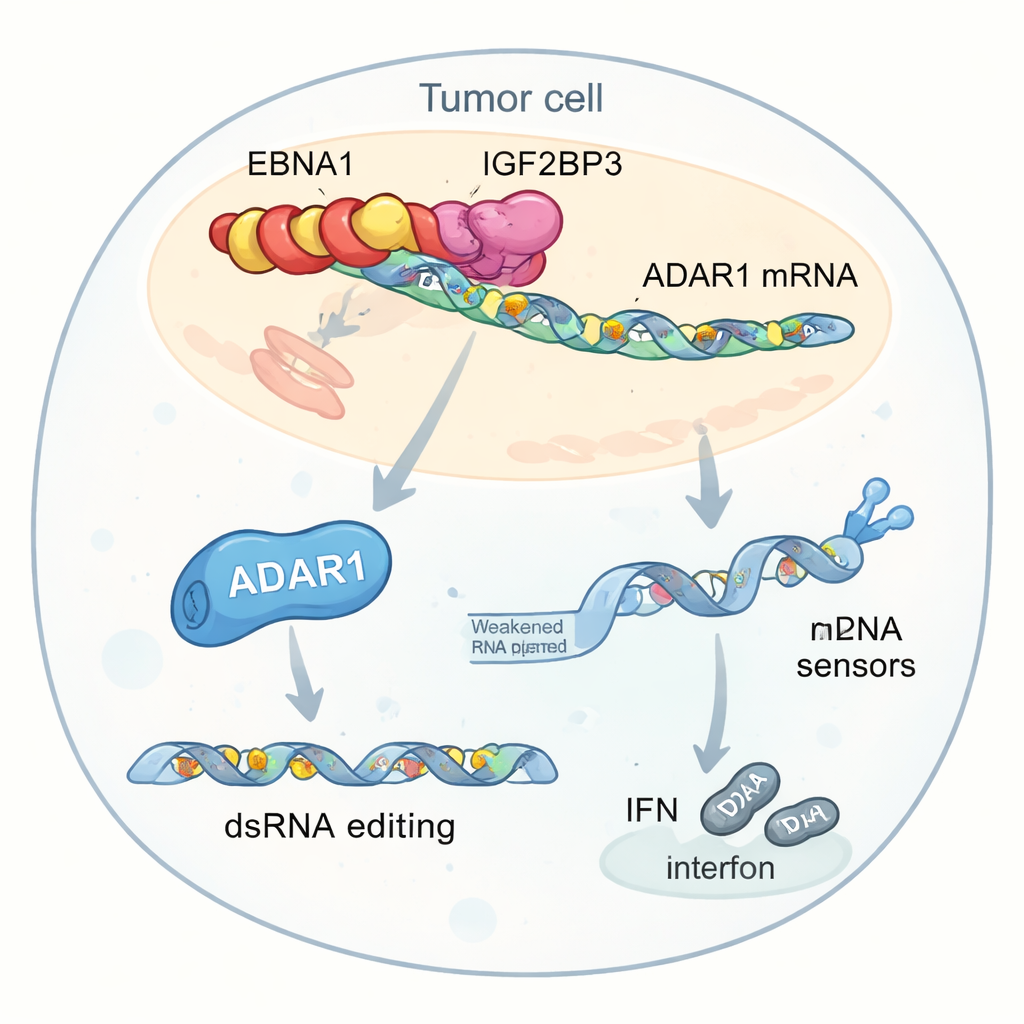
Meno interferone, immunoterapia più debole
Quando cellule tumorali che esprimevano EBNA1 sono state esposte in laboratorio a cellule T e ad anticorpi anti–PD-1, erano più difficili da uccidere rispetto alle cellule di controllo e rilasciavano meno interferone. Anche quando trattate direttamente con interferone, le cellule che portavano EBNA1 erano meno sensibili e i loro sensori interni dell’RNA si attivavano meno intensamente. Ridurre i livelli di ADAR1 ha parzialmente invertito questi effetti, restaurando l’attività dei sensori e la segnalazione interferonica. Esperimenti genetici e di sequenziamento hanno confermato che le cellule che esprimevano EBNA1 mostravano più eventi di editing A-to-I in regioni RNA specifiche, particolarmente dopo stimolazione con interferone, a ulteriore supporto dell’idea che il potenziamento virale di ADAR1 contribuisca a neutralizzare i segnali di pericolo che altrimenti scatenerebbero risposte immunitarie forti.
Un degrader progettato che riaccende l’attacco immunitario
Il gruppo si è poi chiesto se privare i tumori di EBNA1 potesse ripristinarne la vulnerabilità all’immunoterapia. Hanno progettato una molecola PROTAC, EP-1215, che etichetta EBNA1 per la distruzione da parte del sistema di smaltimento della cellula. A basse dosi, EP-1215 degradava efficacemente EBNA1 e riduceva i livelli della proteina ADAR1. Negli esperimenti sui topi, EP-1215 da solo ha avuto un impatto limitato sui tumori EBNA1-positivi, e anche l’anti–PD-1 da solo è risultato debole. Ma quando combinati, i due trattamenti hanno ridotto drasticamente i tumori, aumentato l’infiltrazione di cellule T CD8+ e incrementato le cellule T produttrici di interferone. In modelli murini umanizzati portatori di cellule immunitarie umane e tumori correlati all’EBV, la combinazione ha nuovamente superato i trattamenti singoli, senza tossicità evidente per fegato o reni.
Cosa significa per la cura del cancro in futuro
Per i non specialisti, il messaggio è che un virus comune può silenziosamente riorganizzare le cellule tumorali per attenuare i sistemi di allarme interni, spegnendo segnali chimici che altrimenti attirerebbero e attiverebbero le cellule immunitarie. EBNA1 fa ciò dirottando un lettore dell’RNA dell’ospite (IGF2BP3) e un fattore di traduzione (EIF4G1) per sovraprodurre l’editor dell’RNA ADAR1, che modifica le strutture RNA stesse che i sensori immunitari sono progettati per riconoscere. Degradando EBNA1 con un PROTAC mirato come EP-1215, gli autori sono riusciti a ripristinare questi segnali di pericolo e a rendere nuovamente sensibili i tumori resistenti agli attuali farmaci di checkpoint. Se strategie simili risultassero sicure ed efficaci nell’uomo, mirare agli aiutanti virali come EBNA1 potrebbe offrire un nuovo modo per convertire tumori freddi legati a EBV in bersagli “caldi” che le immunoterapie moderne possono finalmente colpire.
Citazione: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Parole chiave: Virus di Epstein-Barr, resistenza all’immunoterapia, ADAR1, editing dell’RNA, carcinoma nasofaringeo