Clear Sky Science · it
Meccanismo molecolare della fusione di membrana dipendente dal colesterolo nell’ingresso di SARS-CoV-2
Perché il colesterolo è importante per un virus respiratorio
Il virus che causa il COVID-19, SARS-CoV-2, entra nelle nostre cellule fondendo il suo involucro esterno con le membrane cellulari. Questo articolo pone una domanda apparentemente semplice ma dalle grandi implicazioni: quanto incide il colesterolo — una sostanza grassa nota soprattutto per il suo ruolo nelle malattie cardiovascolari — su quella fase di fusione? Gli autori mostrano che il colesterolo nella membrana virale non si limita a modulare l’efficienza dell’infezione; in realtà aiuta a organizzare le proteine spike del virus in potenti piattaforme di aggancio che rendono l’ingresso più facile e più affidabile.
Costruire un modello minimale dell’ingresso virale
Per analizzare questo processo, i ricercatori hanno ricostruito l’incontro virus‑cellula in provetta usando piccole bolle lipidiche chiamate liposomi. Un set di liposomi portava la proteina spike di SARS‑CoV‑2 e rappresentava la membrana virale; l’altro portava il recettore ACE2, mimando la superficie della cellula ospite. Quando miscelati e attivati da enzimi specifici che “tagliano” la spike nella sua forma pronta alla fusione, queste membrane artificiali si sono fuse, permettendo a un colorante fluorescente di passare da una bolla all’altra. Questo sistema essenziale ha permesso al team di regolare con precisione la composizione lipidica — compresi i livelli di colesterolo — su entrambe le superfici e osservare come la fusione si svolgeva passo dopo passo. 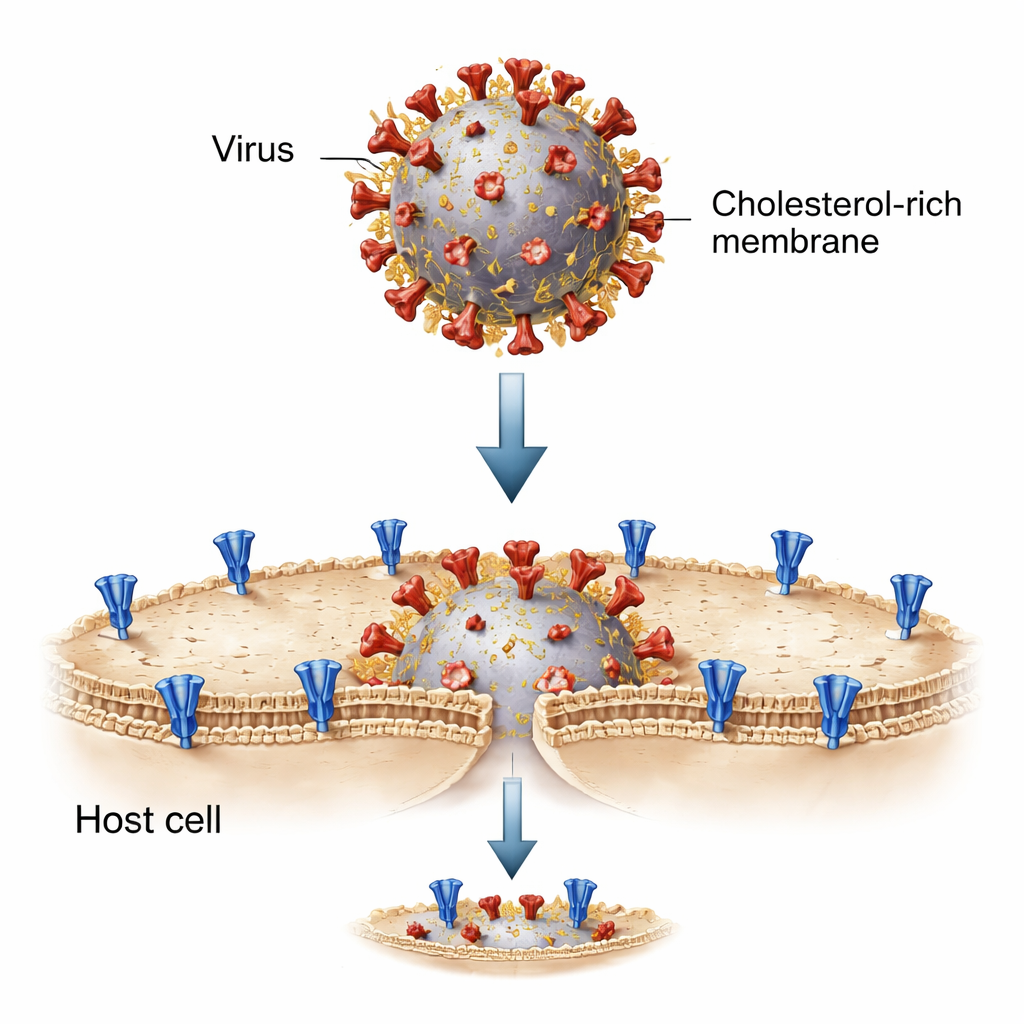
Il colesterolo potenzia l’aggancio più che la fusione
Variando il colesterolo, il gruppo ha scoperto che aggiungerlo alla membrana contenente la spike aumentava la frequenza della fusione, ma non nel modo che si potrebbe immaginare. L’elevato colesterolo non cambiava in modo drammatico la probabilità che due membrane già attaccate si fondessero effettivamente. Piuttosto, aumentava nettamente la frequenza con cui le vescicole con spike si agganciavano inizialmente alle vescicole con ACE2. L’imaging a singola particella ha mostrato molti più eventi di aggancio riusciti quando la spike si trovava in membrane ricche di colesterolo, mentre la probabilità che una coppia agganciata procedesse fino alla fusione completa restava più o meno costante. Interessante notare che caricare di colesterolo il lato ACE2 dava pochi benefici e a livelli molto elevati ostacolava persino la fusione, indicando il colesterolo virale — più che quello dell’ospite — come il principale fattore determinante.
Dal modello membranoso alle cellule vive
I ricercatori hanno poi verificato se lo stesso schema valesse nelle cellule vive. Hanno ingegnerizzato cellule umane per esprimere o la spike o ACE2 e le hanno messe a contatto per osservare la formazione di grandi strutture fuse, i sincizi. Rimuovere il colesterolo dalle cellule che esprimevano la spike ha quasi abolito la formazione dei sincizi, mentre il ripristino del colesterolo ha recuperato la fusione. In esperimenti paralleli con “pseudovirus” SARS‑CoV‑2 (particelle virali innocue che usano la spike del coronavirus per entrare nelle cellule), la rimozione del colesterolo dalla membrana virale ha ridotto drasticamente l’infezione, e il suo reinserimento l’ha aumentata in modo dose‑dipendente. Al contrario, modificare il colesterolo nelle sole cellule che esprimevano ACE2 provocava pochi cambiamenti. In tutti gli esperimenti, il messaggio era coerente: il colesterolo nella membrana contenente la spike è essenziale per un ingresso efficiente.
Cluster di spike: l’arma segreta del colesterolo
Perché il colesterolo sul lato virale conta così tanto? L’imaging ad alta risoluzione delle membrane cellulari ha rivelato che le proteine spike tendono a formare ammassi densi quando il colesterolo è abbondante, mentre restano più disperse quando è scarso. Misure a singola molecola hanno mostrato che questi cluster contengono più copie di spike in condizioni ricche di colesterolo. Gli autori hanno ricondotto questo effetto a una regione ricca di cisteine (CRR) nella coda della spike, all’interno della membrana virale. Questo segmento è modificato mediante palmitoilazione — un tipo di “ancora” lipidica che preferisce i domini ricchi di colesterolo. Quando il team ha troncato la coda della spike o mutato tutte le dieci cisteine per bloccare la palmitoilazione, la spike non si è più raggruppata con il colesterolo, e il potenziamento di aggancio e fusione dovuto al colesterolo è scomparso. 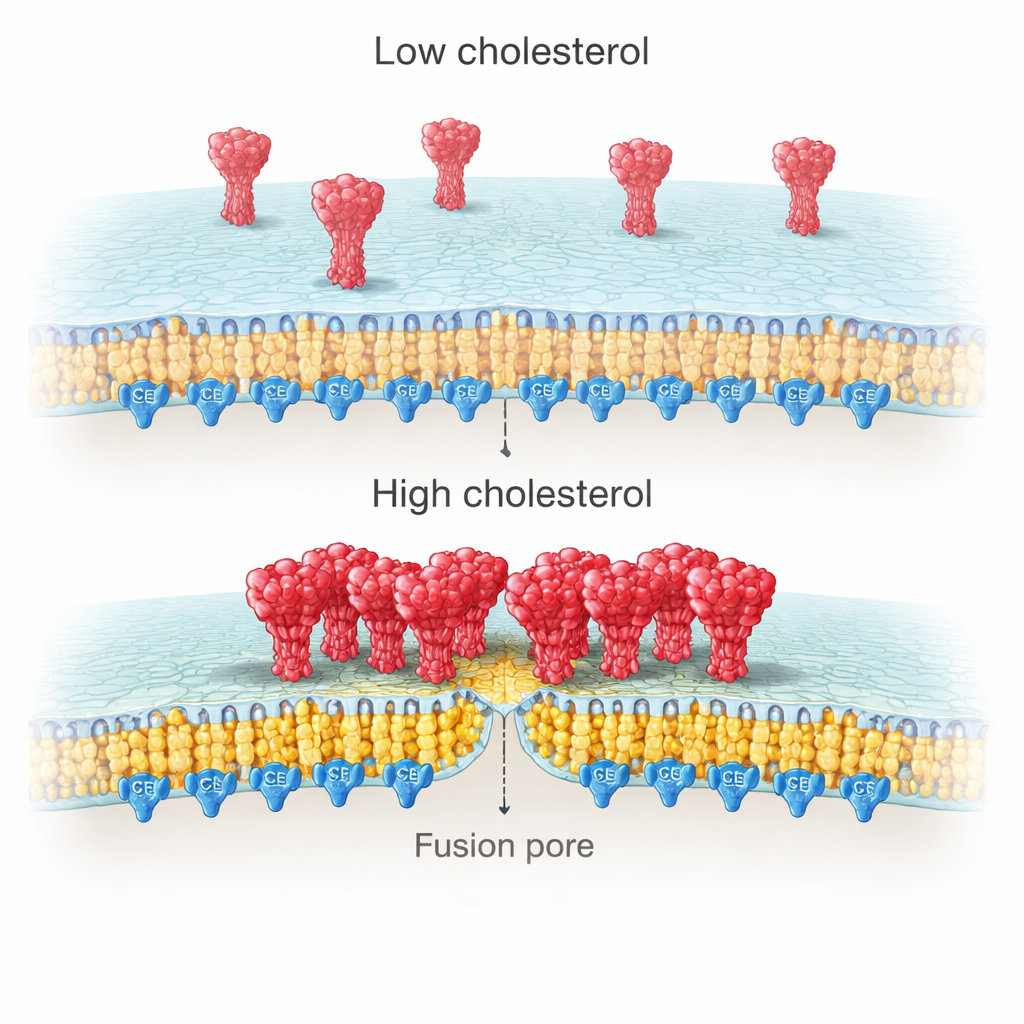
Come questo può aiutare terapie future
In termini semplici, lo studio conclude che il colesterolo trasforma la membrana virale in una piattaforma di fusione raccogliendo molte proteine spike in stretti aggregati mediante la loro regione di coda palmitoilata. Questi cluster si agganciano più efficacemente all’ACE2 sulle cellule ospiti, aumentando le probabilità che un dato incontro conduca a una fusione e a un’infezione riuscite. Per i non specialisti, il punto chiave è che il colesterolo non è solo un ingrediente passivo dell’involucro virale; è un organizzatore attivo della macchina spike. Questo rende la coda ricca di cisteine e sensibile al colesterolo della spike — e gli enzimi che la palmitoilano — bersagli promettenti per strategie antivirali a largo spettro che potrebbero funzionare attraverso varianti diverse del coronavirus.
Citazione: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Parole chiave: colesterolo, spike di SARS-CoV-2, fusione di membrana, ingresso virale, palmitoilazione