Clear Sky Science · it
PKC-eta promuove le metastasi del cancro al seno regolando la via di segnalazione Hippo–YAP
Perché questa ricerca è importante
Il carcinoma mammario triplo negativo (TNBC) è una delle forme più pericolose di cancro al seno perché si diffonde precocemente e manca di terapie mirate. Questo studio svela come un enzima specifico all’interno delle cellule tumorali, chiamato PKC‑eta (PKCη), agisca come un interruttore principale che aiuta i tumori a staccarsi, viaggiare attraverso il corpo e colonizzare nuovi siti. Comprendendo questo interruttore, i ricercatori identificano anche un piccolo peptide naturale in grado di spegnerlo, indicando una potenziale nuova strategia terapeutica per questa malattia aggressiva. 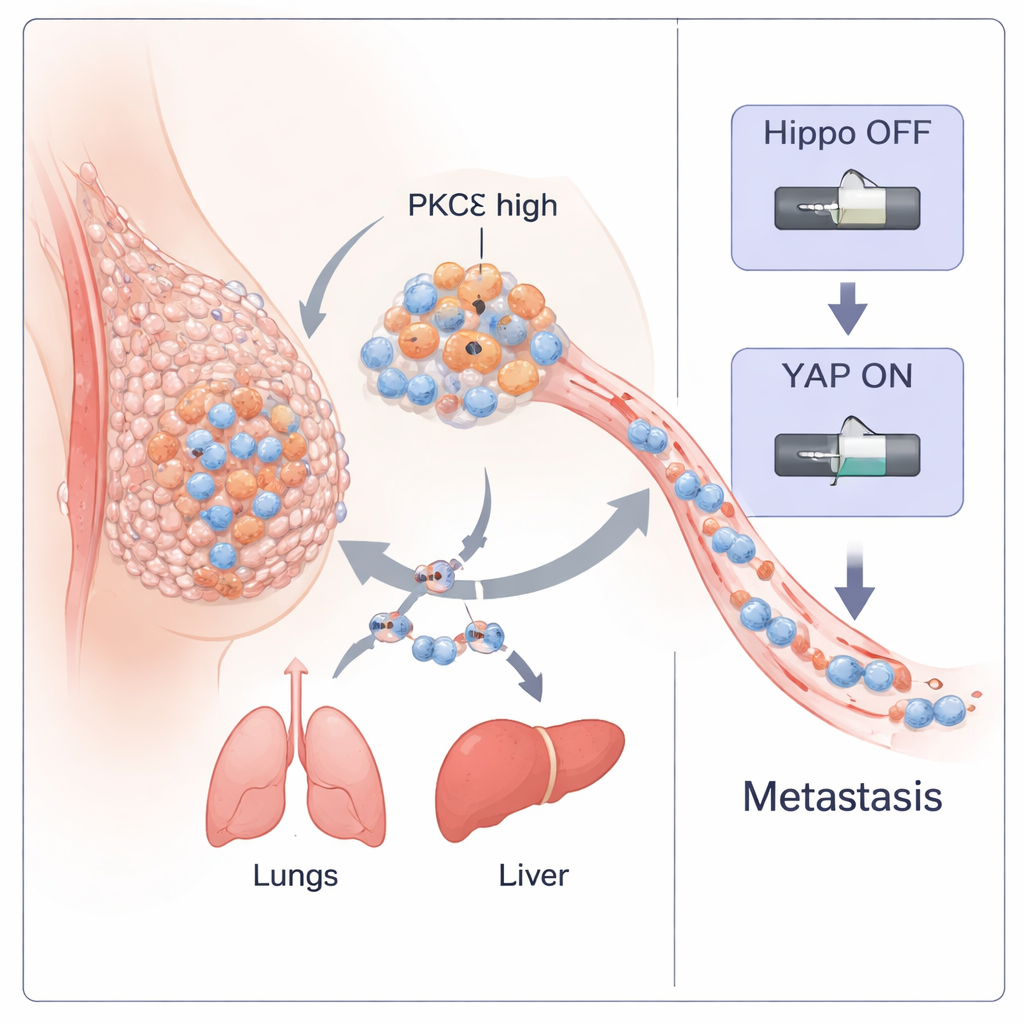
Un fattore nascosto nei tumori mammari aggressivi
Il gruppo ha iniziato analizzando grandi raccolte di dati di pazienti con cancro al seno. Hanno scoperto che il gene che codifica PKCη (PRKCH) è particolarmente elevato in un sottotipo di tumori noto come “claudin‑low”, che si sovrappone fortemente con il TNBC ed è ricco di cellule di tipo staminale, altamente mobili. In più coorti di pazienti, i tumori con alti livelli di PRKCH mostravano marcati segni di transizione epitelio‑mesenchimale (EMT)—un processo in cui cellule precedentemente ordinate allentano i loro attacchi, cambiano forma e diventano più invasive. I livelli di PRKCH erano inoltre più alti nei campioni metastatici rispetto ai tumori primari originari, e la colorazione proteica di tessuti umani TNBC ha mostrato PKCη attivo, perinucleare, nei tumori di grado più elevato e avanzati. Nel complesso, questi risultati suggerivano che PKCη è strettamente legato all’aggressività e alla diffusione tumorale.
Dal piatto di coltura al topo: dimostrare che PKCη alimenta la diffusione
Per testare causa ed effetto, i ricercatori hanno usato l’editing genico CRISPR per rimuovere PKCη da due linee cellulari TNBC altamente metastatiche, una murina (4T1) e una umana (MDA‑MB‑231). Senza PKCη, le cellule tendevano verso uno stato più “epiteliale”: aumentavano proteine di adesione come E‑cadherina ed EpCAM, e riducevano marcatori mesenchimali classici tra cui vimentina e N‑cadherina. Queste cellule prive di PKCη formavano colonie meno numerose e più piccole, migravano e invadevano meno efficacemente, erano più sensibili alla morte cellulare quando staccate e mostravano un netto calo dei tratti di cellule staminali tumorali, incluse meno cellule CD44high/CD24low e ALDH‑positive e ridotta capacità di formazione di sfere. Quando iniettate nei topi, le cellule prive di PKCη hanno generato tumori primari più piccoli e molte meno metastasi a polmoni, fegato, cervello e altri organi; i topi inoltre vivevano più a lungo. Il ripristino di PKCη invertiva questi cambiamenti, confermando che l’enzima promuove attivamente la progressione e la diffusione del TNBC.
Come PKCη dirotta una via di controllo della crescita
Lo studio ha quindi approfondito il meccanismo con cui PKCη esercita questo potere prometastatico. I dati dei pazienti hanno rivelato che i livelli di PKCη aumentano e diminuiscono in tandem con YAP, una proteina regolatrice potente controllata dalla via Hippo—un “freno di sicurezza” cellulare che normalmente limita la crescita. Alti livelli di PRKCH o di YAP1 prevedevano esiti peggiori per i pazienti, e livelli elevati di entrambi insieme erano correlati a una sopravvivenza libera da metastasi a distanza particolarmente bassa. Nelle cellule TNBC, la rimozione di PKCη abbassava i livelli totali di YAP e lo spostava dal nucleo al citoplasma, dove è inattivo. Esperimenti biochimici hanno mostrato che PKCη lega fisicamente YAP e aggiunge specificamente un gruppo fosfato al sito Ser128. Questa modificazione stabilizza YAP e ne favorisce l’ingresso nel nucleo per attivare geni responsabili di EMT, caratteristiche staminali e metastasi. In assenza di PKCη, YAP viene invece fosforilato in altri siti (Ser127 e Ser397) che ne favoriscono il legame con le proteine 14‑3‑3, il sequestro nel citoplasma e infine la degradazione. PKCη aumenta anche PTEN—un freno naturale sull’enzima AKT—mantenendo così bassa l’attività di AKT e sopprimendo le chinasi Hippo a monte che altrimenti inattiverebbero YAP. In questo modo, PKCη attiva direttamente YAP e, indirettamente, mantiene il “freno” Hippo disinserito. 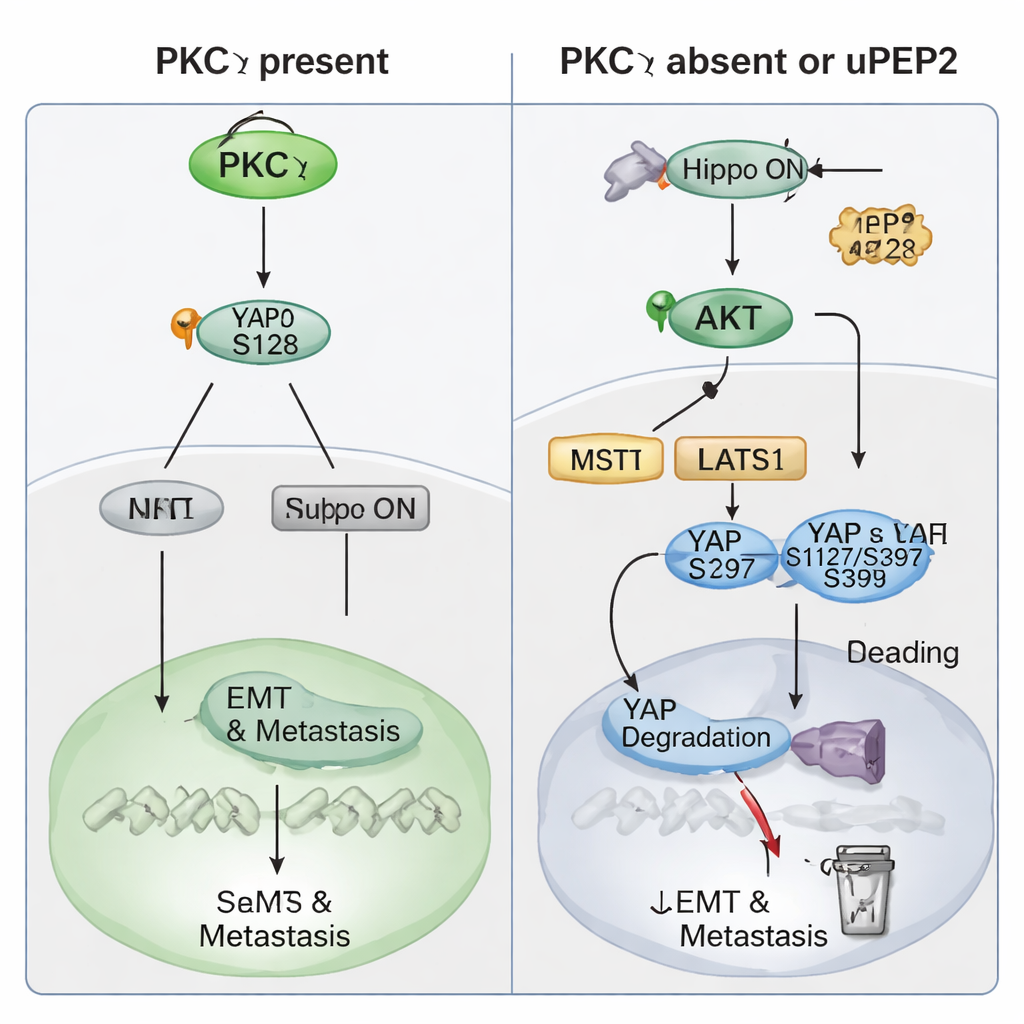
Un piccolo peptide che disarma l’interruttore del cancro
In modo intrigante, il gene PKCη contiene un breve open reading frame a monte (uORF) che codifica un micropeptide chiamato uPEP2. Lavori precedenti avevano mostrato che uPEP2 può legare e inibire PKCη e enzimi correlati. Qui, il trattamento delle cellule TNBC con uPEP2 sintetico ha riprodotto gli effetti del knockout di PKCη: migrazione, invasione e comportamento di tipo staminale sono diminuiti, i marcatori EMT si sono spostati verso un profilo meno aggressivo e i livelli di YAP sono calati mentre le fosforilazioni associate allo stato “off” sono aumentate. Nei tumori murini, uPEP2 ha ridotto PKCη e YAP nei tumori primari, ha aumentato l’inattivazione di YAP ed è stato associato a meno micrometastasi in fegato e polmoni. Meccanisticamente, uPEP2 promuove la degradazione di PKCη, riattiva la via Hippo e spinge YAP verso il sequestro citoplasmatico e la degradazione.
Cosa significa per i trattamenti futuri
Per un lettore non specialista, il messaggio chiave è che i ricercatori hanno identificato PKCη come un perno che aiuta i tumori al seno più aggressivi a distaccarsi, muoversi e colonizzare organi distanti disabilitando un sistema naturale di controllo della crescita e attivando il “pedale dell’acceleratore” YAP. Sopprimendo PKCη o utilizzando il piccolo peptide naturale uPEP2 per degradarlo, sono riusciti a ripristinare il freno di sicurezza Hippo, mettere a tacere YAP e ridurre ampiamente le metastasi in modelli preclinici. Sebbene questo lavoro sia ancora in fase sperimentale e sia stato condotto in linee cellulari e in topi immunodeficienti, mette in evidenza PKCη e la sua interazione con YAP come bersagli promettenti per nuove terapie del TNBC e suggerisce che farmaci simili a uPEP2 potrebbero un giorno aiutare a prevenire o limitare la diffusione di questo cancro difficile da trattare.
Citazione: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Parole chiave: carcinoma mammario triplo negativo, PKC-eta, via Hippo-YAP, transizione epitelio-mesenchimale, metastasi del cancro