Clear Sky Science · it
Serpina3c protegge dalla steatosi epatica associata a disfunzione metabolica nei discendenti indotta dall’esposizione prenatale al prednisone
Perché questa ricerca è importante per i bambini del futuro
Molte donne necessitano di prednisone durante la gravidanza per controllare gravi malattie autoimmuni e infiammatorie. I medici sanno che può salvare la vita della madre, ma si conosce molto meno su come influenzi la salute a lungo termine dei loro figli. Questo studio pone una domanda urgente: assumere prednisone in gravidanza può silenziosamente predisporre il fegato del bambino a sviluppare steatosi epatica in età adulta, soprattutto se combinato con una dieta non salutare? E, in tal caso, esiste un modo per invertire tale rischio?
Un problema epatico in crescita nel mondo
La steatosi epatica associata a disfunzione metabolica, o MASLD, è oggi una delle condizioni epatiche croniche più diffuse, colpendo circa un terzo della popolazione globale e con prospettive di ulteriore aumento. Comprende l’accumulo semplice di grasso nel fegato, l’epatite steatosica infiammatoria, la fibrosi, la cirrosi e perfino il cancro epatico. La MASLD è strettamente legata a obesità, ipertensione e diabete di tipo 2. Sempre più scienziati riconoscono che i semi di questa malattia possono essere piantati prima della nascita, quando il feto in sviluppo è esposto a stress come cattiva nutrizione, inquinamento o farmaci. Questa idea — che gli ambienti precoci della vita plasmano il rischio di malattia per tutta la vita — è nota come “origini dello sviluppo della salute e della malattia.” 
Il prednisone prima della nascita come primo insulto
Per esaminare come il prednisone prenatale influenzi il fegato, i ricercatori hanno trattato ratti e topi gravidi con dosi scelte per imitare i bassi dosaggi clinici usati negli esseri umani. Hanno poi seguito i discendenti prima della nascita e fino alla giovane età adulta. Da soli, i piccoli esposti a prednisone nell’utero erano più piccoli e mostravano già segni di un metabolismo dei grassi alterato nel fegato: più goccioline lipidiche, trigliceridi epatici più elevati e un uso dei grassi per energia più debole. Con la crescita, i loro fegati continuavano a immagazzinare più grasso del normale, anche con una dieta regolare. Quando gli animali sono stati poi sottoposti a una dieta ricca di grassi — l’equivalente di uno stile alimentare occidentale da fast food — le differenze sono diventate drammatiche. I discendenti esposti a prednisone hanno sviluppato una steatosi più grave, infiammazione e, nei maschi, chiari segni di fibrosi. Anche il controllo della glicemia è peggiorato, indicando problemi metabolici più ampi.
Un’importante proteina epatica protettiva che scompare
Approfondendo, il team ha utilizzato profili genici su larga scala per cercare cambiamenti molecolari condivisi nei fegati dei discendenti maschi e femmine. Un gene è emerso in modo netto: Serpina3c, che codifica una proteina secreta appartenente a una famiglia di inibitori enzimatici naturali. In entrambi i sessi, il prednisone prenatale ha ridotto in modo marcato e persistente Serpina3c nel fegato e nel sangue, dalla vita fetale avanzata fino all’età adulta. Quando gli scienziati hanno deliberatamente abbassato Serpina3c solo nel fegato di topi sani, anche quegli animali sono diventati inclini alla steatosi e a un cattivo controllo della glicemia, soprattutto con una dieta ricca di grassi. Al contrario, aumentare Serpina3c nei fegati dei discendenti esposti a prednisone dopo la nascita li ha in gran parte recuperati: i loro fegati accumulavano meno grasso, gestivano meglio il glucosio e mostravano meno infiammazione e fibrosi.
Come il prednisone riconfigura gli interruttori di controllo del fegato
I ricercatori si sono poi chiesti come il prednisone prenatale riduca Serpina3c. Hanno scoperto che la forma attiva del prednisone, il prednisolone, iperattiva il recettore dei glucocorticoidi — una proteina sensibile al farmaco presente nelle cellule epatiche. Questo recettore si associa quindi con un’altra proteina, HDAC3, che compatta il confezionamento del DNA rimuovendo piccole etichette “acetil” dalle proteine istoniche. Sia nei fegati degli animali sia in cellule epatiche in coltura, il prednisolone ha aumentato l’attività del recettore dei glucocorticoidi e di HDAC3 proprio sul gene Serpina3c, eliminando i segni acetilici in un sito chiave chiamato H3K27. Con queste etichette rimosse, l’attività del gene è calata e i livelli proteici di Serpina3c sono diminuiti. Bloccare il recettore o HDAC3, o inibire la deacetilazione, ha ripristinato questi segni acetilici, aumentato Serpina3c e migliorato la gestione dei lipidi e del glucosio nelle cellule epatiche.
Una catena di eventi dannosi all’interno del fegato
La bassa quantità di Serpina3c ha innescato una seconda cascata dannosa. In condizioni normali, Serpina3c aiuta a contenere enzimi come la chymasi che generano l’ormone angiotensina II direttamente nei tessuti. Quando Serpina3c scarseggiava, i livelli e l’attività della chymasi aumentavano, producendo più angiotensina II nel fegato e iperattivando il suo recettore, AT1R, sulle cellule epatiche. Questo aumento locale di ormone è noto per promuovere stress ossidativo, insulino-resistenza, accumulo di grasso, infiammazione e formazione di cicatrici. Sia negli animali esposti a prednisone sia nei topi con silenziamento epatico specifico di Serpina3c, la via chymasi–angiotensina II–AT1R è risultata attivata, e geni chiave che normalmente supportano la combustione dei grassi e l’assorbimento del glucosio erano soppressi. Ripristinare Serpina3c dopo la nascita ha attenuato questa via e ripristinato un metabolismo più sano. 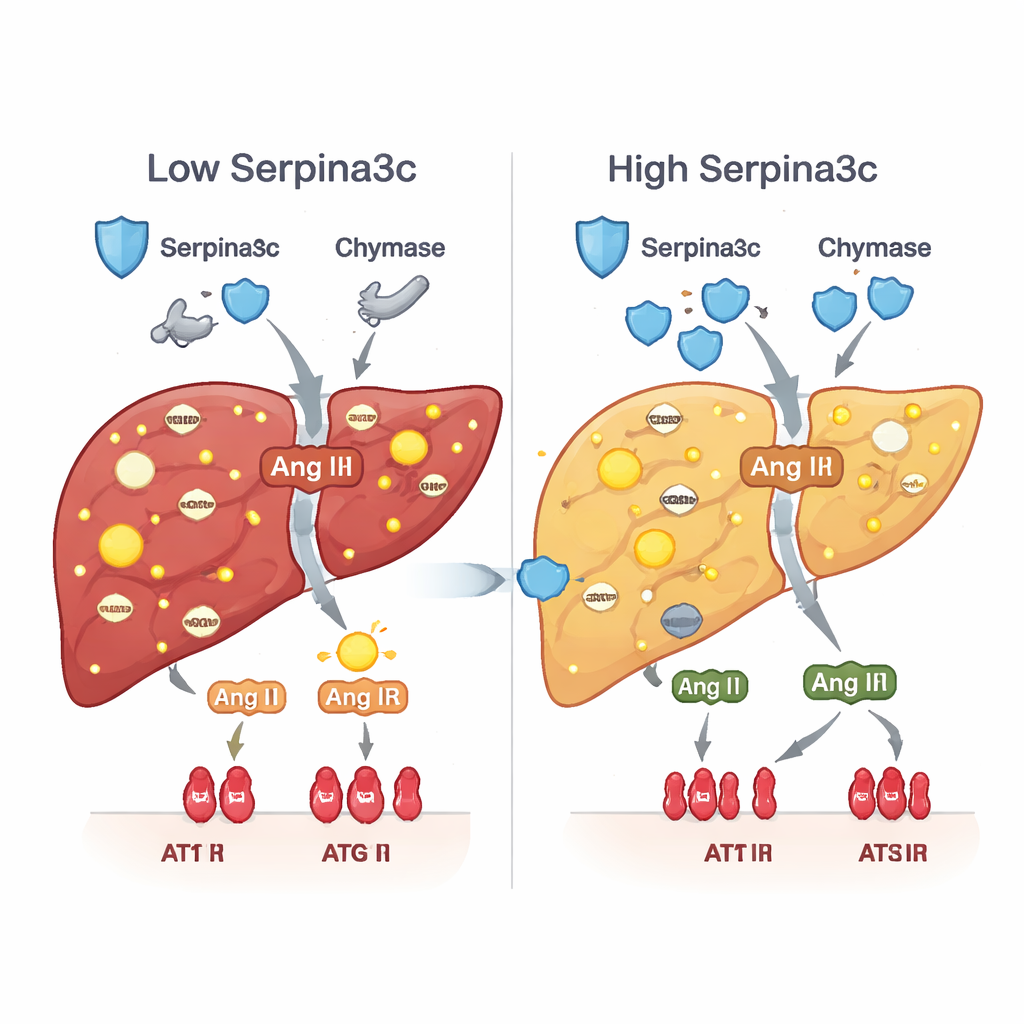
Cosa significa per pazienti e famiglie
Per i non specialisti, il messaggio principale è che i farmaci assunti durante la gravidanza possono lasciare un’impronta molecolare sul fegato in sviluppo che persiste fino all’età adulta. In questo studio, il prednisone ha agito come un “primo insulto”, riducendo una proteina protettiva (Serpina3c) attraverso cambiamenti epigenetici — marchi chimici sulle proteine che avvolgono il DNA — in modo che un successivo “secondo insulto” come una dieta ricca di grassi scatenasse più facilmente la malattia del fegato grasso. Il lato incoraggiante è che questo rischio non era definitivo: ripristinare Serpina3c nel fegato dopo la nascita ha ridotto notevolmente il danno epatico. Pur essendo risultati ottenuti in roditori, sollevano questioni importanti su come monitorare e supportare i bambini le cui madri hanno richiesto prednisone in gravidanza, e indicano Serpina3c e il sistema chymasi–angiotensina II come promettenti bersagli futuri per prevenire o trattare la steatosi epatica che ha origine prima della nascita.
Citazione: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
Parole chiave: prednisone prenatale, fegato grasso, epigenetica, Serpina3c, origini dello sviluppo