Clear Sky Science · it
Cellule T CD4 citotossiche: origine, funzioni biologiche, malattie e bersagli terapeutici
Quando le cellule helper diventano assassine
Il sistema immunitario viene spesso descritto con ruoli semplici: alcune cellule individuano il pericolo, altre combattono. Questo articolo si concentra su un gruppo sorprendente che sfuma questa distinzione: le cellule T CD4 citotossiche. A lungo note soprattutto come cellule “helper” che coordinano le difese, alcune cellule CD4 possono trasformarsi esse stesse in effettori armati. Capire come nascono queste cellule camaleontiche, cosa fanno e come contribuiscono a malattie come il cancro, le infezioni virali, le patologie autoimmuni e le malattie cardiovascolari potrebbe aprire nuove strade per rafforzare l’immunità o attenuare l’infiammazione dannosa. 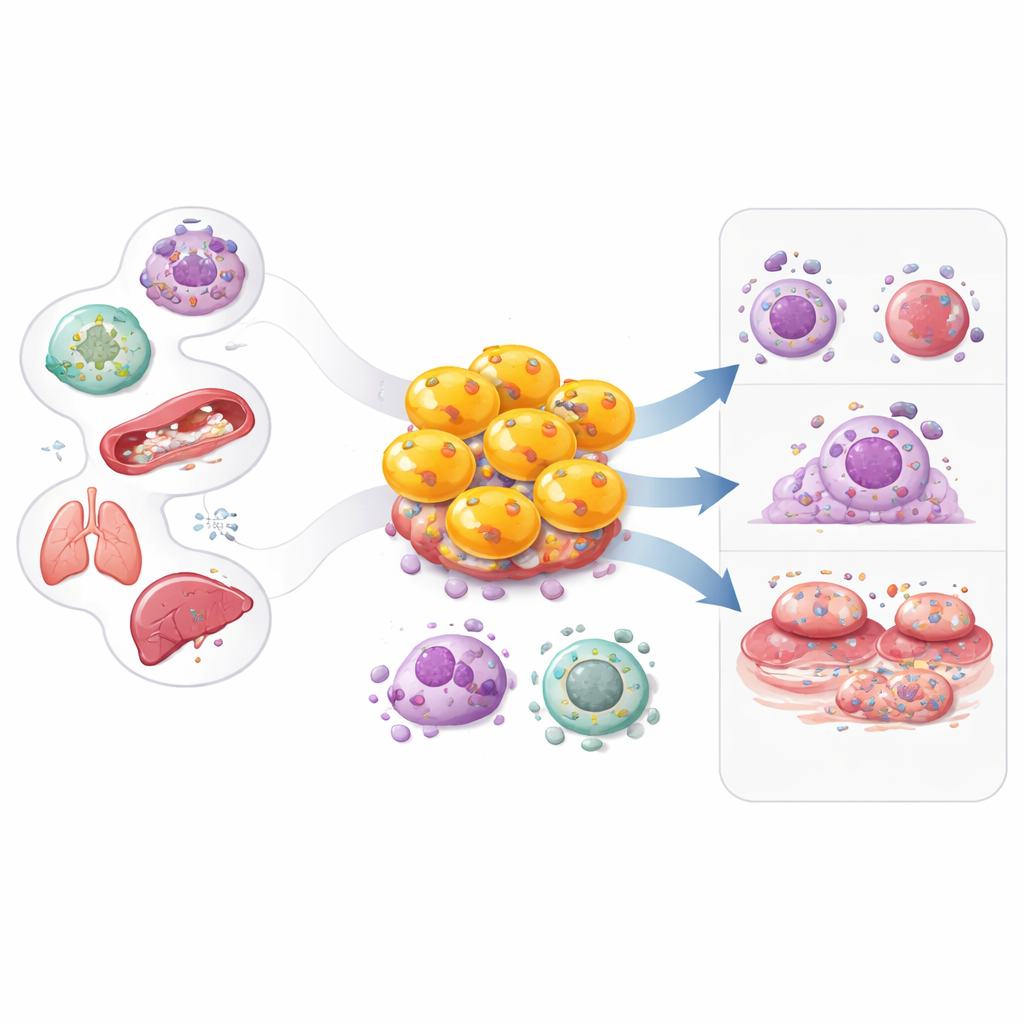
Come è emerso un difensore flessibile
I primi studi alla fine degli anni ’70 e negli anni ’80 mostrarono che una frazione di cellule T CD4 poteva uccidere direttamente altre cellule che esprimevano i segnali immunitari appropriati, in modo simile alle classiche cellule T CD8 “killer”. All’inizio molti scienziati considerarono questi risultati come artefatti dei sistemi di coltura. Nel corso dei decenni successivi, modelli animali di influenza e studi su pazienti con artrite reumatoide, malattie cardiache, infezioni virali croniche e cancro hanno confermato che le cellule T CD4 citotossiche esistono davvero e hanno rilevanza clinica. Strumenti moderni come la citometria a flusso e il sequenziamento dell’RNA a singola cellula hanno mappato la loro diversità, rivelando che queste cellule si espandono nelle infezioni croniche, nei tumori, nell’invecchiamento e in diverse malattie infiammatorie, dove possono persistere per lunghi periodi.
Da dove vengono questi helper assassini
La review spiega che le cellule T CD4 citotossiche probabilmente derivano soprattutto in due modi. Un’ipotesi è che somiglino in parte alle cellule natural killer perché condividono molti recettori di superficie e molecole citotossiche, suggerendo un percorso di sviluppo correlato. Tuttavia, prove crescenti favoriscono un’altra visione: la maggior parte di queste cellule inizia come normali cellule helper CD4 — in particolare di tipo Th1 — che, sotto esposizione cronica all’antigene e forti segnali infiammatori, si “riqualificano” in uno stato citotossico terminalmente differenziato. Questo cambiamento è regolato da una rete di stimoli esterni (come le interleuchine 2, 7 e 15) e di interruttori intracellulari (inclusi Runx3, T-bet, Eomes, Blimp-1 e Hobit) che insieme attivano i geni per perforina, granzimi e ligandi induttori di morte.
Come uccidono e modulano l’infiammazione
Funzionalmente, le cellule T CD4 citotossiche operano attraverso due principali vie d’attacco. Nella via dei granuli, formano un contatto stretto con la cellula bersaglio e rilasciano pacchetti contenenti perforina e granzimi, che perforano la membrana e innescano la morte programmata dall’interno. Nella via dei ligandi di morte, espongono molecole come Fas ligand e TRAIL sulla loro superficie, che si legano ai recettori corrispondenti sulle cellule bersaglio per avviare un programma di suicidio interno. Oltre alla citotossicità diretta, queste cellule secernono messaggeri infiammatori come interferone-gamma, fattore di necrosi tumorale e fattori di crescita che reclutano e attivano altre cellule immunitarie, rimodellano i vasi e alterano il comportamento tessutale locale. A differenza degli helper classici, spesso sono resistenti ai normali «freni» come le cellule T regolatorie e sono meno inclini all’apoptosi, il che permette loro di accumularsi nelle malattie croniche. 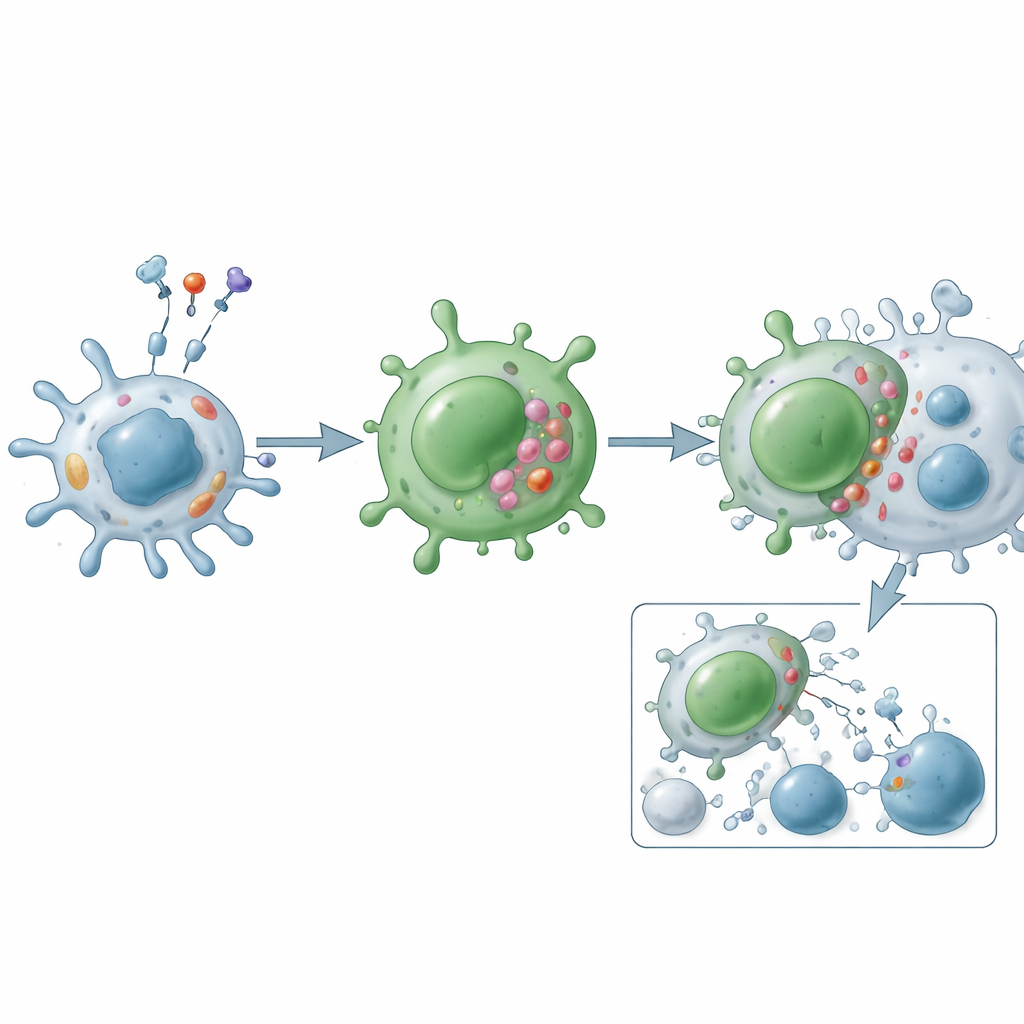
Alleati nelle infezioni e nel cancro, nemici in autoimmunità e malattia cardiaca
Questo comportamento a doppio taglio si manifesta in molte condizioni. Nell’epatite cronica B, nell’HIV e nella COVID-19, le cellule T CD4 citotossiche aiutano a controllare i virus quando i killer CD8 sono esausti, e la loro presenza può associarsi a un migliore controllo o recupero. Nei tumori solidi e nei tumori del sangue, possono riconoscere direttamente cellule tumorali che espongono i segnali immunitari o segnali di stress appropriati e migliorare le risposte alle immunoterapie come gli inibitori dei checkpoint e i trattamenti con CAR-T. Allo stesso tempo, questi stessi meccanismi possono causare danno: nel lupus, nell’artrite reumatoide, nelle malattie infiammatorie intestinali, nella malattia coronarica, nella fibrillazione atriale, nell’arterite a cellule giganti e nel rigetto dei trapianti, le cellule T CD4 citotossiche espanse infiltrano i tessuti, danneggiano vasi o organi e amplificano un’infiammazione persistente, spesso correlata a una prognosi peggiore.
Trasformare uno strumento rischioso in una terapia
Poiché le cellule T CD4 citotossiche possono essere sia protettive sia distruttive, l’articolo mette in luce strategie terapeutiche emergenti volte a modulare finemente questa popolazione invece di eliminarla. Un approccio consiste nell’attenuare la loro attività dannosa con inibitori selettivi che prendono di mira recettori costimolatori (come OX40 o 4-1BB), citochine infiammatorie, canali ionici o vie di sopravvivenza. Un altro è sfruttare il loro potere citotossico nelle terapie adottive cellulari, incluse cellule T modificate geneticamente e CAR-T, dove le cellule CD4 citotossiche spesso mostrano una persistenza superiore rispetto ai prodotti composti solo da CD8. Una terza strategia propone di reindirizzare cellule T CD4 killer di lunga durata e specifiche per virus verso i tumori mediante vaccini o peptidi derivati da patogeni presentati dalle cellule tumorali. Queste linee di ricerca pongono le cellule T CD4 citotossiche non solo come una curiosità biologica, ma come una leva centrale per future terapie in grado di potenziare in modo più preciso la difesa contro infezioni e cancro riducendo l’infiammazione dannosa per i tessuti.
Una nuova leva per le future terapie immunitarie
Per i non specialisti, il messaggio chiave è che le cellule T CD4 “helper” sono molto più versatili di quanto si pensasse: alcune possono trasformarsi in veri e propri killer armati che ci proteggono da infezioni persistenti e tumori, ma che possono anche favorire l’autoimmunità, il danno vascolare e il rigetto dei trapianti. La review sostiene che imparare a monitorare queste cellule, prevedere quando saranno di aiuto o dannose e modulare il loro comportamento con farmaci o terapie ingegnerizzate potrebbe rimodellare il trattamento di molte malattie croniche — dall’epatite e dall’HIV all’artrite, alla colite, alle malattie cardiache e alle leucemie. Piuttosto che limitarsi ad alzare o abbassare l’attività del sistema immunitario, le future terapie potranno sempre più guidare tipi cellulari potenti come le cellule T CD4 citotossiche verso bersagli benefici e lontano dai nostri tessuti.
Citazione: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Parole chiave: cellule T CD4 citotossiche, plasticità delle cellule immunitarie, infiammazione cronica, immunoterapia oncologica, malattia autoimmune