Clear Sky Science · it
IFFO1 inibisce il cancro al seno coordinando la fissione mitocondriale e la sintesi degli acidi grassi tramite l’asse LaminA/C-PGC1α
Perché questa ricerca è importante
Il cancro al seno resta una delle principali cause di morte per cancro nelle donne, in larga parte perché alcuni tumori continuano a crescere, diffondersi e sfuggire alle terapie attuali. Questo studio rivela un “freno” cellulare finora poco considerato, chiamato IFFO1, che rallenta il cancro al seno domando due motori centrali della crescita tumorale: le centrali energetiche della cellula, i mitocondri, e la sua capacità di produrre e immagazzinare lipidi. Comprendere questo freno offre una nuova prospettiva per terapie che potrebbero funzionare in diversi sottotipi di cancro al seno.
Un guardiano nascosto nelle cellule mammarie
I ricercatori hanno iniziato esaminando campioni di 30 donne con cancro al seno e grandi banche dati pubbliche sul cancro. Hanno osservato che i livelli della proteina IFFO1 erano costantemente più bassi nei tessuti tumorali rispetto al tessuto mammario normale adiacente. Più avanzato era lo stadio del tumore, minore era la presenza di IFFO1, e i pazienti i cui tumori esprimevano livelli più alti di IFFO1 tendevano a vivere più a lungo. In colture di cellule di cancro al seno, forzare l’espressione di IFFO1 riduceva drasticamente la loro capacità di crescere, dividersi e migrare — comportamenti necessari per l’espansione e la diffusione tumorale. IFFO1 attenuava inoltre un programma cellulare noto come transizione epitelio–mesenchimale, che aiuta le cellule tumorali a staccarsi e invadere altri tessuti.
Calmare centrali energetiche iperattive
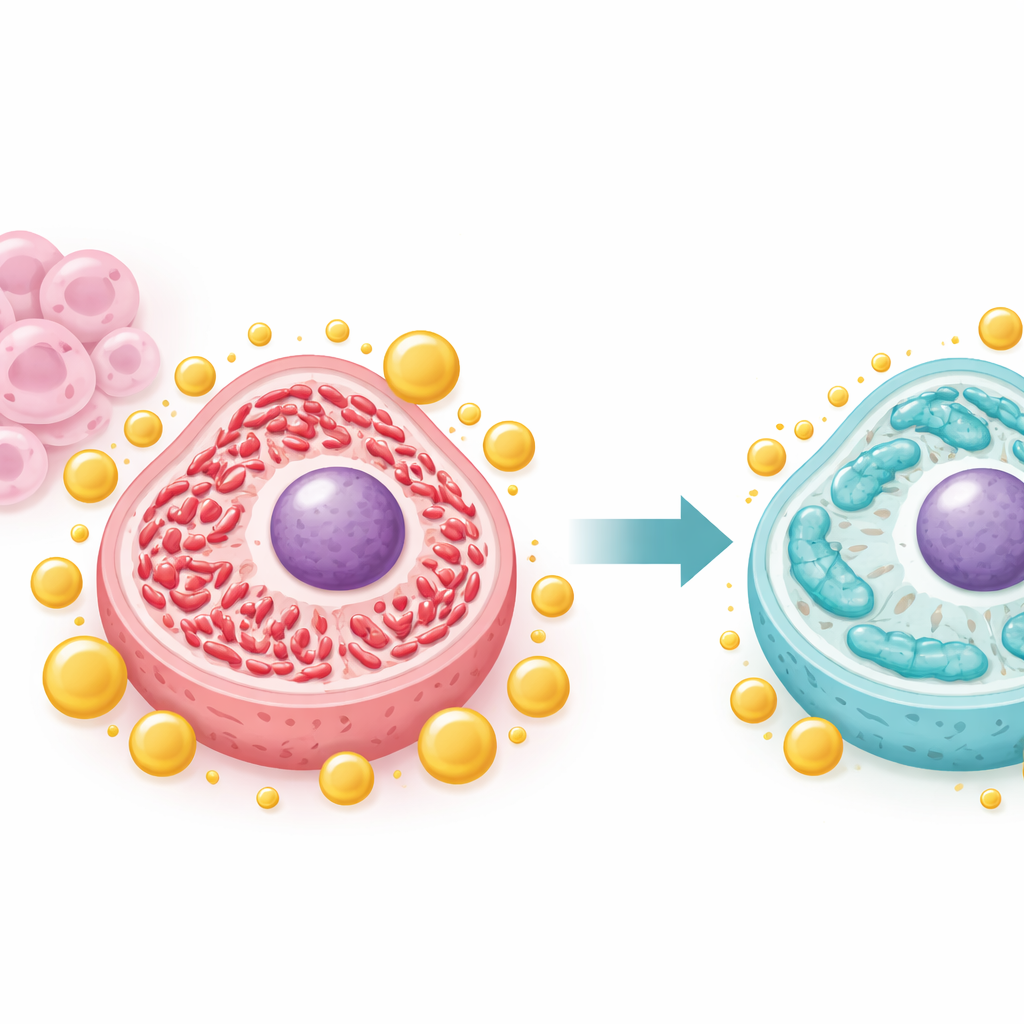
Le cellule tumorali spesso rimodellano i loro mitocondri, le piccole centrali energetiche intracellulari, per alimentare una crescita rapida. Il team ha dimostrato che IFFO1 sposta questo equilibrio da uno stato fortemente frammentato di «fissione» verso uno stato più allungato di «fusione», generalmente associato a mitocondri più sani e stabili. Quando IFFO1 era abbondante, proteine chiave della fissione come Drp1 e Fis1 diminuivano, mentre le proteine della fusione aumentavano. La microscopia ha rivelato mitocondri più lunghi e meno frammentati, e le misure del DNA mitocondriale e della produzione di energia si riducevano rispetto ai livelli abnormally elevati osservati nelle cellule aggressive. Questi cambiamenti suggeriscono che IFFO1 impedisce ai mitocondri di entrare in una configurazione iperattiva che sostiene la crescita tumorale incontrollata.
Tagliare la linea di approvvigionamento lipidico
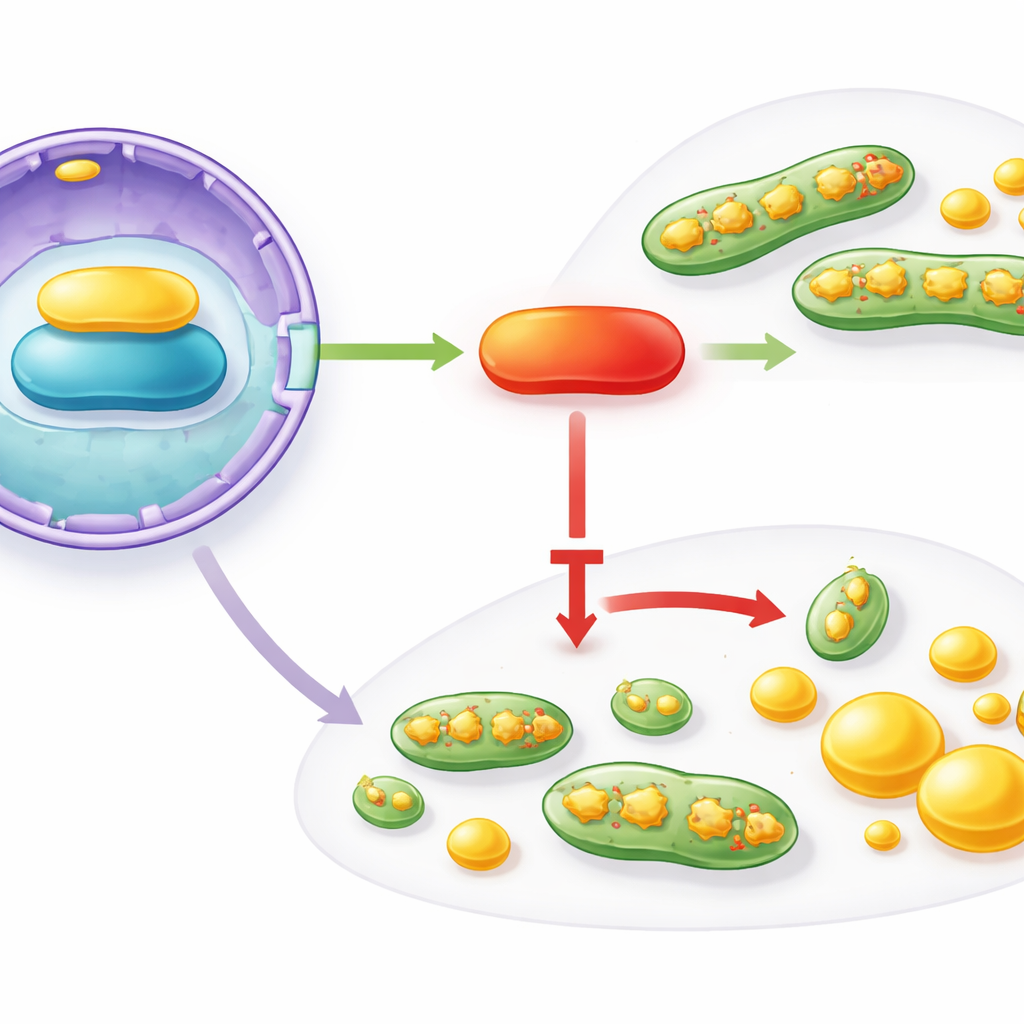
I tumori in rapida crescita non necessitano solo di energia; richiedono anche un flusso costante di lipidi per costruire nuove membrane e molecole di segnalazione. Lo studio ha rilevato che IFFO1 sopprime anche questo acceleratore metabolico. Nelle cellule con IFFO1 sovraespresso, proteine centrali per la sintesi dei lipidi — tra cui FASN, SREBP‑1, SCD1 e altre — risultavano ridotte. Test enzimatici hanno confermato una minore attività sintetica di lipidi, e saggi chimici hanno evidenziato cali di acidi grassi liberi, trigliceridi e colesterolo. Coloranti di imaging che evidenziano le riserve lipidiche hanno mostrato meno goccioline lipidiche e una diminuzione complessiva dei grassi neutri all’interno delle cellule tumorali. Al contrario, l’aumento della proteina di fissione Drp1 produceva l’effetto opposto, potenziando la produzione di lipidi, mentre il silenziamento di Drp1 la riduceva — a sostegno di un legame diretto tra la forma mitocondriale e l’approvvigionamento lipidico nel cancro.
Una catena di segnalazione dal nucleo ai mitocondri
Come fa IFFO1 a orchestrare questi ampi cambiamenti? Gli autori hanno tracciato una catena di interazioni che parte dal nucleo cellulare e arriva ai mitocondri e alla macchina di sintesi lipidica. IFFO1 si lega fisicamente a una proteina strutturale dell’involucro nucleare chiamata Lamin A/C, incrementandone i livelli. Lamin A/C, a sua volta, sostiene l’attività di PGC1α, un regolatore maestro che controlla la salute mitocondriale e il metabolismo. Nei tessuti e nelle cellule di cancro al seno, sia Lamin A/C sia PGC1α risultavano ridotti, rispecchiando la perdita di IFFO1. Quando gli scienziati aumentavano artificialmente IFFO1, Lamin A/C e PGC1α aumentavano, la fissione mitocondriale diminuiva e la sintesi lipidica si indeboliva. L’abbattimento di Lamin A/C annullava questi benefici, ma il ripristino di PGC1α li riportava, identificando un asse funzionale IFFO1 → Lamin A/C → PGC1α che limita i cambiamenti mitocondriali e lipidici favorevoli al tumore.
Testare il freno negli animali viventi
Per valutare se questi effetti cellulari si traducono in tumori reali, il team ha impiantato cellule umane di cancro al seno con o senza IFFO1 sovraespresso nei topi. I tumori con IFFO1 aumentato crescevano più lentamente, pesavano meno al termine dell’esperimento e mostravano minori segni di accumulo lipidico. In un modello separato, in cui cellule tumorali venivano iniettate nel circolo sanguigno per formare metastasi polmonari, le cellule che sovraproducevano IFFO1 formarono un numero nettamente inferiore di noduli tumorali polmonari. Le analisi tissutali di questi topi confermavano i risultati delle colture cellulari: livelli più alti di Lamin A/C e PGC1α, minore fissione mitocondriale e ridotta sintesi lipidica.
Cosa significa per le terapie future
Nel complesso, il lavoro presenta IFFO1 come un soppressore tumorale multilivello che connette l’impalcatura strutturale della cellula, le sue centrali energetiche e la macchina per la sintesi dei lipidi. Stabilizzando Lamin A/C e potenziando PGC1α, IFFO1 impedisce ai mitocondri di frammentarsi eccessivamente e taglia l’eccessiva produzione di lipidi di cui le cellule tumorali dipendono. Per i non specialisti, il messaggio chiave è che questa proteina funziona come un freno interno sia sull’energia sia sui mattoni con cui il cancro al seno cresce e si diffonde. Farmaci che aumentino i livelli di IFFO1 o ne mimino gli effetti sull’asse Lamin A/C–PGC1α potrebbero un giorno offrire nuove opzioni, specialmente per forme aggressive o resistenti alle terapie del cancro al seno.
Citazione: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Parole chiave: cancro al seno, dinamiche mitocondriali, sintesi degli acidi grassi, metabolismo tumorale, via PGC1α