Clear Sky Science · it
Il controllo oncogenico della sintesi dei nucleotidi
Perché le cellule tumorali si interessano ai mattoni
Il cancro viene spesso descritto come un insieme di cellule che non smettono di dividersi. Ma per copiarsi, queste cellule hanno bisogno di un rifornimento costante di piccoli mattoni chiamati nucleotidi, che costituiscono il DNA e l'RNA e partecipano anche al funzionamento energetico di molti processi cellulari. Questa rassegna spiega come i geni che causano il cancro rimodellano la chimica cellulare per mantenere alta la produzione di nucleotidi, come i tumori passano tra diverse modalità per ottenere queste molecole e come i medici possono sfruttare questi stratagemmi con farmaci vecchi e nuovi.
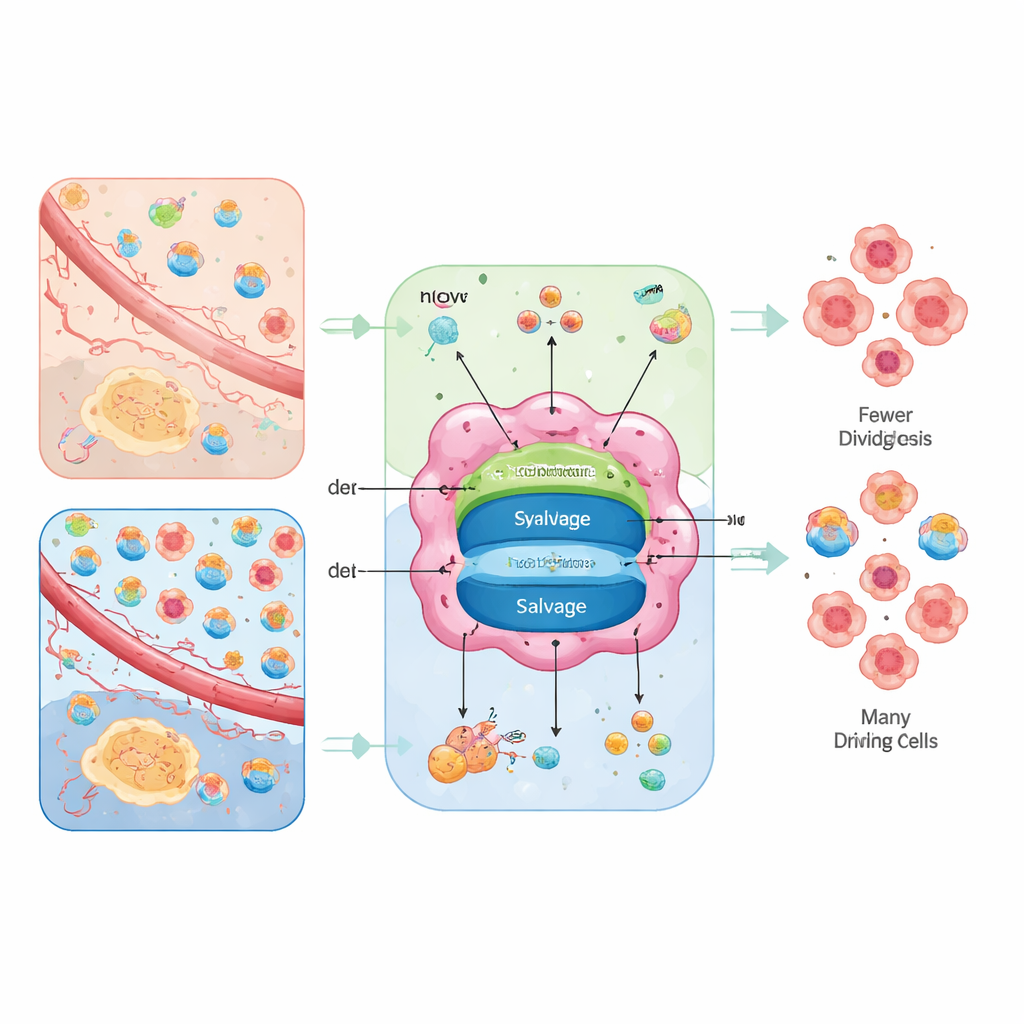
Due strade per gli stessi mattoni
Le cellule possono sintetizzare i nucleotidi da zero oppure riciclarli. La via “da zero”, chiamata sintesi de novo, costruisce gli anelli a partire da nutrienti di base come glucosio, amminoacidi, anidride carbonica e bicarbonato, attraverso reazioni multi-step ad alto consumo energetico. La via di riciclo, detta salvage, recupera basi e nucleosidi degradati dall’esterno o dai rifiuti cellulari e li reintegra in nucleotidi utili a un costo energetico molto inferiore. I tumori usano entrambe le opzioni, ma il bilancio tra esse dipende dalla disponibilità energetica interna e da ciò che il tessuto circostante mette a disposizione.
Come l’ambiente tumorale indirizza la scelta
Gli autori inquadrano la fornitura di nucleotidi come un problema di “instradamento modellato dall’ambiente”. Nelle regioni poco nutritive, dove gli amminoacidi sono presenti ma i nucleosidi liberi scarseggiano, le cellule tumorali fanno forte affidamento sulle vie de novo e diventano vulnerabili ai farmaci che bloccano questi passaggi. Nelle regioni meglio perfuse, dove il sangue porta abbondanti nucleosidi o dove i mitocondri sono compromessi, i tumori possono contare maggiormente sul salvage, risultando invece sensibili a inibitori dei trasportatori che impediscono l’ingresso dei nucleosidi. Quando entrambe le opzioni sono disponibili, i tumori mostrano flessibilità metabolica e possono eludere singoli farmaci; quando entrambe sono chiuse, le cellule si arrestano nella replicazione del DNA, accumulano danni e possono andare incontro a morte o differenziarsi in stati più maturi e meno aggressivi.
Linee di supporto nascoste che alimentano l’offerta di nucleotidi
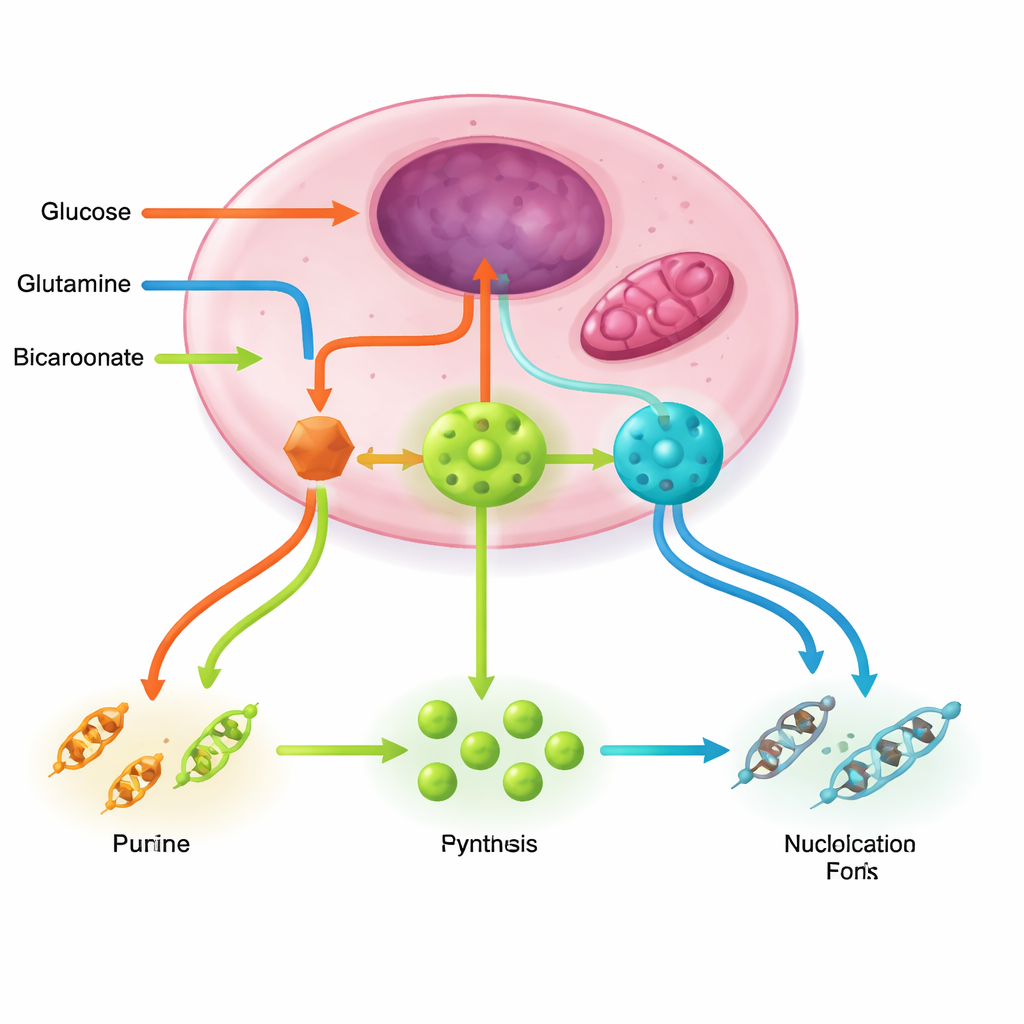
Per mantenere attive le “fabbriche” di nucleotidi servono diversi circuiti di supporto. La via del pentoso fosfato fornisce lo scheletro zuccherino e il potere riducente; la glutammina e il ciclo energetico nei mitocondri forniscono azoto e aspartato; la chimica di serina, glicina e folati dona unità monocarboniose che completano gli anelli; il bicarbonato apporta carboni essenziali. Driver oncogeni come PI3K–AKT–mTORC1, RAS–MAPK e MYC attivano congiuntamente queste vie, aumentano gli enzimi chiave e persino assemblano complessi multi-enzimatici che convogliano efficacemente intermedi instabili. Al contrario, sensori di stress come LKB1–AMPK e p53 agiscono normalmente come freni, riducendo la produzione di nucleotidi quando l’energia o l’integrità del DNA sono minacciate—freni che molti tumori disattivano.
Vecchia chemioterapia, nuova logica metabolica
Poiché le cellule in rapida crescita dipendono fortemente dai nucleotidi, alcune delle prime chemioterapie hanno preso di mira questa debolezza. Farmaci classici come metotrexato, 5‑fluorouracile, citarabina, gemcitabina e vari analoghi delle purine ostruiscono l’uso dei folati, inibiscono enzimi specifici o si comportano da falsi mattoni che avvelenano DNA e RNA. La rassegna rilegge questi medicinali alla luce del modello di instradamento, spiegando perché effetti collaterali e resistenza sono comuni: anche i tessuti non tumorali necessitano di nucleotidi e i tumori spesso reindirizzano il flusso attraverso il salvage o vie parallele quando un nodo è bloccato.
Strategie di nuova generazione e questioni aperte
Le strategie più recenti puntano a essere più selettive colpendo gli anelli della rete più sbilanciati verso il cancro. Sono in sviluppo farmaci sperimentali contro enzimi mitocondriali della via monocarboniosa come MTHFD2, l’enzima pirimidinico DHODH e enzimi delle purine come IMPDH e PAICS, spesso in combinazione con inibitori dei trasportatori del salvage. Gli autori propongono marcatori pratici—come livelli dei trasportatori, densità dei vasi sanguigni, efficienza mitocondriale ed espressione di specifici enzimi metabolici—per stabilire quali tumori dipendono più dalla sintesi de novo o dal salvage e per abbinare i pazienti a terapie mirate alle vie. Guardando avanti, evidenziano domande chiave, tra cui come queste rotte cambino nello spazio e nel tempo all’interno dei tumori reali, come le cellule immunitarie e stromali circostanti modulino la disponibilità di nucleotidi e come progettare schemi di trattamento tollerabili che sfruttino lo stress da replicazione senza sovraccaricare i tessuti sani. Insieme, questo lavoro sostiene che comprendere e colpire il metabolismo dei nucleotidi potrebbe trasformare un requisito fondamentale della divisione cellulare in una leva potente e personalizzata contro il cancro.
Citazione: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Parole chiave: metabolismo dei nucleotidi, metabolismo del cancro, sintesi de novo, vie di salvataggio, terapie metaboliche