Clear Sky Science · it
Profilo trascrittomico di cellule tumorali e ospiti co-coltivate identifica l’ipossia come motore dell’effetto anti-proliferativo delle cellule muscolari scheletriche sulle cellule tumorali
Perché alcuni tessuti resistono alla diffusione del cancro
Il cancro diventa di solito mortale quando le cellule tumorali lasciano il sito d’origine e si stabiliscono in organi distanti. Curiosamente, alcuni tessuti, come i polmoni, sono punti di arrivo frequenti, mentre altri, come il muscolo scheletrico, sono quasi mai colonizzati nonostante rappresentino una grande parte del peso corporeo. Questo studio pone una domanda semplice ma importante per pazienti e medici: che cosa rende il muscolo un terreno così sfavorevole per la crescita delle cellule tumorali, e capire questa difesa naturale potrebbe cambiare il modo in cui consideriamo il trattamento delle metastasi?
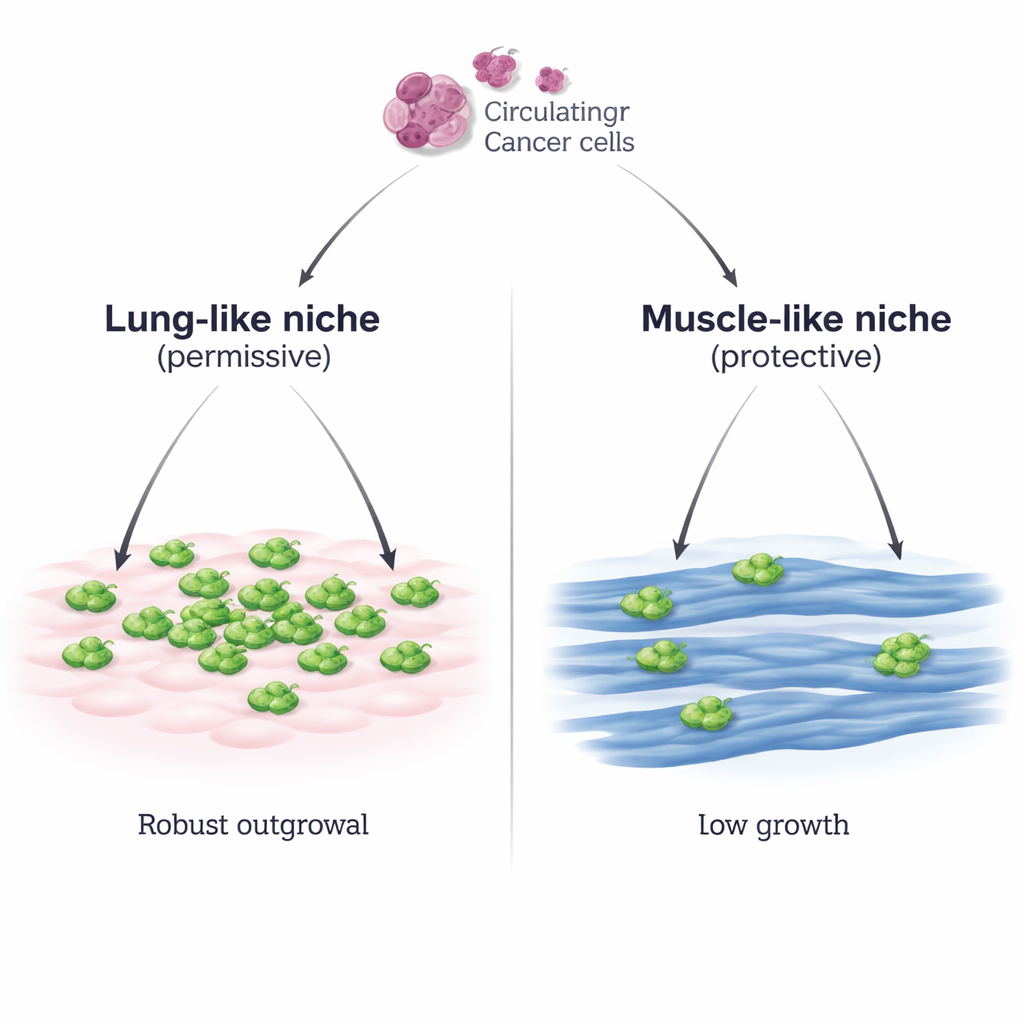
Due ‘quartieri’ per le cellule tumorali in viaggio
I ricercatori hanno costruito un sistema di laboratorio controllato che imita due diversi ambienti che una cellula di carcinoma mammario potrebbe incontrare: un ambiente simile al polmone composto da cellule connettivali polmonari (MLg) e un ambiente simile al muscolo formato da fibre muscolari scheletriche mature (miotubi C2C12). Hanno posto cellule di carcinoma mammario murino sopra ogni strato e osservato cosa accadeva. Sulle cellule simili al polmone, le cellule tumorali si attaccavano bene e poi si moltiplicavano rapidamente, formando macchie dense. Sulle cellule muscolari, si attaccavano altrettanto bene, ma la loro crescita restava scarsa e lenta, anche aumentando molto il numero iniziale di cellule tumorali o usando una seconda linea tumorale mammaria. Una linea di muscolo scheletrico separata (Sol8) ha mostrato la stessa capacità di frenare la crescita tumorale, sottolineando che si tratta di una proprietà generale delle cellule muscolari più che di una caratteristica di una singola linea cellulare.
Come le cellule tumorali e dell’ospite riorganizzano la loro attività
Per capire cosa stava accadendo all’interno delle cellule, il team ha isolato le cellule tumorali e quelle dell’ospite da queste colture miste e ha sequenziato il loro RNA, una lettura di quali geni sono accesi o spenti. Le cellule tumorali posate sui miotubi subirono cambiamenti dell’attività genica molto più estesi rispetto a quelle cresciute sulle cellule polmonari, suggerendo che l’ambiente muscolare le costringe ad adattarsi in modo marcato. Nell’ambiente muscolare, le cellule tumorali attivavano programmi legati a caratteristiche simili al muscolo, al metabolismo energetico e, sorprendentemente, a risposte tipiche dell’ipossia. Allo stesso tempo, i programmi genetici abituali che guidano la rapida divisione cellulare venivano depotenziati. Al contrario, le cellule tumorali sulle cellule polmonari mantenevano un profilo fortemente orientato alla crescita e necessitavano di molta meno riprogrammazione, coerente con l’idea che il nicchia simile al polmone sia permissiva e facilmente sfruttabile dalle cellule tumorali.
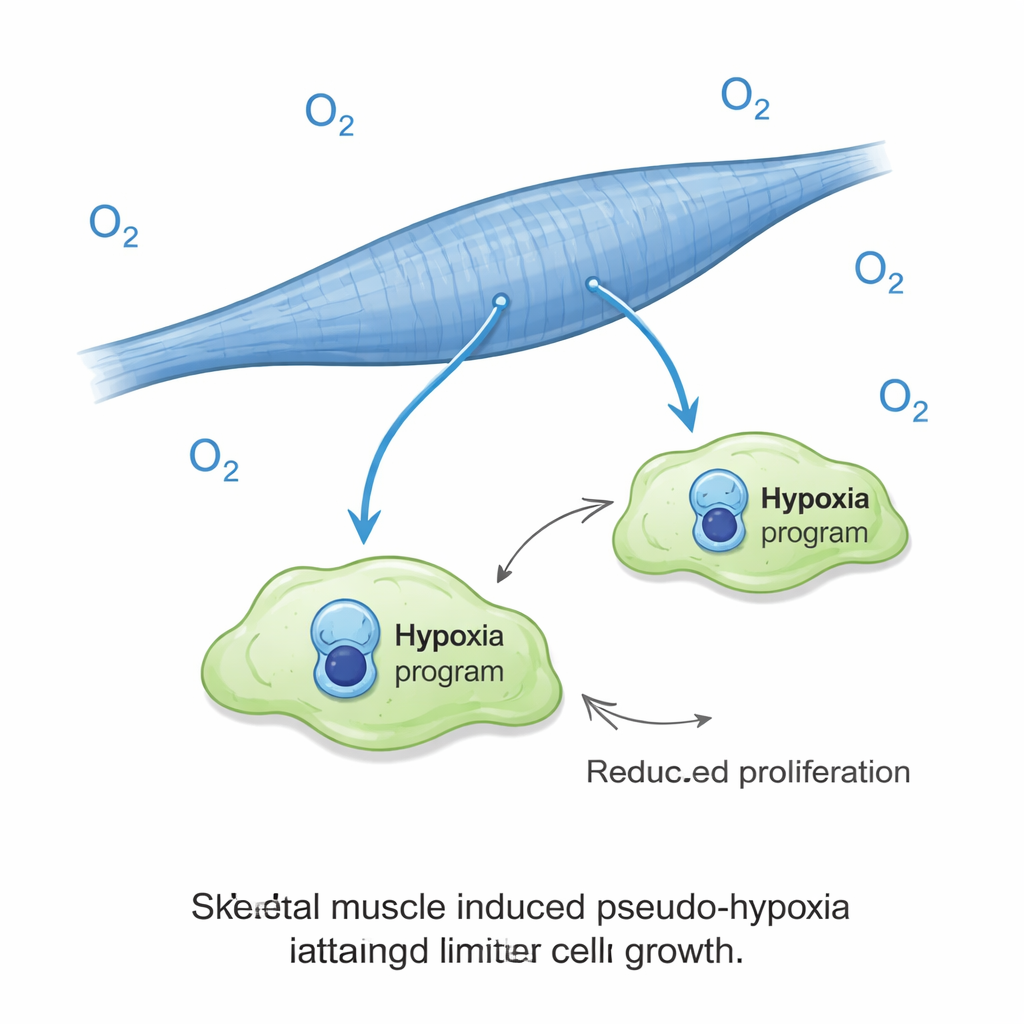
Un ruolo sorprendente per i segnali da basso ossigeno
Una delle scoperte più sorprendenti è stata che le cellule tumorali sui miotubi attivavano una firma genica simile all’ipossia nonostante fossero coltivate in condizioni normali di ossigeno. Nella maggior parte dei tumori, l’ipossia è un cattivo segno, di solito associato a comportamento aggressivo e risultati peggiori. Qui, era collegata all’opposto: scarsa crescita. Gli scienziati hanno quindi esposto le colture a vera bassa ossigenazione e hanno scoperto che questo quasi annullava l’espansione delle cellule tumorali sul muscolo, mentre in realtà aumentava la crescita tumorale nelle colture simili al polmone. In altre parole, lo stesso segnale che normalmente aiuta i tumori a prosperare divenne un freno quando le cellule tumorali si trovavano in un ambiente muscolare. Questo effetto dell’ossigeno non sembrava spiegabile con semplici cambiamenti di lattato, acidità o disponibilità di zuccheri nel mezzo di coltura.
Più che semplici fattori secreti
Il gruppo ha anche testato se semplici sostanze solubili rilasciate dalle cellule muscolari potessero spiegare il loro effetto protettivo. Aggiungere lattato extra, modificare l’acidità, cambiare i livelli di glucosio o far crescere le cellule tumorali in un mezzo che aveva precedentemente immerso cellule muscolari non riproduceva la forte soppressione osservata nelle co-colture a contatto diretto. Questo suggerisce che il contatto fisico ravvicinato, o segnali a brevissima distanza sulla superficie cellulare, siano la chiave di come le cellule muscolari spingono le cellule tumorali in uno stato di bassa crescita, possibilmente dormiente. È interessante notare che le cellule muscolari rimasero relativamente stabili nella loro attività genica di fronte al cancro, mentre le cellule polmonari venivano riprogrammate più facilmente, evidenziando il muscolo come un tessuto robusto e “resistente alle metastasi”.
Cosa significa per i pazienti e le terapie
Complessivamente, lo studio rivela che il muscolo scheletrico agisce come un habitat ostile che costringe le cellule tumorali in una modalità simile all’ipossia e a bassa proliferazione, anche quando l’ossigeno è abbondante. Questo aiuta a spiegare perché il muscolo è un sito così raro di metastasi. Offre anche un messaggio di cautela per lo sviluppo farmacologico: terapie progettate per bloccare la segnalazione dell’ipossia a livello sistemico potrebbero indebolire involontariamente questa difesa naturale basata sul muscolo, rendendo più facile per le cellule tumorali crescere dove normalmente non lo farebbero. Capire e preservare, o persino imitare, le caratteristiche protettive del tessuto muscolare potrebbe aprire nuove strade per prevenire o controllare la malattia metastatica.
Citazione: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Parole chiave: metastasi del cancro, muscolo scheletrico, ipossia, microambiente tumorale, dormienza tumorale