Clear Sky Science · it
L’assorbimento degli acidi grassi mediato da FABP4 favorisce la senescenza delle cellule T CD8+ tramite perossidazione lipidica nel microambiente ricco di adipociti del carcinoma ovarico
Perché il grasso e le cellule immunitarie contano nel carcinoma ovarico
Il carcinoma ovarico spesso si diffonde nella cavità addominale, dove incontra vaste riserve di tessuto adiposo. Questo ambiente grasso non è un semplice sfondo passivo: modella attivamente il comportamento delle cellule immunitarie. In particolare, può indebolire le cellule T CD8 “killer” che dovrebbero attaccare i tumori. Questo studio esplora come le sostanze derivate dal grasso spingano queste T cell in uno stato invecchiato e logoro, e come bloccare una proteina chiave del trasporto lipidico possa aiutare a ripristinare la loro capacità di combattere il cancro.
Ambienti ricchi di grasso che invecchiano i difensori immunitari
I medici da tempo osservano che molte donne con carcinoma ovarico avanzato accumulano liquido nell’addome e presentano tumori insediati in tessuti ricchi di grasso chiamati omento. Analizzando dati di RNA a singola cellula di pazienti e esaminando campioni tumorali al microscopio, i ricercatori hanno riscontrato che le cellule T CD8 vicine a questi depositi adiposi mostravano più frequentemente segni della senescenza cellulare. Queste T cell “invecchiate” accumulano pigmenti di scarto, smettono di dividersi e producono segnali infiammatori invece di uccidere le cellule tumorali. Sia nei campioni umani sia nei modelli murini, le CD8 T prelevate dalle aree tumorali ricche di grasso e liquido risultavano nettamente più senescenti rispetto a quelle provenienti da linfonodi o milza, collegando direttamente il microambiente tumorale ricco di adipociti all’invecchiamento delle T cell.
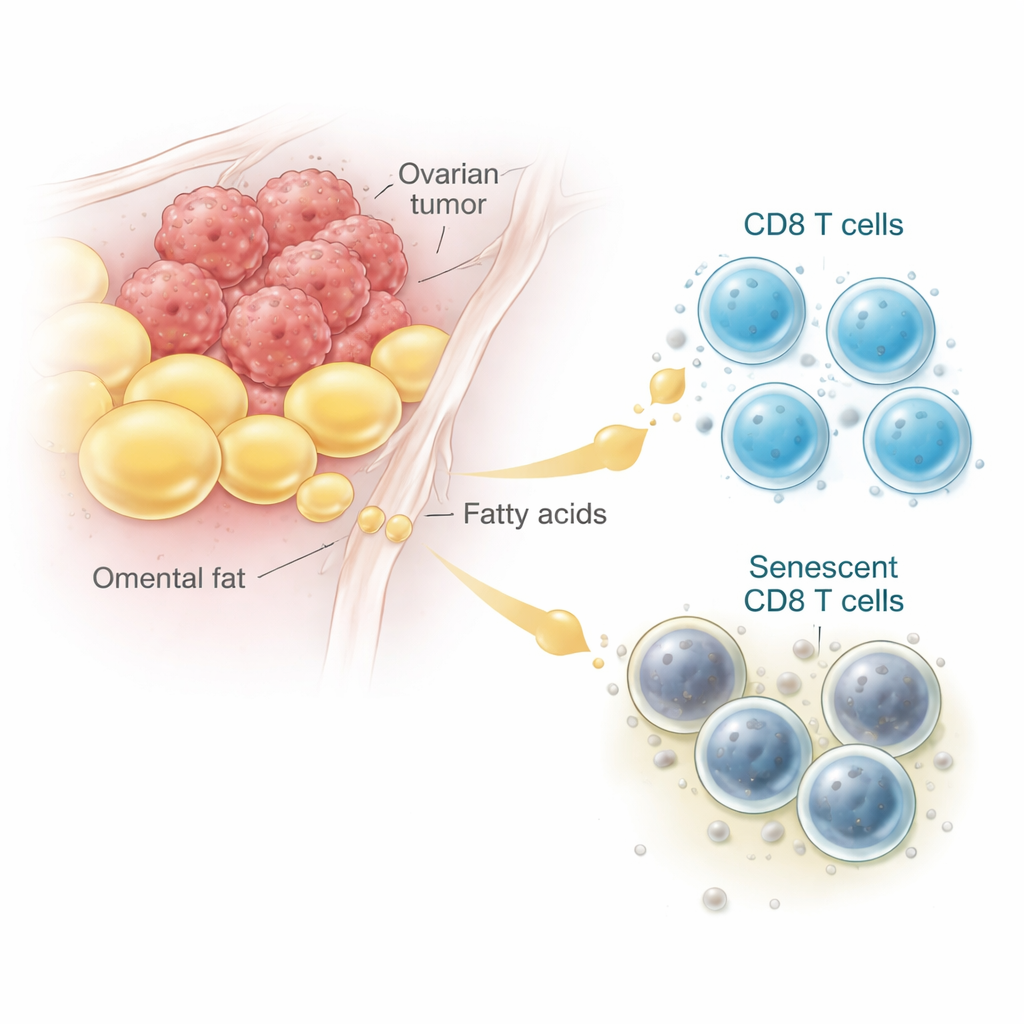
Come un comune acido grasso trasforma il carburante utile in danno
Per capire cosa il grasso stesse facendo alle T cell, il team ha ricreato in laboratorio il contesto tumorale. Hanno coltivato cellule di carcinoma ovarico insieme a T CD8 murine, quindi hanno aggiunto estratti di tessuto adiposo o un acido grasso specifico chiamato acido oleico, abbondante nel liquido associato al carcinoma ovarico. A dosi moderate-alte, l’acido oleico ha indotto un maggior numero di CD8 T a diventare senescenti—ma solo in presenza delle cellule tumorali. Invece di usare il grasso in ingresso come fonte energetica, le T cell accumulavano lipidi che venivano chimicamente danneggiati, in un processo noto come perossidazione lipidica. Analisi geniche e lipidiche hanno mostrato un aumento dei marcatori di grassi ossidati e dello stress, mentre la produzione energetica dal grasso rimaneva invariata. In breve, in presenza del tumore, il grasso che avrebbe dovuto essere carburante veniva deviato in reazioni dannose che invecchiano e disabilitano le T cell.
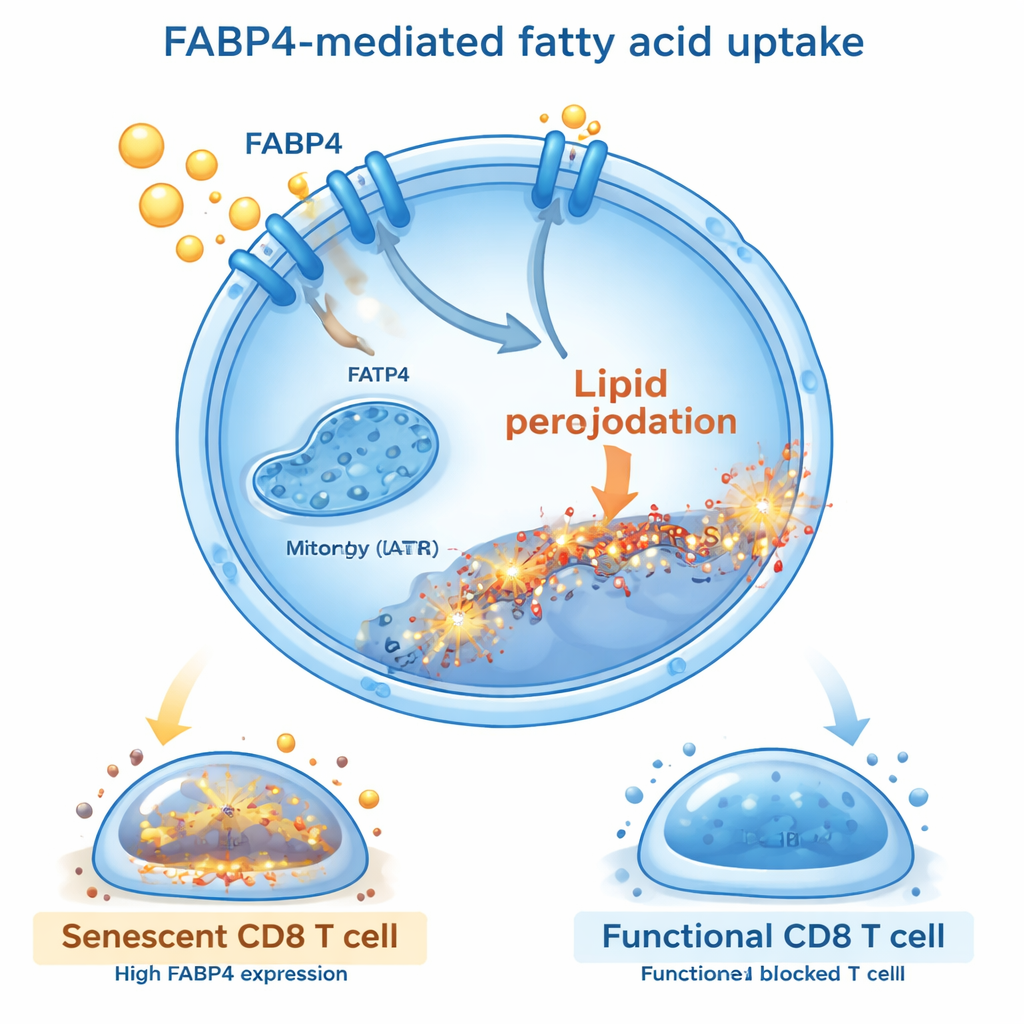
Il trasportatore di lipidi FABP4 come guardiano chiave
Approfondendo, i ricercatori hanno indagato quali molecole controllassero questo ingresso dannoso di lipidi. Hanno scoperto che una proteina trasportatrice chiamata FABP4 risultava fortemente attivata nelle CD8 T esposte agli estratti di grasso o all’acido oleico. FABP4 funge da navetta, trasportando acidi grassi a catena lunga nelle cellule. Quando hanno bloccato FABP4 usando sia un farmaco a piccola molecola (BMS309403) sia il silenziamento genetico, le T cell hanno assorbito meno grasso, mostrato minore perossidazione lipidica e sono risultate meno propense a diventare senescenti. Queste T protette si dividevano meglio, producevano più molecole anticancro come interferone-gamma e granzima B, e rilasciavano meno segnali soppressivi e infiammatori. Il ripristino dei livelli di FABP4 annullava questi benefici, confermando che questo trasportatore è un interruttore centrale che collega l’assorbimento lipidico all’invecchiamento delle T cell.
Dagli esperimenti murini a una strategia terapeutica potenziale
Il team ha poi testato il blocco di FABP4 in topi vivi con carcinoma ovarico diffuso nella cavità addominale. Il trattamento con l’inibitore di FABP4 ha ridotto l’assorbimento di grasso e i danni lipidici nelle CD8 T prelevate dal liquido addominale, ha abbassato la proporzione di T senescenti e ha aumentato i livelli delle principali molecole effettrici. Quando l’inibitore di FABP4 è stato combinato con la chemioterapia standard, i topi presentavano meno noduli tumorali visibili, risposte T più forti in milza, linfonodi e ascite, e sopravvivevano più a lungo rispetto a quelli trattati solo con chemioterapia. Questi risultati suggeriscono che mirare al metabolismo lipidico può rendere i trattamenti esistenti più efficaci risvegliando i soldati in prima linea del sistema immunitario.
Cosa significa questo per i pazienti
Per i lettori non specialisti, la conclusione è che nel carcinoma ovarico non conta solo il tumore, ma anche il quartiere grasso in cui vive. Le molecole derivate dal grasso, in particolare certi acidi grassi, possono invecchiare prematuramente le T killer, privandole della capacità di attaccare il cancro. Questo lavoro identifica il trasportatore lipidico FABP4 come un colpevole chiave di questo processo. Bloccando FABP4, almeno nei topi, i ricercatori sono riusciti a ridurre la senescenza T, a ripristinarne la funzione citotossica e a migliorare l’efficacia della chemioterapia. Sebbene siano necessarie ulteriori ricerche prima di trasformare questo approccio in una terapia clinica, lo studio apre una nuova strada: trattare non solo il cancro stesso, ma anche le trappole metaboliche del suo ambiente che disarmano il sistema immunitario.
Citazione: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Parole chiave: carcinoma ovarico, senescenza delle cellule T, metabolismo degli acidi grassi, microambiente tumorale, FABP4