Clear Sky Science · it
Il ruolo della demetilasi delle istoni PHF2 come soppressore tumorale nel carcinoma epatocellulare regolando SRXN1
Perché questo studio sul cancro al fegato è importante
Il cancro del fegato è uno dei tumori più letali a livello mondiale e i farmaci attuali estendono la sopravvivenza solo in misura modesta per molti pazienti. Questo studio pone una domanda diversa: invece di mirare ai soliti geni oncogeni, possiamo sfruttare il modo in cui il DNA è impacchettato e chimicamente marcato all’interno delle cellule epatiche per trovare opzioni di trattamento nuove e più precise? I ricercatori si concentrano su una proteina poco studiata chiamata PHF2 e rivelano come potrebbe contribuire a impedire che le cellule epatiche diventino cancerose.
Alla ricerca di punti deboli nel sistema di controllo del cancro
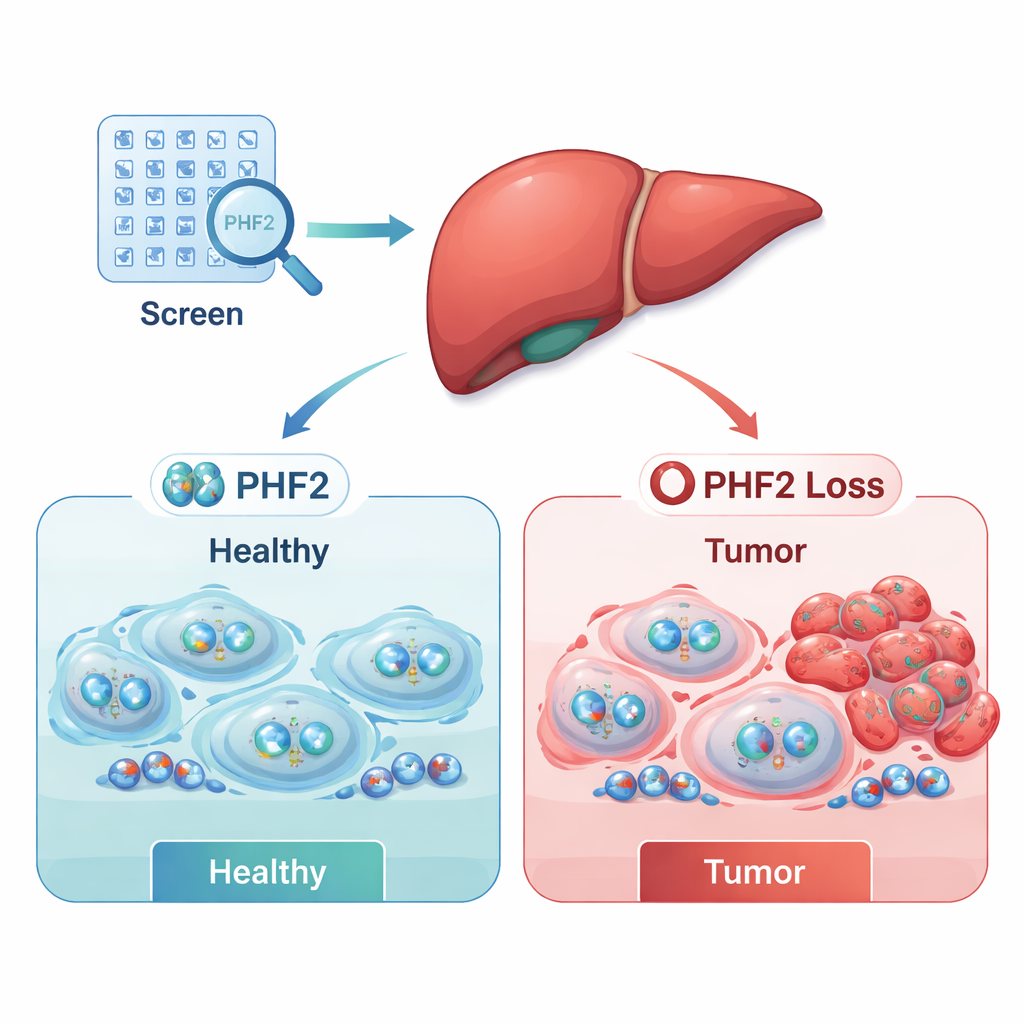
Il cancro non è alimentato solo da geni danneggiati; è anche sostenuto da controlli «epigenetici» difettosi — i marcatori chimici e i complessi proteici che decidono quali geni vengono accesi o spenti. Nel carcinoma epatocellulare, la forma più comune di cancro del fegato, molti di questi regolatori sono alterati. Il gruppo ha testato in modo sistematico 497 regolatori epigenetici in sei linee cellulari di cancro al fegato, usando strumenti di RNA per ridurre temporaneamente ognuno di essi uno per uno e poi misurando la sopravvivenza delle cellule tumorali. Questo ampio screening è stato progettato per rivelare quali regolatori le neoplasie dipendono per crescere e quali agiscono normalmente come freni alla formazione tumorale.
Trovare nuovi «acceleratori» e «protettori» del cancro
Lo screening ha portato alla luce due gruppi principali: potenziali «acceleratori» del cancro (oncogeni) la cui perdita danneggiava la sopravvivenza cellulare, e potenziali «freni» (soppressori tumorali) la cui perdita favoriva la crescita delle cellule tumorali. Integrando i dati di laboratorio con ampi dataset pubblici di pazienti, i ricercatori hanno ristretto la lista a pochi candidati con rilevanza clinica. Due regolatori, SUPT7L e SMARCC1, risultavano più attivi nei tumori e associati a una sopravvivenza peggiore. Al contrario, un regolatore — PHF2 — era spesso meno attivo nei tumori del fegato, e i pazienti i cui tumori mantenevano livelli più alti di PHF2 tendevano a vivere più a lungo. Questi schemi hanno suggerito che PHF2 potrebbe agire come soppressore tumorale nel cancro epatico umano.
Come la perdita di PHF2 cambia le cellule del carcinoma epatocellulare
Per approfondire il ruolo di PHF2, il team ha ingegnerizzato cellule di carcinoma epatocellulare per produrre in modo stabile meno di questa proteina e ha seguito il loro comportamento nel tempo. Le cellule con PHF2 ridotto crescevano più rapidamente e mostraveno livelli più elevati di Ki-67, un marcatore di proliferazione attiva, indicando che PHF2 normalmente contribuisce a limitare la proliferazione. Questi effetti erano più marcati nelle linee cellulari già aggressive, suggerendo che la sola perdita di PHF2 potrebbe non essere sufficiente ad avviare il cancro autonomamente, ma può accelerare la crescita delle cellule maligne una volta che i tumori si sono formati.
Un sorprendente collegamento con le difese dallo stress cellulare
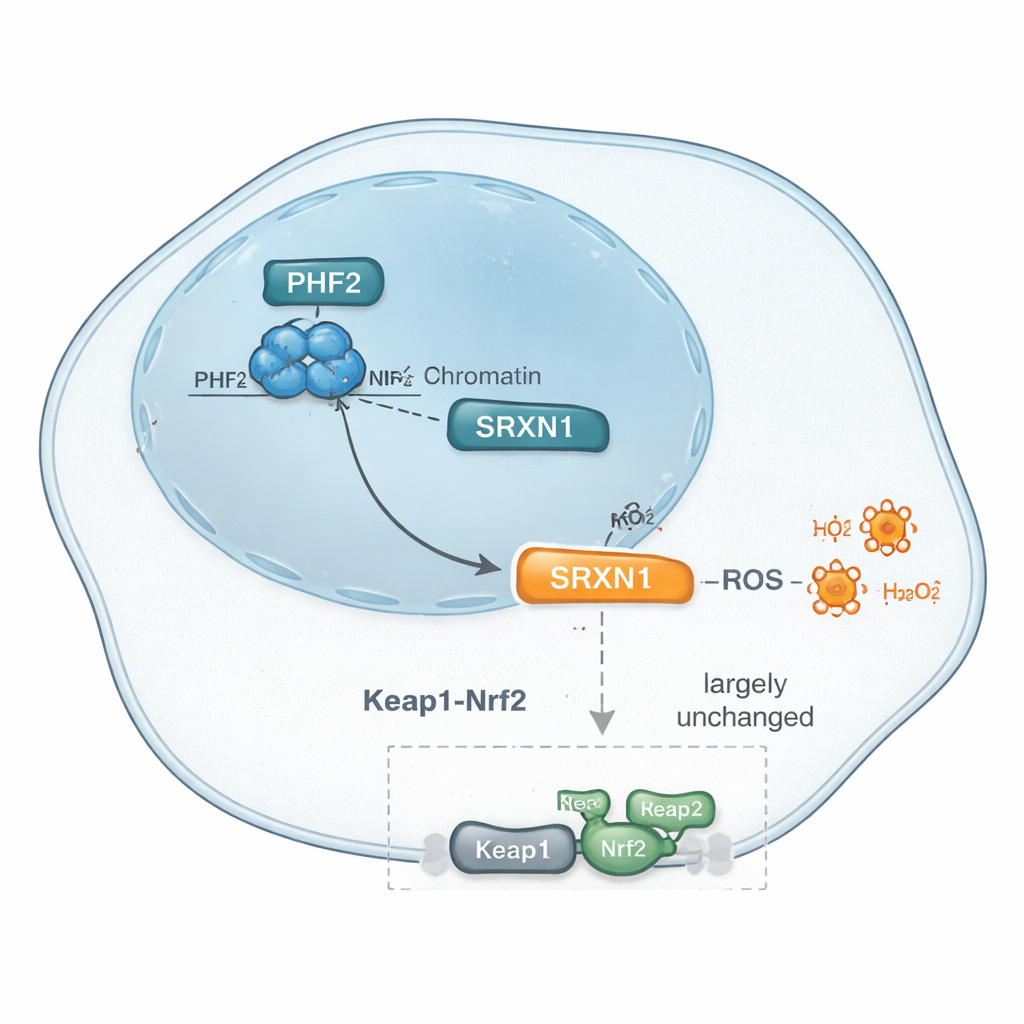
Successivamente, i ricercatori hanno utilizzato metodi moderni di proteomica per catalogare migliaia di proteine i cui livelli cambiavano quando PHF2 veniva ridotto. Tra molti spostamenti sottili, un modello è emerso con chiarezza: i livelli di una proteina protettiva dallo stress chiamata SRXN1 diminuivano costantemente con la perdita di PHF2. SRXN1 aiuta le cellule a gestire le specie reattive dell’ossigeno — sottoprodotti chimicamente reattivi che possono danneggiare DNA e proteine ma che possono anche spingere le cellule tumorali ad adattarsi. I dati suggeriscono che PHF2 contribuisce a mantenere i livelli di SRXN1 e che alterare questo equilibrio può influenzare come le cellule del carcinoma epatocellulare rispondono allo stress interno e, in definitiva, quanto rapidamente proliferano.
Agire al di fuori di una via di stress ben nota
SRXN1 è solitamente controllata da un interruttore maestro della risposta allo stress chiamato Nrf2, che attiva molti geni antiossidanti quando le cellule affrontano stress ossidativo. Poiché SRXN1 diminuiva quando PHF2 era soppresso, il team ha chiesto se PHF2 potesse semplicemente agire tramite questa nota via di Nrf2. Hanno esaminato geni e proteine chiave correlati a Nrf2, trattato le cellule con farmaci che attivano Nrf2 bloccando il suo inibitore Keap1, e utilizzato strumenti genetici per ridurre direttamente Keap1. In questi test, la risposta delle cellule carenti di PHF2 somigliava in gran parte a quella delle cellule normali, e analisi più ampie di vie e fattori di trascrizione non hanno indicato Nrf2 come protagonista principale. Invece, altri fattori, tra cui ZNF384 e Nrf1 — entrambi precedentemente collegati al cancro al fegato — sono emersi come candidati. Nel complesso, le evidenze suggeriscono che il controllo di PHF2 su SRXN1 e sulle risposte antiossidanti potrebbe bypassare la classica segnalazione Nrf2, suggerendo una via distinta di regolazione dello stress in questi tumori.
Cosa potrebbe significare per trattamenti futuri
Per un pubblico non specialista, il messaggio chiave è che questo studio identifica PHF2 come un promettente fattore protettivo nel cancro al fegato: quando PHF2 è presente e attivo, le cellule tumorali crescono più lentamente; quando è ridotto, acquisiscono un vantaggio di crescita e modificano il modo in cui gestiscono lo stress cellulare. Poiché PHF2 stessa potrebbe essere difficile da bloccare o potenziare con i tradizionali farmaci a piccola molecola, gli autori indicano strategie emergenti come terapie basate su RNA o farmaci che ne potenziano l’attività attraverso partner di segnalazione a monte. Sottolineano inoltre che gli effetti di PHF2 dipendono dal contesto — il suo impatto può variare in presenza di altre mutazioni come lo stato di p53 — quindi qualsiasi terapia futura richiederà probabilmente una selezione accurata dei pazienti. Nel complesso, il lavoro affina la nostra comprensione di come i regolatori epigenetici modellino il comportamento del cancro al fegato e apre nuove strade per progettare trattamenti che ripristinino o imitino l’influenza soppressiva tumorale di PHF2.
Citazione: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Parole chiave: carcinoma epatocellulare, regolazione epigenetica, PHF2, SRXN1, terapia del cancro al fegato