Clear Sky Science · it
La degradazione mediata da TRIM21 di HILPDA supera la resistenza all’immunoterapia anti‑PD‑1 nel cancro al seno limitando la palmitoilazione di PD‑L1
Perché alcune immunoterapie contro il cancro smettono di funzionare
I farmaci che liberano la risposta immunitaria, come le terapie anti–PD‑1, hanno trasformato il trattamento di diversi tumori, comprese forme aggressive di cancro al seno. Tuttavia molti tumori o non rispondono mai o trovano col tempo modi per eludere la risposta. Questo studio indaga una di queste vie di fuga nel carcinoma mammario triplo‑negativo e mostra come rimodellare il metabolismo lipidico tumorale — e un farmaco riproposto chiamato fenretinide — potrebbe riaprire la porta al sistema immunitario quando l’immunoterapia standard fallisce. 
Un aiutante nascosto che protegge i tumori
I ricercatori si sono concentrati su una proteina poco conosciuta chiamata HILPDA, precedentemente collegata al modo in cui le cellule gestiscono i grassi sotto stress. Confrontando tumori mammari di topo che restavano sensibili alla terapia anti‑PD‑1 con tumori che erano diventati resistenti, hanno rilevato che i livelli di HILPDA erano molto più alti nei tumori resistenti. Analisi su ampi database di pazienti e campioni tumorali di donne con carcinoma mammario hanno confermato che HILPDA è più abbondante nei tumori rispetto al tessuto mammario normale, specialmente nella malattia triplo‑negativa, e che le pazienti i cui tumori esprimono più HILPDA tendono ad avere esiti peggiori. I tumori di persone che non hanno beneficiato dei farmaci che bloccano PD‑1 presentavano anch’essi più HILPDA, collegando direttamente questa proteina al fallimento del trattamento.
Come i tumori trasformano il paesaggio immunitario contro di noi
Per capire cosa fa realmente HILPDA all’interno dei tumori, il team ha ingegnerizzato cellule di cancro al seno per sovraesprimere o per essere prive della proteina e poi le ha coltivate con cellule immunitarie umane o in topi. Quando HILPDA era elevata, i tumori attiravano più cellule T regolatorie, cellule soppressive di derivazione mieloide e macrofagi di tipo M2 — tipi di cellule immunitarie che attenuano l’attacco e aiutano i tumori a nascondersi. Allo stesso tempo, il numero e la vitalità delle cellule killer CD8 e delle cellule natural killer diminuivano, così come la loro capacità di rilasciare molecole tossiche e segnali infiammatori. Silenziare HILPDA invertiva questo quadro: i tumori ospitavano meno cellule soppressive, più cellule killer attive, cresceva più lentamente e davano meno metastasi. In modo cruciale, quando animali con tumori a bassa espressione di HILPDA ricevevano terapia anti‑PD‑1, i loro tumori si riducevano di più e i topi vivevano più a lungo, dimostrando che HILPDA controlla l’efficacia dell’immunoterapia.
Produzione di lipidi, corazza molecolare ed evasione immunitaria
Approfondendo, gli scienziati hanno scoperto come HILPDA rimodella il metabolismo tumorale per irrobustire le difese immunitarie. All’interno delle cellule cancerose, HILPDA si lega a una proteina chaperone chiamata HSP90 per stabilizzare un fattore di trascrizione, KLF5, che guida la produzione di lipidi. Questo trio potenzia la sintesi di acidi grassi, in particolare del palmitato, e riempie le cellule tumorali di goccioline lipidiche. Uno di questi grassi viene poi attaccato a PD‑L1, la proteina checkpoint che si trova sulla superficie tumorale e invia un segnale di “non attaccare” alle cellule immunitarie. Il team ha dimostrato che l’aggiunta di palmitato in un punto specifico di PD‑L1 funziona come una colla molecolare: aiuta PD‑L1 a stabilizzarsi nella membrana cellulare e ne impedisce la degradazione. La mutazione di questo singolo sito di attacco privava PD‑L1 della sua stabilità e indeboliva la sua capacità di proteggere le cellule tumorali, anche quando HILPDA era abbondante. In altre parole, la produzione di lipidi guidata da HILPDA alimenta una modifica chimica su PD‑L1 che trasforma lo scudo immunitario del tumore da fragile a rinforzato come l’acciaio.
Il freno incorporato che può essere premuto
Ogni acceleratore ha bisogno di un freno, e qui il freno è un’altra proteina chiamata TRIM21. Gli autori hanno scoperto che TRIM21 riconosce HILPDA e la marca con “flag” molecolari che la indirizzano alla macchina di smaltimento della cellula. Nei tumori mammari dei pazienti, i livelli di TRIM21 tendevano a essere bassi quando HILPDA era elevata, e un basso TRIM21 era associato a esiti sfavorevoli, suggerendo che questo sistema di frenata naturale è spesso indebolito nel cancro. Il team ha quindi cercato farmaci in grado di rafforzare TRIM21 e ha identificato il fenretinide, un retinoide già testato nell’uomo. In modelli cellulari e animali di carcinoma mammario triplo‑negativo, il fenretinide ha aumentato l’attività di TRIM21, accelerato la degradazione di HILPDA, ridotto la sintesi di lipidi e la modificazione protettiva di PD‑L1 e rallentato la crescita e la diffusione tumorale. Più sorprendente, la combinazione di fenretinide con terapia anti‑PD‑1 ha reso i tumori più vulnerabili all’attacco immunitario, aumentando le cellule T killer e le natural killer e riducendo le cellule soppressive nel microambiente tumorale. 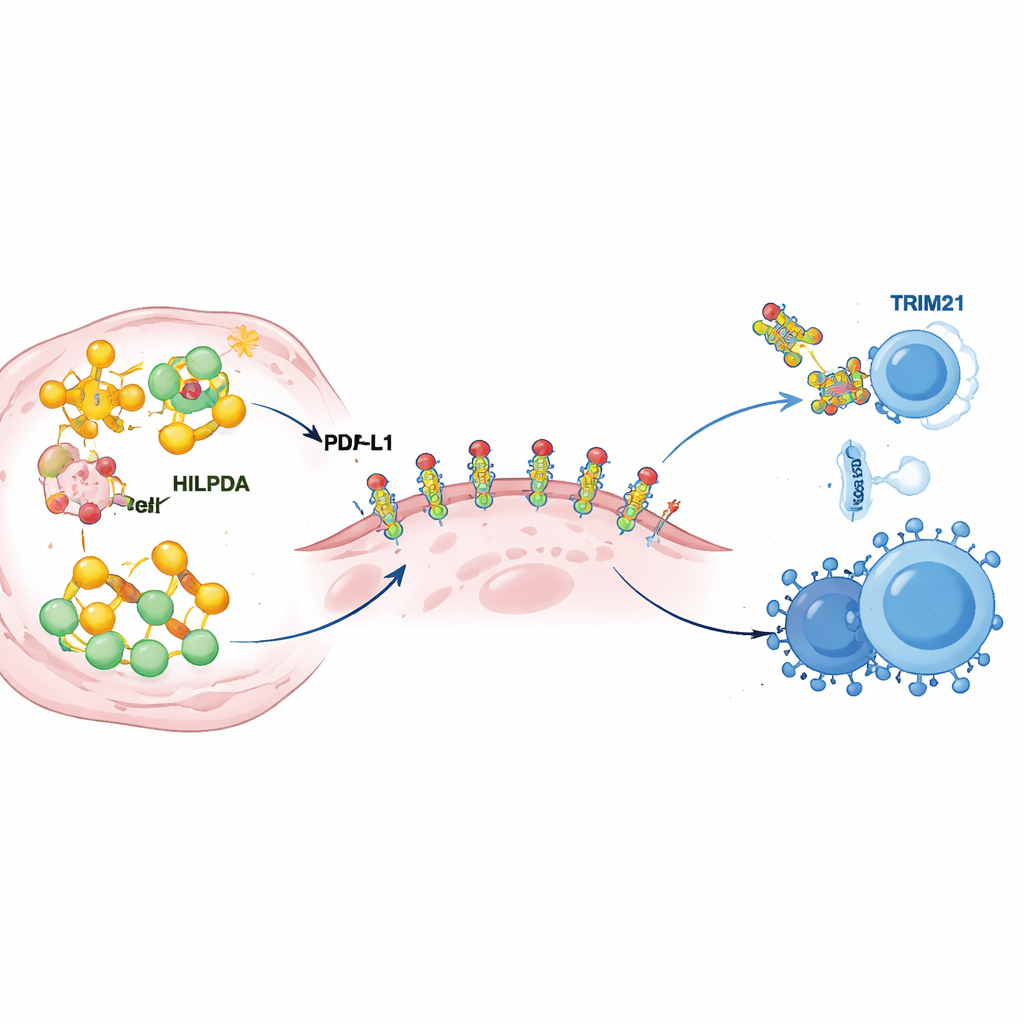
Cosa significa per la cura del cancro in futuro
Questo lavoro rivela una catena di eventi in cui le cellule di carcinoma mammario sotto stress aumentano HILPDA, intensificano la produzione di lipidi e rinforzano chimicamente PD‑L1 sulla loro superficie, permettendo loro di continuare a reprimere le cellule immunitarie anche di fronte ai farmaci che bloccano PD‑1. TRIM21 funge da salvaguardia interna in grado di smantellare HILPDA, ma spesso è troppo debole nei tumori. Trovando che il fenretinide può riattivare questa salvaguardia, lo studio indica una via pratica per combinare un farmaco metabolico con l’immunoterapia esistente per superare la resistenza. Se confermato in studi clinici, il targeting dell’asse TRIM21–HILPDA–PD‑L1 potrebbe offrire alle pazienti con carcinoma mammario triplo‑negativo difficile da trattare una seconda opportunità di beneficiare di terapie basate sul sistema immunitario.
Citazione: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Parole chiave: cancro al seno triplo negativo, resistenza all’immunoterapia, palmitoilazione di PD‑L1, metabolismo lipidico tumorale, fenretinide