Clear Sky Science · it
Cereblon (CRBN) inibisce la metastasi del cancro alla prostata regolando negativamente la 6‑fosfogluconato deidrogenasi (6PGD)
Perché questa ricerca è importante
Quando il cancro alla prostata si diffonde dalla ghiandola prostatica ad altri organi diventa molto più difficile da trattare e spesso letale. Questo studio rivela come una proteina di “controllo qualità” cellulare poco conosciuta, cereblon (CRBN), contribuisca a impedire la diffusione del cancro alla prostata smantellando un enzima metabolico che alimenta il comportamento aggressivo. Capire questo sistema di freno intrinseco suggerisce nuovi modi per rallentare o fermare le metastasi, soprattutto nelle forme difficili da trattare della malattia.
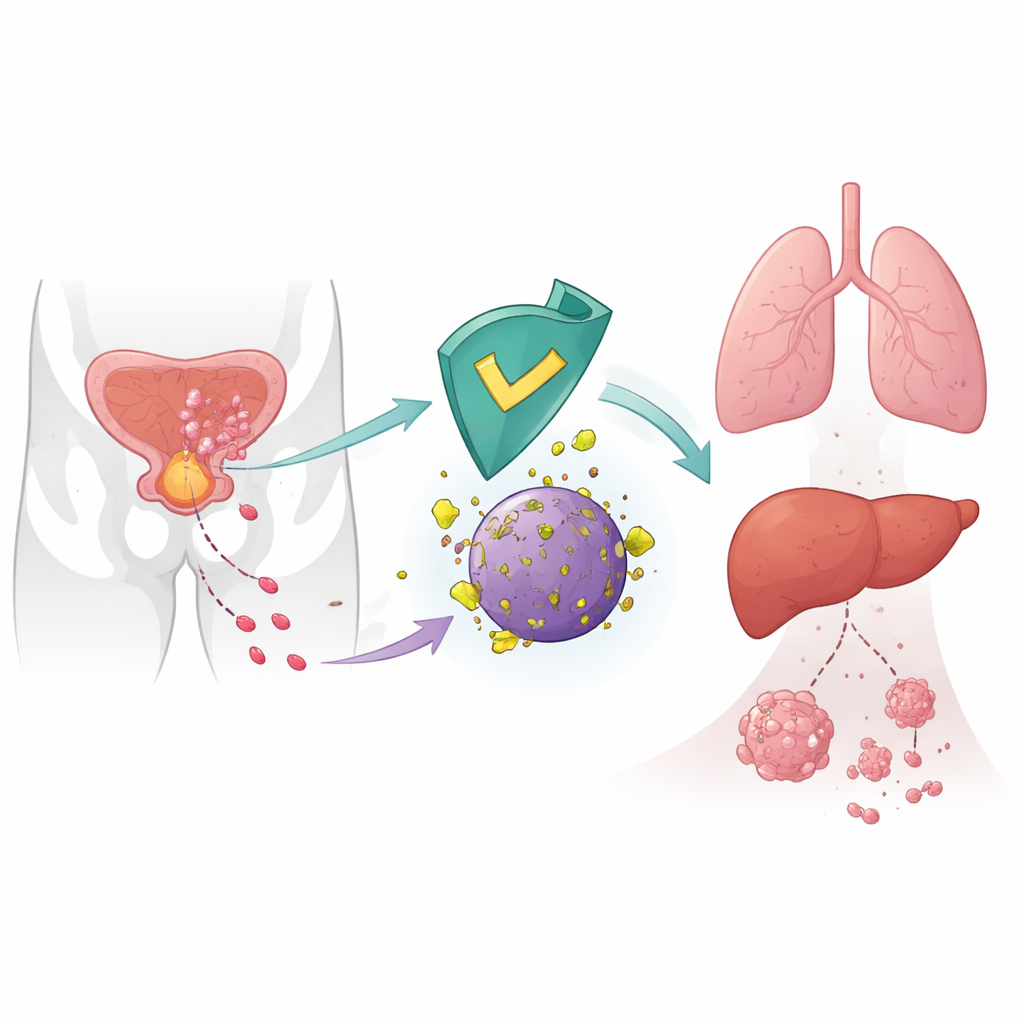
Un freno interno alla diffusione del cancro
Le cellule tumorali non si diffondono a caso; riorganizzano la loro macchina interna per muoversi, invadere e colonizzare organi lontani. Gli autori si sono concentrati su CRBN, una proteina nota soprattutto come bersaglio di farmaci come la talidomide impiegati nei tumori del sangue. Nelle cellule sane CRBN fa parte di un’unità molecolare di smaltimento che marca certe proteine per la distruzione. Lavori precedenti avevano suggerito che bassi livelli di CRBN nei tumori erano associati a esiti peggiori, ma il suo ruolo diretto nelle metastasi non era chiaro. Qui i ricercatori dimostrano che CRBN agisce come soppressore naturale della diffusione del cancro alla prostata prendendo di mira per la degradazione un enzima metabolico chiamato 6‑fosfogluconato deidrogenasi (6PGD).
Un motore metabolico che il cancro sfrutta
La 6PGD opera in una via metabolica nota come via ossidativa delle pentoso‑fosfati, che aiuta le cellule a generare NADPH, una molecola che fornisce sia i mattoni per la sintesi che capacità antiossidante. Molti tumori potenziano questa via per crescere più rapidamente e tollerare lo stress. Il gruppo ha scoperto che campioni di tumore prostatico dei pazienti tendono ad avere meno CRBN e più 6PGD rispetto al tessuto prostatico normale, e che questo squilibrio è particolarmente marcato nelle forme aggressive. Nelle linee cellulari di cancro alla prostata, l’abbattimento di CRBN o la sua degradazione mediante un composto progettato ha aumentato i livelli proteici e l’attività enzimatica della 6PGD, incrementando il NADPH. Ripristinare CRBN ha avuto l’effetto opposto, abbassando 6PGD e NADPH senza modificare il messaggio genico della 6PGD, indicando un controllo a livello proteico.
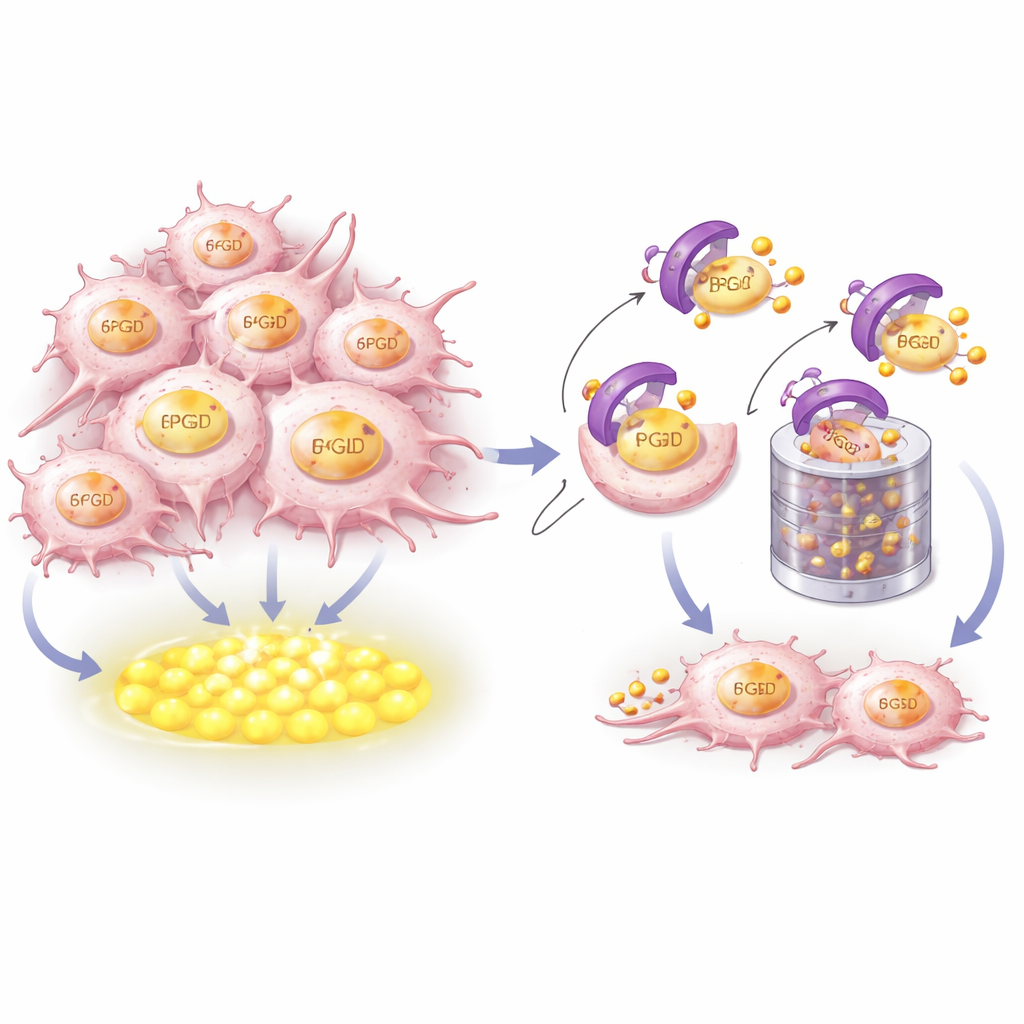
Come CRBN riconosce e distrugge la fonte di carburante
Per capire come CRBN controlli la 6PGD, i ricercatori hanno combinato modellizzazione strutturale ed esperimenti biochimici. Hanno mostrato che CRBN afferra fisicamente un breve segmento elicoidale altamente conservato vicino all’estremità C‑terminal della 6PGD. Aminoacidi chiave di entrambe le proteine formano un’interfaccia di accoppiamento compatta. Quando questi punti di contatto sono stati alterati, CRBN non poteva più legarsi alla 6PGD, attaccare i piccoli tag ubiquitina che la segnalano per la degradazione, né inviarla allo sminuzzatore cellulare noto come proteasoma. È importante notare che questa superficie di riconoscimento è separata dalla tasca dove si legano farmaci che modulano il sistema immunitario, il che significa che il controllo di CRBN sulla 6PGD fa parte del suo ruolo di manutenzione naturale e non è un effetto indotto dai farmaci.
Dal metabolismo alterato alle cellule erranti
Le conseguenze di questa stretta molecolare si osservano a livello del comportamento cellulare. Nelle cellule di cancro alla prostata prive di CRBN, l’aumento di 6PGD e NADPH si è accompagnato a una maggiore mobilità e capacità di invasione attraverso barriere artificiali, caratteristiche della potenzialità metastatica. Quando CRBN veniva sovraespresso, le cellule diventavano meno mobili e invasive, sebbene il loro tasso di crescita non cambiasse. Il profiling dell’attività genica ha mostrato che CRBN aumentava i livelli di CDH1, associato a cellule epiteliali compatte, e diminuiva i livelli di MMP1, legato alla degradazione tissutale e alla migrazione. Importante, questi cambiamenti richiedevano il legame diretto CRBN–6PGD e potevano essere invertiti bloccando l’attività enzimatica della 6PGD, collegando le modifiche metaboliche ai cambiamenti nel comportamento metastatico.
Evidenze da modelli animali e altri tumori
Il gruppo ha testato queste idee nei topi iniettando cellule di cancro alla prostata nel flusso sanguigno o nella milza. Le cellule ingegnerizzate per produrre CRBN in eccesso hanno formato molti meno noduli metastatici nel fegato e nei polmoni rispetto alle cellule di controllo, confermando un ruolo anti‑metastatico negli animali vivi. Topi privi di CRBN mostravano livelli più alti di proteina 6PGD in diversi organi. Schemi simili sono emersi in linee cellulari di glioblastoma, polmone e rene: la rimozione di CRBN aumentava 6PGD e potenziava movimento e invasione cellulare, mentre l’inibizione genetica o farmacologica della 6PGD attenuava questo comportamento aggressivo. Queste osservazioni suggeriscono che il freno CRBN–6PGD sulle metastasi non è esclusivo del cancro alla prostata.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, lo studio propone che CRBN funzioni da guardiano metabolico che limita la fornitura energetica necessaria alle cellule tumorali per distaccarsi, migrare e impiantarsi in nuove sedi tumorali. Quando CRBN viene perso o è presente in basse quantità, la 6PGD si accumula, la produzione di NADPH sale e le cellule sono più propense a subire cambiamenti che favoriscono le metastasi. Per i pazienti, questo indica due possibili applicazioni: misurare i livelli di CRBN e 6PGD potrebbe aiutare a identificare i tumori ad alto rischio metastatico, e terapie che aumentino la funzione di CRBN — o che sopprimano selettivamente la 6PGD nei tumori poveri di CRBN — potrebbero offrire nuovi modi per rallentare o prevenire la diffusione del cancro alla prostata e di altri tumori.
Citazione: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Parole chiave: metastasi del cancro alla prostata, metabolismo tumorale, cereblon, enzima 6PGD, via NADPH