Clear Sky Science · it
L1TD1 favorisce la progressione dell’adenocarcinoma mucinoso colorettale incrementando la stabilità dell’mRNA di ABCC3
Perché questo cancro ricco di muco è importante
Il cancro colorettale è una delle principali cause di morte per cancro nel mondo. Al suo interno, un sottotipo particolare chiamato adenocarcinoma mucinoso si distingue perché i tumori sono pieni di muco denso che costituisce più della metà della massa tumorale. Questa barriera viscida può aiutare le cellule tumorali a nascondersi dalla chemioterapia e dalle difese dell’organismo. Lo studio pone una domanda semplice ma cruciale: cosa controlla tutta questa produzione di muco e possiamo bloccarla per rallentare il tumore e rendere i trattamenti più efficaci?
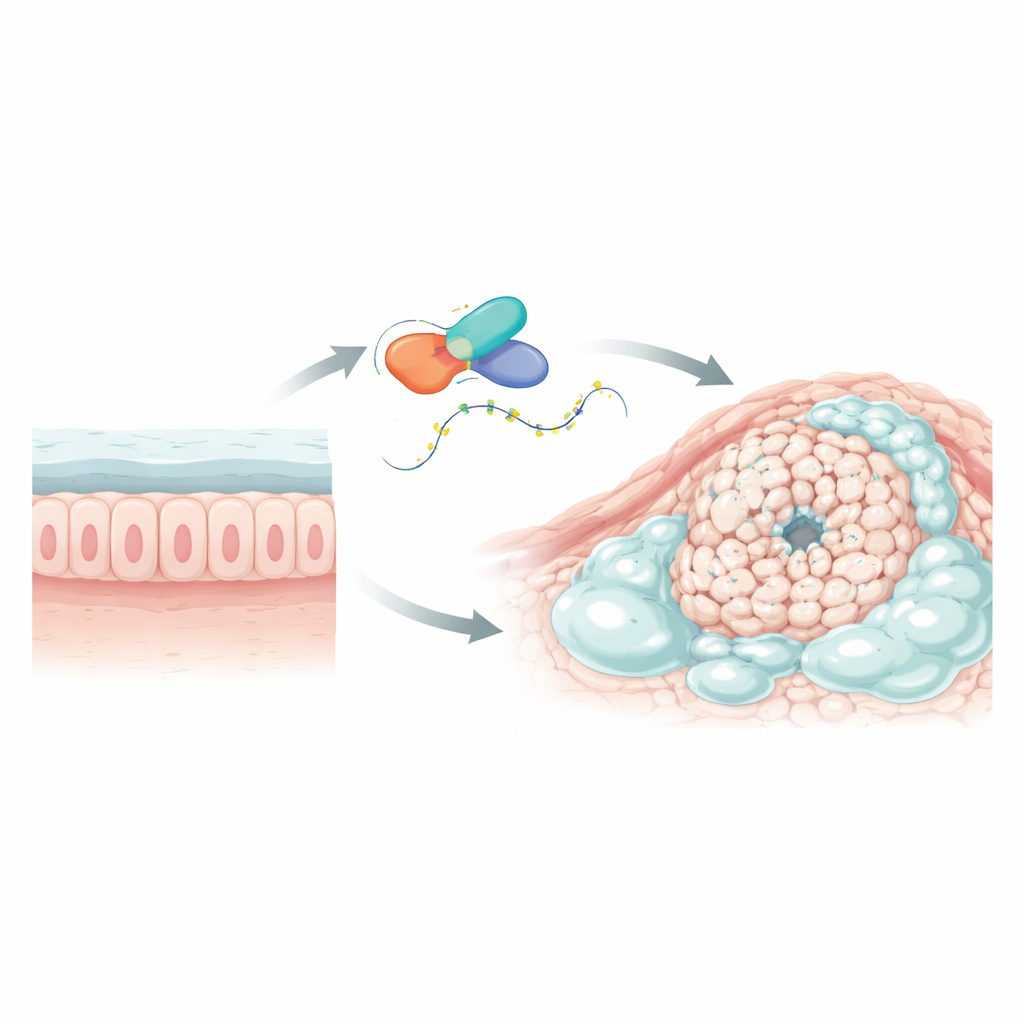
Individuare un gene chiave responsabile
I ricercatori hanno innanzitutto esplorato grandi database sul cancro e dati di sequenziamento a singola cellula per identificare geni che si comportano in modo diverso nei tumori colorettali ricchi di muco rispetto ai tumori colorettali ordinari e al tessuto sano circostante. Un gene, chiamato L1TD1, è emerso con forza. Risultava fortemente aumentato nei tumori mucinosi ma non nei tumori non mucinosi ed era maggiormente espresso nel tessuto tumorale rispetto al colon normale circostante. L1TD1 codifica per una proteina legante l’RNA, la molecola che trasporta i messaggi genetici dal DNA alla machineria cellulare di sintesi proteica. Poiché le proteine leganti l’RNA possono modulare quanto a lungo i messaggi persistono e quanto vengono tradotti, L1TD1 è apparso un candidato plausibile come regolatore principale in questi tumori carichi di muco.
Come L1TD1 favorisce crescita e diffusione del tumore
Per verificare la funzione di L1TD1, il gruppo ha usato linee cellulari di carcinoma colon-rettale e modelli murini. Quando hanno aumentato i livelli di L1TD1 nelle cellule tumorali, queste proliferavano più rapidamente, migravano con maggiore facilità e invadevano barriere tissutali simulate in modo più aggressivo. Ridurre L1TD1 ha avuto l’effetto opposto, rallentando la crescita e riducendo l’invasione. Nei topi iniettati con cellule ad alta espressione di L1TD1, i tumori erano più grandi e si diffondevano più spesso al fegato e alla cavità addominale. Nei pazienti, tumori con più L1TD1 tendevano inoltre a essere più grandi, meno differenziati e in stadi più avanzati, collegando questo gene a un comportamento clinico peggiore della malattia.
Attivazione del muco e della resistenza ai farmaci
Il muco si è rivelato centrale per l’impatto di L1TD1. Le cellule con più L1TD1 producevano quantità maggiori di proteine chiave che formano il muco, in particolare MUC2 e MUC5AC, e mostravano caratteristiche delle cellule caliciformi, le normali cellule secernenti muco dell’intestino. Colture tridimensionali e colorazioni tissutali da pazienti e topi hanno confermato che l’aumentata espressione di L1TD1 andava di pari passo con muco più spesso e abbondante. Importante, questo muco non era solo un osservatore passivo: quando i ricercatori riducevano selettivamente MUC2, la crescita aggiuntiva, l’invasione e la resistenza alla chemioterapia indotte da L1TD1 scomparivano in gran parte. Le cellule ricche di L1TD1 erano più difficili da eliminare con l’ossaliplatino, farmaco comunemente usato, e i tumori contenenti tali cellule si riducevano meno nei topi trattati, sottolineando il ruolo protettivo del muco che L1TD1 contribuisce a costruire.
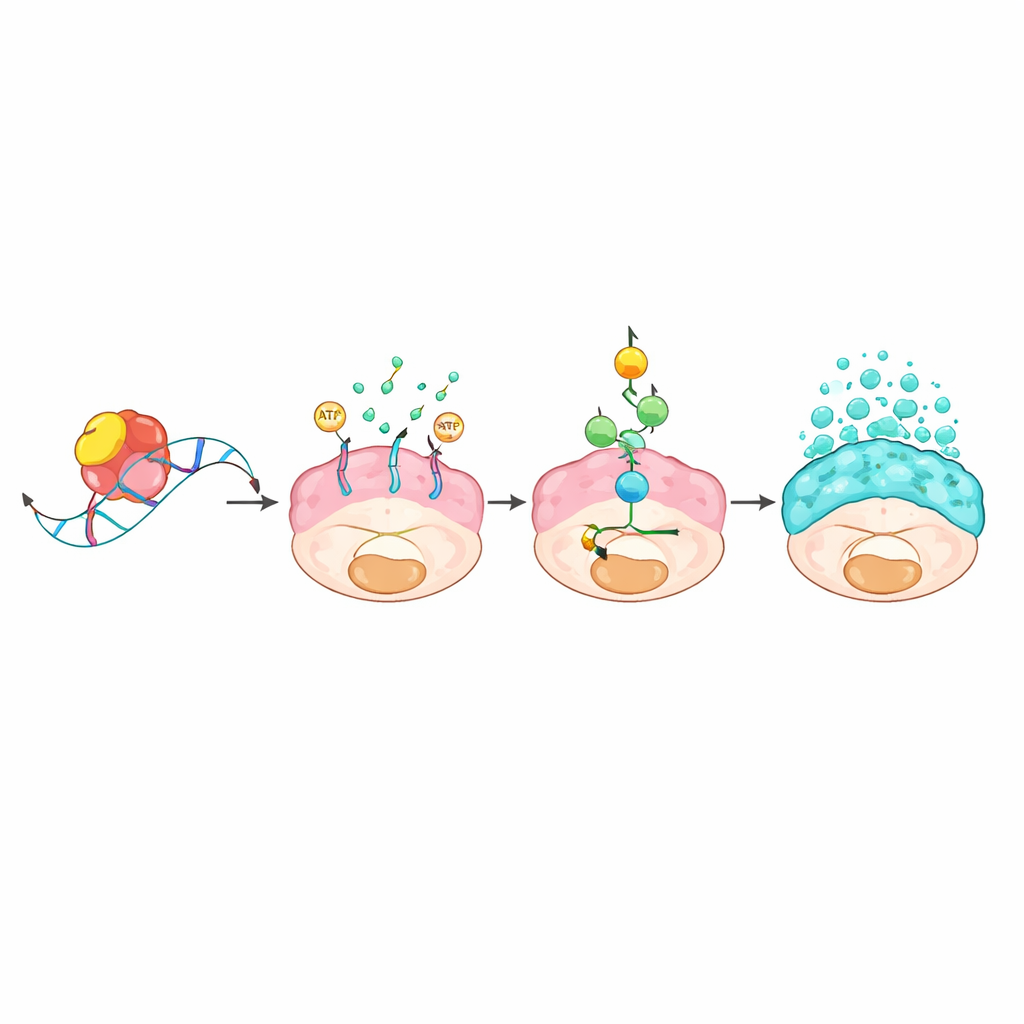
Una catena molecolare che collega il controllo dell’RNA alle inondazioni di muco
Il gruppo ha poi indagato come una proteina legante l’RNA potesse causare cambiamenti così marcati. Mediante l’isolamento delle molecole di RNA fisicamente legate a L1TD1 e il confronto dell’attività genica con e senza L1TD1, hanno identificato un gene trasportatore chiamato ABCC3 come bersaglio principale. L1TD1 si legava a un breve motivo “GUGU” nella regione terminale dell’RNA di ABCC3, stabilizzandolo in modo che la cellula producesse più proteina ABCC3, nota come MRP3. Questo trasportatore si trova nella membrana cellulare e usa energia per pompare sostanze fuori dalla cellula. Il conseguente dispendio energetico ha attivato un sistema di allarme metabolico centrato sul sensore AMPK, che a sua volta ha acceso una classica via di crescita e risposta allo stress nota come MAPK. Una volta attivata, questa cascata ha aumentato la produzione e il rilascio delle proteine del muco e ha rinforzato la capacità delle cellule tumorali di crescere, migrare e resistere ai farmaci. Bloccare ABCC3 geneticamente o con un composto sperimentale, oppure inibire la via MAPK, ha attenuato la produzione di muco e indebolito i tumori.
Cosa significa per i pazienti
Nel complesso, il lavoro rivela un sistema di controllo passo dopo passo per il cancro colorettale ricco di muco: L1TD1 stabilizza l’RNA di ABCC3, ABCC3 prosciuga l’energia cellulare, la via AMPK–MAPK si attiva e il tumore risponde sovraproducendo muco e diventando più aggressivo e resistente ai farmaci. Per i pazienti, questo indica diverse strade promettenti. I livelli di L1TD1 e ABCC3 potrebbero aiutare a identificare i tumori destinati a comportarsi in modo più aggressivo o a resistere alla chemioterapia standard. Ancora più importante, farmaci che interrompono l’interazione L1TD1–ABCC3, bloccano l’attività di pompaggio di MRP3 o bersagliano la via di segnalazione a valle potrebbero assottigliare la barriera mucosa, rallentare la crescita tumorale e rendere i trattamenti esistenti più efficaci per questa forma difficile di cancro colorettale.
Citazione: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Parole chiave: cancro colorettale mucinoso, L1TD1, ABCC3 MRP3, produzione di muco, resistenza chemioterapica