Clear Sky Science · it
L’elica polifunzionale dell’RNA DDX39A guida la progressione del glioblastoma modulando lo splicing alternativo di WISP1 che induce una polarizzazione immunosoppressiva dei macrofagi
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma è uno dei tumori cerebrali più letali, noto per recidivare dopo il trattamento e resistere alle terapie farmacologiche. Questo studio rivela come un singolo “interruttore” molecolare nelle cellule tumorali non solo favorisca la crescita del cancro, ma convinca anche le cellule immunitarie vicine a smettere di combattere e a proteggere invece il tumore. Tracciando questa catena di eventi, i ricercatori individuano anche un farmaco antipsicotico già esistente che potrebbe essere riproposto per interrompere questa rete dannosa.
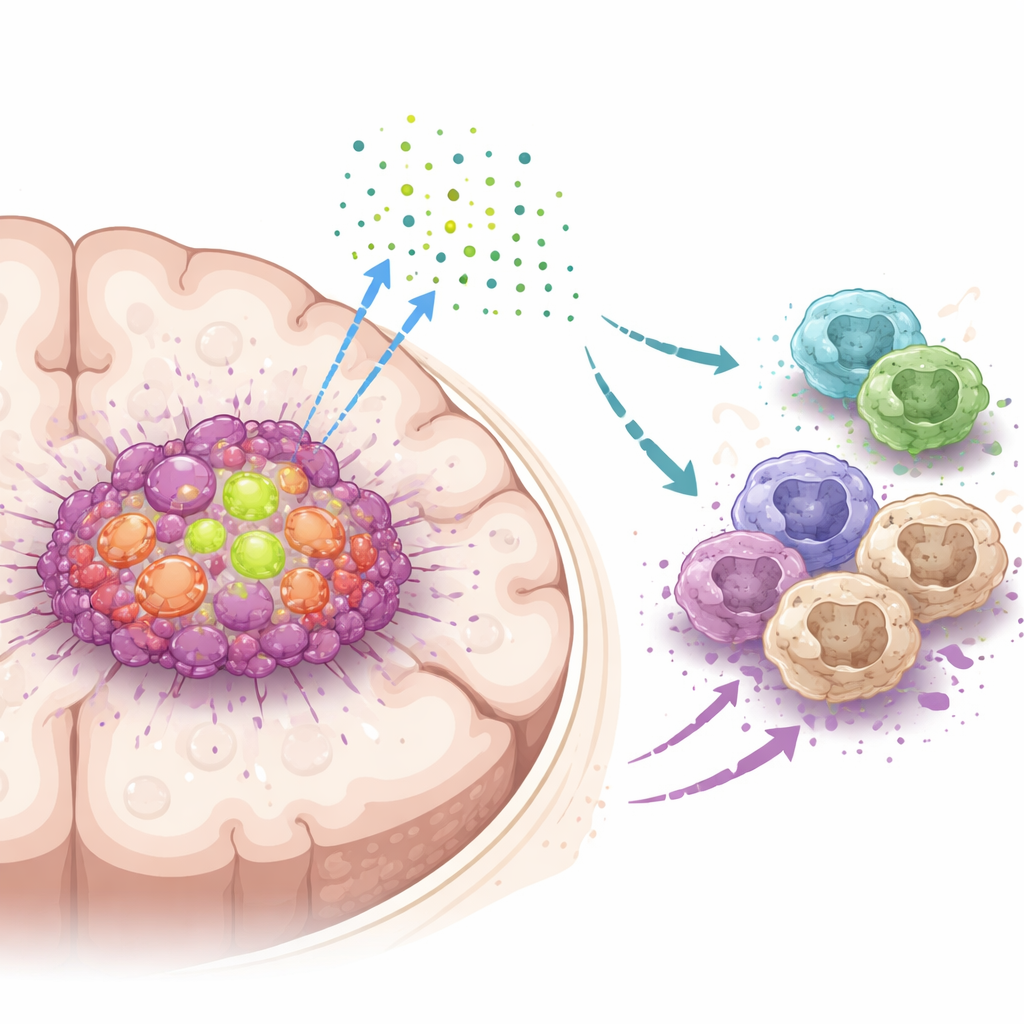
Un aiuto chiave all’interno delle cellule tumorali cerebrali
Il gruppo si è concentrato su una proteina chiamata DDX39A, una macchina molecolare che aiuta le cellule a processare l’RNA, la copia operativa dell’informazione genetica. Analizzando grandi database di pazienti e campioni tumorali, hanno scoperto che DDX39A è molto più attiva nel glioblastoma rispetto al tessuto cerebrale normale e che i suoi livelli aumentano con il grado tumorale. Analisi a singola cellula hanno mostrato che DDX39A è particolarmente abbondante nelle cellule tumorali che si dividono rapidamente e in alcuni macrofagi presenti nella massa tumorale. I pazienti i cui tumori mostravano livelli più alti di DDX39A tendevano ad avere esiti peggiori, suggerendo che questa proteina sia strettamente legata a una malattia più aggressiva.
Come questo fattore alimenta crescita e diffusione
Per verificare cosa faccia effettivamente DDX39A, i ricercatori hanno usato strumenti genetici per ridurne l’espressione in cellule staminali tumorali di glioblastoma coltivate in laboratorio e in modelli murini di tumore cerebrale. Quando DDX39A veniva ridotta, le cellule tumorali crescevano più lentamente, invadevano meno i tessuti circostanti e erano più propense a entrare in apoptosi. Le cellule staminali tumorali perdevano molto della loro capacità di formare nuove sfere tumorali, segno che l’autorinnovamento era compromesso. Nei topi, i tumori con DDX39A ridotta erano più piccoli e gli animali sopravvivevano più a lungo, confermando che questa proteina guida attivamente la progressione tumorale e non la marca solo passivamente.
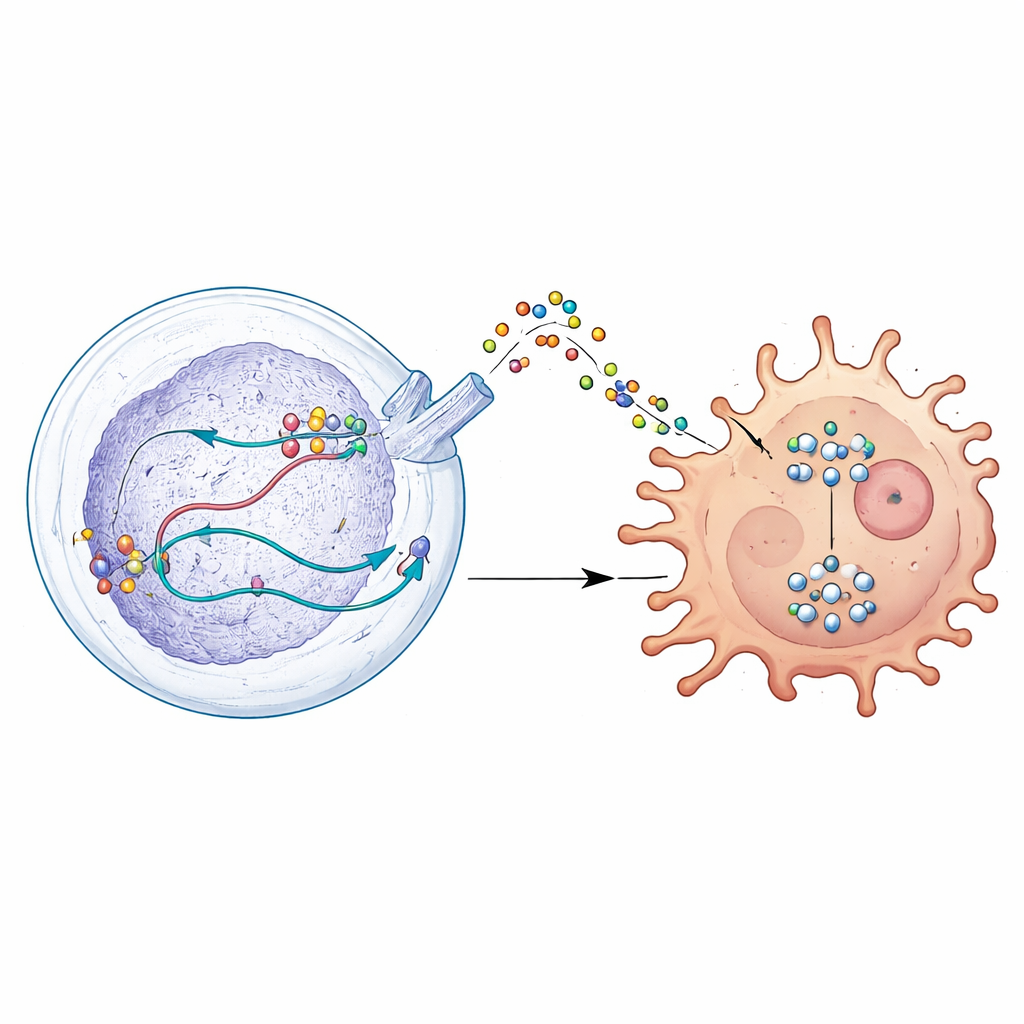
Un segnale segreto che disarma i difensori immunitari
Approfondendo, gli scienziati hanno scoperto che DDX39A modifica il processamento di un gene chiamato WISP1. Invece di limitarsi ad accendere o spegnere WISP1, DDX39A contribuisce a modellarne l’RNA in modo da stabilizzare il messaggio e aumentare la produzione della proteina WISP1. Le cellule tumorali rilasciano poi WISP1 nell’ambiente circostante, dove agisce come un segnale ingannevole. I macrofagi vicini, che possono attaccare i tumori o sostenerli, rispondono a questo segnale spostandosi in uno stato immunosoppressivo e favorevole al tumore. Questo cambiamento è mediato dall’attivazione di una via di controllo della crescita nota come AKT. Quando DDX39A o WISP1 venivano ridotti, questa via si attenuava, le cellule tumorali diventavano meno aggressive e i macrofagi tornavano verso un profilo più anti-tumorale.
Trasformare un farmaco psichiatrico in un’arma contro il cancro
Con questa mappa dei percorsi molecolari, i ricercatori hanno cercato nei database di farmaci molecole in grado di interferire con l’attività di DDX39A. Hanno individuato la flufenazina, un antipsicotico di lunga data noto per raggiungere il cervello. Modellizzazione al computer e test di legame hanno mostrato che la flufenazina può legarsi direttamente a DDX39A. Nelle cellule tumorali, il farmaco indeboliva l’interazione di DDX39A con l’RNA di WISP1, riduceva i livelli di WISP1 e attenuava la segnalazione AKT. Le cellule trattate crescevano meno, invadevano di meno, formavano meno sfere tumorali e tendevano maggiormente alla morte. Nei modelli murini, la flufenazina rallentava la crescita dei tumori cerebrali, riduceva il numero di macrofagi che supportano il tumore e prolungava la sopravvivenza, il tutto a dosi simili a quelle già impiegate nell’uomo per altre condizioni.
Cosa significa per i trattamenti futuri
In termini semplici, questo studio mostra che le cellule di glioblastoma sfruttano DDX39A per mettere a punto un messaggio (WISP1) che sia potenzia la loro resistenza sia riprogramma le cellule immunitarie vicine in guardie del corpo anziché in combattenti. Bloccare questo “aiutante”, geneticamente o con un farmaco come la flufenazina, indebolisce il cancro su due fronti: le stesse cellule tumorali e lo scudo protettivo dei macrofagi immunosoppressivi. Pur essendo necessari molti ulteriori test prima che questa strategia possa arrivare ai pazienti, il lavoro apre una strada promettente per riproporre un medicinale noto colpendo un punto debole appena rivelato in uno dei tumori cerebrali più ostinati.
Citazione: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Parole chiave: glioblastoma, splicing dell'RNA, microambiente tumorale, polarizzazione dei macrofagi, riutilizzo di farmaci