Clear Sky Science · it
PMM2 interagisce con TRIM28 per reclutare E2F4 e promuovere la glicolisi tumorale mediata da KIFC3 e la progressione del carcinoma colorettale
Perché questa storia sul cancro è importante
Il carcinoma colorettale è uno dei tumori più letali al mondo, in parte perché molti tumori imparano a dirottare i sistemi energetici dell’organismo per alimentare una crescita incontrollata. Questo studio svela come un enzima poco noto, PMM2, aiuti i tumori colorettali a bruciare zuccheri in modo più aggressivo e a diffondersi, e spiega perché ciò lo rende un promettente nuovo bersaglio per futuri farmaci e test diagnostici.
Un motore tumorale affamato di zucchero
Le cellule cancerose spesso riorganizzano il modo in cui utilizzano il glucosio, favorendo una forma di combustione dello zucchero ad alta velocità e bassa efficienza nota come glicolisi. I ricercatori hanno iniziato confrontando migliaia di geni in campioni di tumore colorettale con il tessuto sano adiacente. PMM2, un enzima solitamente coinvolto nell’ancoraggio di catene di zuccheri alle proteine, è emerso come uno dei geni maggiormente sovraespressi nel cancro. Le cellule tumorali con PMM2 in eccesso crescevano più velocemente, formavano più colonie e si diffondevano più facilmente in coltura, mentre le cellule in cui PMM2 era spento rallentavano la crescita, migravano meno ed erano più inclini a morire.
Come le cellule tumorali potenziano l’uso dello zucchero
Quando il gruppo ha ridotto i livelli di PMM2 nelle cellule di carcinoma colorettale, le cellule hanno assorbito meno glucosio, prodotto meno ATP (la loro principale valuta energetica) e rilasciato meno lattato, il prodotto di scarto della glicolisi. Misurazioni metaboliche sensibili hanno confermato che l’acidificazione complessiva del mezzo circostante è diminuita, mentre l’uso di ossigeno è aumentato, indicando che le cellule si sono spostate dalla glicolisi sovralimentata verso una respirazione più normale. Anche proteine chiave di supporto alla glicolisi, PKM2 e LDHA, sono diminuite. Sorprendentemente, anche una versione cataliticamente “morta” di PMM2 poteva ancora promuovere questo comportamento affamato di zucchero, dimostrando che il ruolo di PMM2 nel cancro non dipende dalla sua attività enzimatica classica, ma dalle interazioni con altre proteine all’interno della cellula.
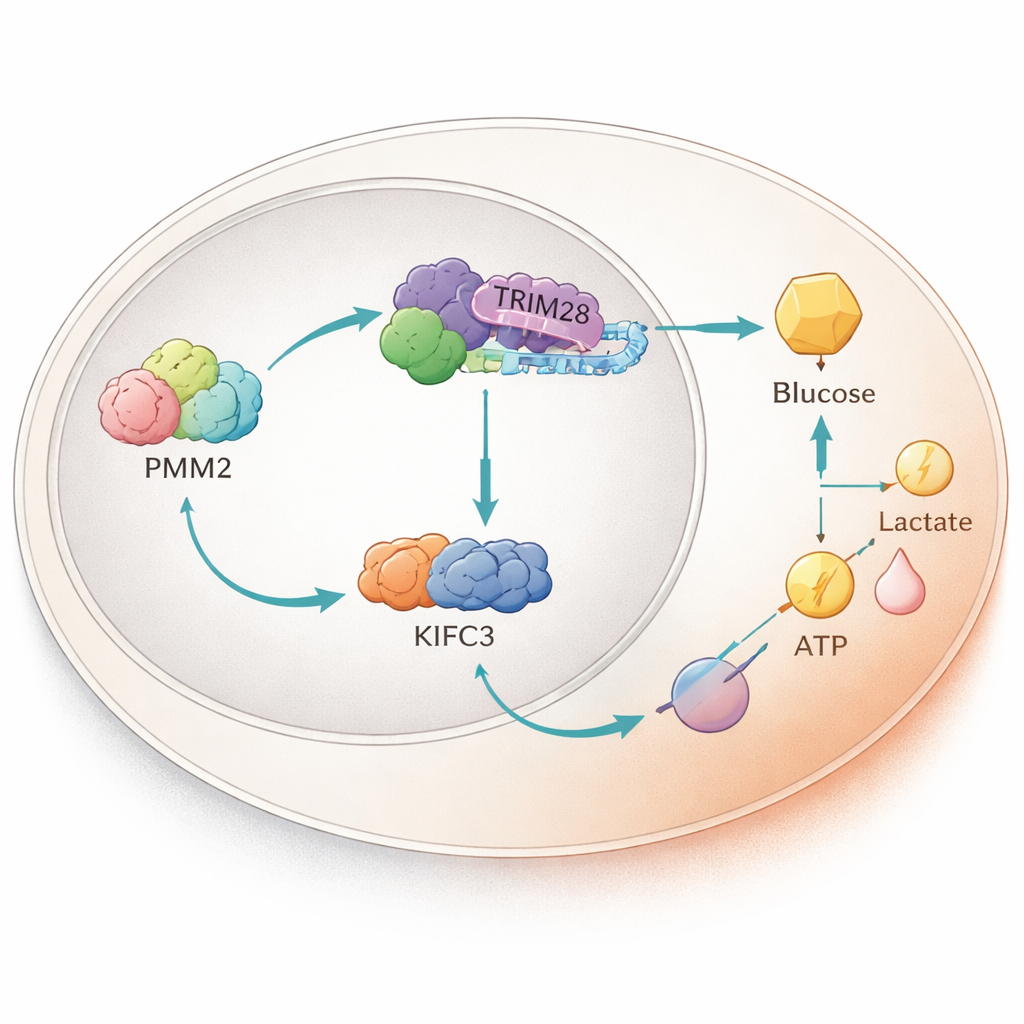
Una staffetta proteica all’interno del nucleo
Approfondendo, gli scienziati hanno scoperto che PMM2 si lega fisicamente a un’altra proteina chiamata TRIM28, che può entrare nel nucleo cellulare e influenzare l’attività genica. PMM2 favorisce l’accumulo di TRIM28 nel nucleo, dove TRIM28 si associa a un fattore di trascrizione, E2F4. Insieme, questo trio aumenta la produzione di una proteina motrice chiamata KIFC3 legandosi a una specifica regione di controllo del suo DNA. Esperimenti che hanno eliminato la regione di PMM2 necessaria per il legame con TRIM28 hanno annullato la capacità di PMM2 di intensificare la glicolisi e la crescita cellulare, sottolineando che è questa collaborazione tra proteine—e non la funzione enzimatica classica di PMM2—a fornire il vantaggio tumorale.
Attivare un interruttore metabolico chiave
KIFC3, noto soprattutto per il suo ruolo nel trasporto di carichi lungo l’impalcatura interna della cellula, si è rivelato un interruttore metabolico cruciale. Quando i ricercatori hanno ridotto i livelli di KIFC3, le cellule di carcinoma colorettale hanno consumato meno glucosio, prodotto meno ATP e lattato e mostrato una ridotta attività glicolitica, mentre il loro uso di ossigeno è aumentato. È importante che il silenziamento di KIFC3 abbia annullato parzialmente l’incremento della glicolisi e il vantaggio di crescita normalmente indotti da PMM2. In topi impiantati con cellule umane di carcinoma colorettale, i tumori con PMM2 in eccesso crescevano di più, ma questo effetto è stato attenuato quando KIFC3 è stato ridotto. I campioni tumorali di questi animali mostravano livelli più elevati di PMM2, KIFC3 e marcatori di glicolisi, collegando l’intera catena di eventi anche nei tessuti viventi.
Dai modelli di laboratorio ai campioni dei pazienti
Per avvicinare il lavoro alla clinica, il team ha creato miniature tridimensionali di tumori, note come organoidi, a partire da carcinomi colorettali di pazienti. Gli organoidi con livelli più alti di PMM2 e KIFC3 crescevano più rapidamente e producevano più ATP e lattato rispetto a quelli con livelli più bassi. Forzare gli organoidi a esprimere più PMM2 aumentava KIFC3 e la glicolisi, mentre ridurre PMM2 aveva effetti opposti. Analisi di matrici tumorali di pazienti hanno inoltre mostrato che alti livelli di PMM2 erano associati a malattia più avanzata, diffusione ai linfonodi e una sopravvivenza globale più breve, indicando PMM2 come un forte candidato a biomarcatore.
Cosa significa questo per le cure future
In termini semplici, questo studio mostra che molti tumori colorettali sembrano inserire PMM2 in una staffetta proteica nucleare—attraverso TRIM28 ed E2F4—per aumentare KIFC3 e, di conseguenza, la loro macchina di combustione degli zuccheri. Questo scatto metabolico aiuta i tumori a crescere e a metastatizzare. Poiché questa via dipende dalle interazioni tra proteine piuttosto che dal ruolo enzimatica abituale di PMM2, apre nuove strade terapeutiche: piccole molecole, peptidi o farmaci degradanti che interrompono il legame di PMM2 con TRIM28, bloccano l’accesso di E2F4 al DNA o attenuano l’attività di KIFC3 potrebbero, in linea di principio, privare i tumori del loro carburante preferito. Sebbene tali terapie non siano ancora disponibili, la catena PMM2–TRIM28–E2F4–KIFC3 si distingue ora come una promettente road map per strategie più precise e focalizzate sul metabolismo contro il carcinoma colorettale.
Citazione: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Parole chiave: carcinoma colorettale, metabolismo tumorale, glicolisi, segnalazione oncogenica, biomarcatore