Clear Sky Science · it
ULK1 promuove la progressione metastatica nei modelli sperimentali del carcinoma ovarico epiteliale
Perché questa ricerca è importante
Il carcinoma ovarico epiteliale viene spesso scoperto solo dopo essersi diffuso silenziosamente nella cavità addominale, rendendolo uno dei tumori più letali che colpiscono le donne. Un passaggio chiave di questa diffusione è la formazione di piccoli aggregati di cellule tumorali, detti sfere o sferoidi, che galleggiano nel liquido addominale, sopravvivono alla chemioterapia e danno origine a nuovi tumori. Questo studio pone una domanda mirata con grandi implicazioni: un “interruttore di sopravvivenza” cellulare chiamato ULK1 aiuta questi aggregati a resistere e a diffondersi, e spegnerlo potrebbe aprire nuove strade per trattare il carcinoma ovarico avanzato?
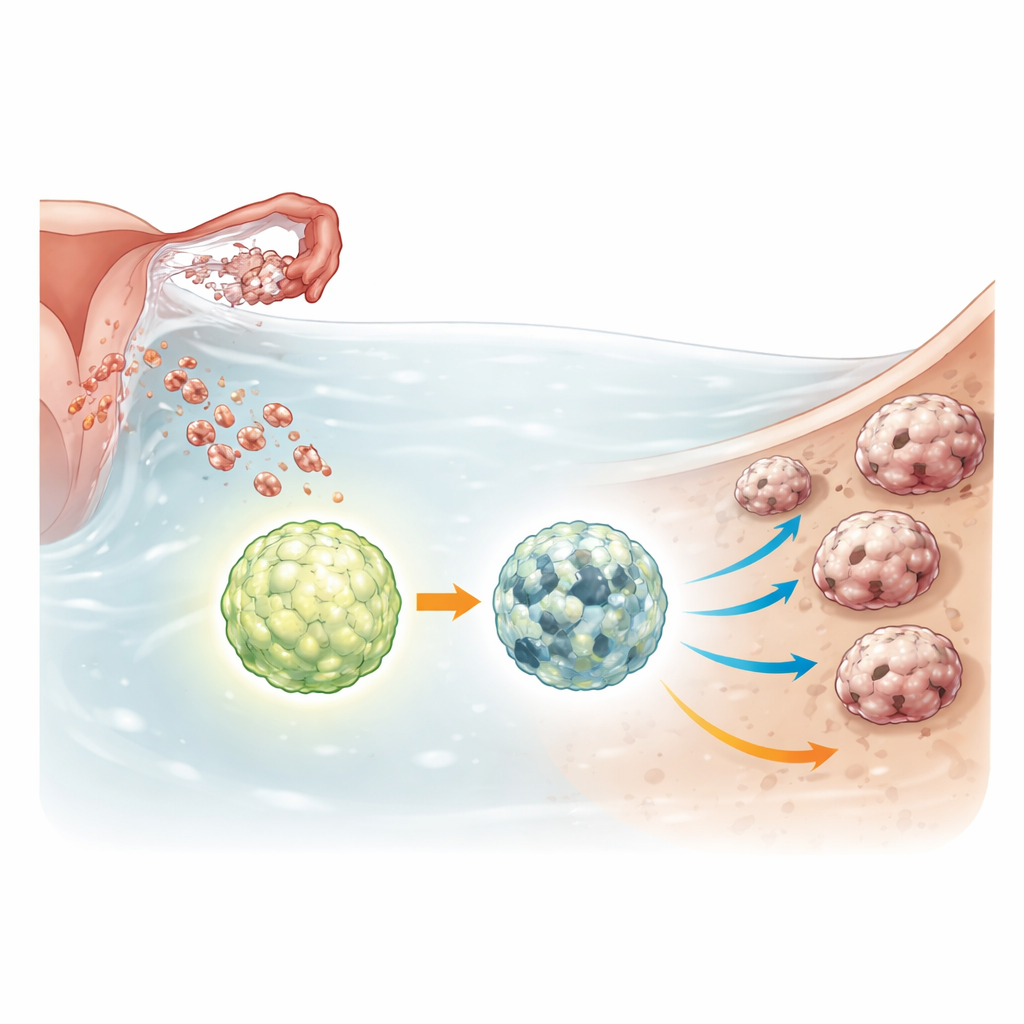
Un interruttore di sopravvivenza all’interno degli aggregati tumorali
I sferoidi del carcinoma ovarico sopportano condizioni avverse: scarsa disponibilità di nutrienti, mancata adesione e esposizione alla chemioterapia. Per affrontare questi stress aumentano un processo di riciclo noto come autofagia, che degrada e riutilizza componenti intracellulari per mantenere le cellule in vita. ULK1 è lo switch maestro che attiva questo sistema di riciclo. I ricercatori hanno usato strumenti di editing genico per rimuovere completamente ULK1 da diverse linee cellulari di carcinoma ovarico e da una linea di cellule non tumorali della tuba di Falloppio che rappresenta stadi precancerosi. Hanno poi confrontato il comportamento delle cellule normali e quelle prive di ULK1 quando venivano coltivate come sferoidi in sospensione o come organoidi tridimensionali.
Cosa succede quando lo switch viene spento
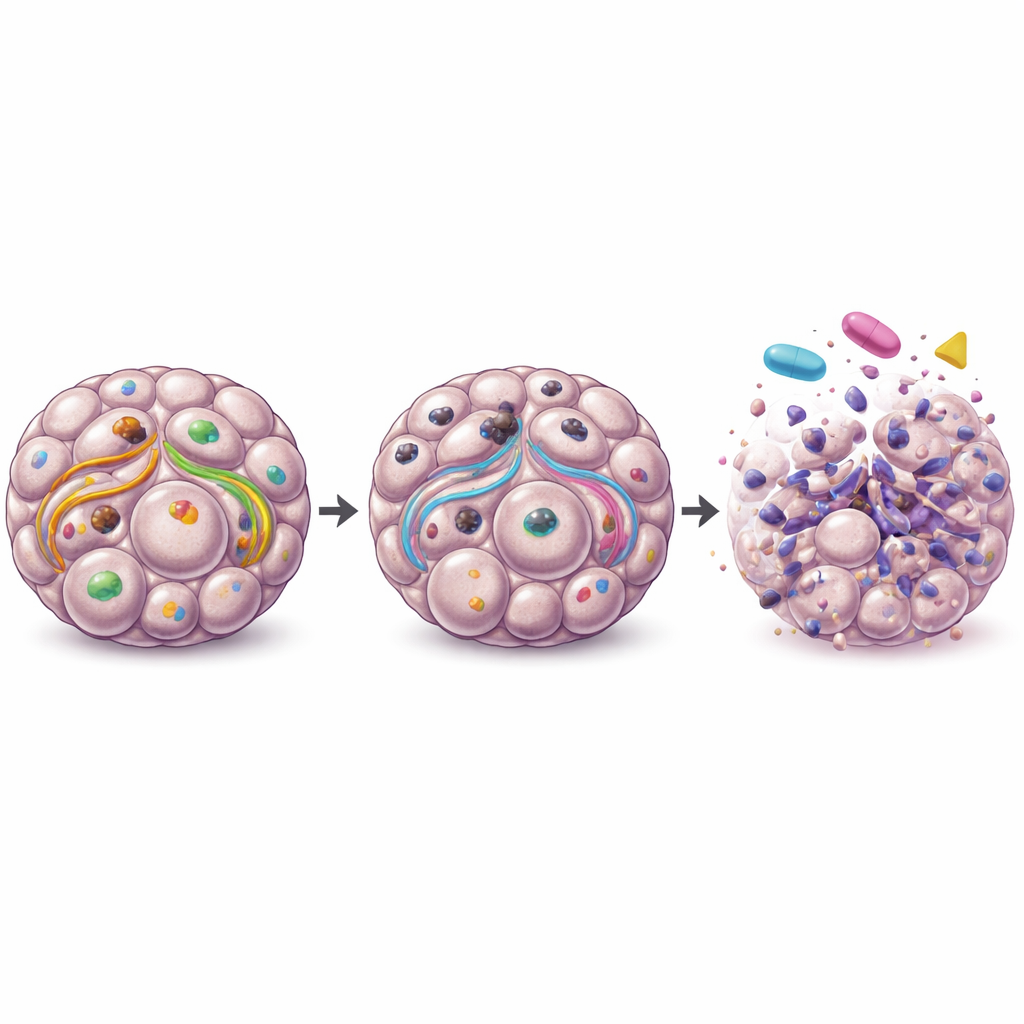
Quando ULK1 è stato eliminato nelle cellule del carcinoma ovarico, la loro capacità di eseguire l’autofagia nei sferoidi è risultata fortemente compromessa, come mostrato dalle variazioni in proteine chiave del riciclo. Questi sferoidi privi di ULK1 contenevano meno cellule vive e mostravano segni aumentati di morte cellulare programmata, indicando che gli aggregati tumorali non riuscivano più a resistere efficacemente alle condizioni di stress. È interessante che la rimozione di ULK1 nelle cellule precursori non tumorali non abbia spento il loro sistema di riciclo allo stesso livello, suggerendo che le cellule tumorali dipendono maggiormente da ULK1 rispetto alle controparti sane. Questa dipendenza specifica del cancro rende ULK1 un bersaglio terapeutico interessante.
Rallentare la diffusione e indebolire gli avamposti tumorali
Oltre alla sopravvivenza in sospensione, i sferoidi devono attaccarsi e invadere il rivestimento liscio della cavità addominale per formare nuovi tumori. Utilizzando modelli in vitro che imitano questo primo passo della metastasi, il gruppo ha mostrato che i sferoidi privi di ULK1 erano nettamente meno efficaci nel spingere via e invadere uno strato di cellule mesoteliali, che normalmente rivestono gli organi addominali. Quando coltivate come organoidi incapsulati in una matrice gelatinosa, le cellule tumorali senza ULK1 formavano anche strutture tumorali più piccole e meno robuste. Nei modelli murini in cui cellule umane di carcinoma ovarico venivano iniettate nella cavità addominale, la perdita di ULK1 ha portato a un numero inferiore di depositi tumorali e a minore accumulo di liquido, entrambi segni distintivi di malattia avanzata, anche se la sopravvivenza complessiva degli animali non è migliorata.
Indebolire segnali chiave e potenziare l’effetto di farmaci mirati
Per capire come ULK1 supporti il cancro oltre l’autofagia, i ricercatori hanno mappato i cambiamenti proteici nei sferoidi privi di ULK1. Hanno rilevato che importanti vie di crescita e sopravvivenza intracellulare—soprattutto le vie MEK–MAPK e PI3K–AKT–mTOR—erano disturbate. Queste vie normalmente aiutano le cellule tumorali a resistere alla morte e a continuare a dividersi. Quando il team ha trattato i sferoidi privi di ULK1 con farmaci che bloccano MEK o mTOR, gli aggregati tumorali sono diventati molto più vulnerabili, con una vitalità e una capacità di riadesione drasticamente ridotte. Al contrario, la rimozione di ULK1 non ha migliorato l’efficacia dei comuni chemioterapici come carboplatino, paclitaxel, o dell’inibitore PARP olaparib, e in alcune condizioni sembra anzi averne attenuato il beneficio.
Indizi dai tumori dei pazienti e dai modelli miniaturizzati
Analizzando grandi database pubblici di tumori ovarici, gli autori hanno riscontrato che un’attività genica più elevata di ULK1 era associata a una peggiore sopravvivenza a lungo termine ed era particolarmente aumentata nei campioni metastatici rispetto ai tumori primari e al tessuto normale. Per avvicinarsi alla clinica, hanno testato una compressa clinica che blocca ULK1, DCC-3116, su organoidi derivati da pazienti coltivati da campioni metastatici. In una sottopopolazione di questi modelli di pazienti, il blocco di ULK1 da solo, o l’uso isolato di farmaci per MEK o mTOR, ha ridotto la sopravvivenza degli organoidi, sebbene la combinazione degli agenti non abbia aggiunto in modo coerente un beneficio ulteriore. Altri organoidi di pazienti erano resistenti a tutti i trattamenti, sottolineando quanto i carcinomi ovarici possano essere diversi e la necessità di biomarcatori per identificare chi potrebbe trarne vantaggio.
Cosa significa per le cure future
Complessivamente, i risultati dipingono ULK1 come un collaboratore centrale della diffusione del carcinoma ovarico: alimenta il riciclo interno che mantiene vivi i sferoidi, sostiene la loro capacità di invadere nuovi siti e contribuisce a mantenere potenti segnali di crescita. Spegnere ULK1 indebolisce questi processi, riduce i tumori sperimentali e rende gli aggregati tumorali più sensibili ad alcuni farmaci mirati, sebbene non alla chemioterapia standard. Per i pazienti, questo lavoro suggerisce che ULK1 potrebbe entrare a far parte di una strategia di medicina di precisione—soprattutto per chi ha malattia metastatica con elevata espressione di ULK1—in cui inibitori mirati di ULK1 vengono combinati con bloccanti di MEK o mTOR per limitare la crescita e la diffusione tumorale, a condizione che test accurati possano identificare quali tumori sono più probabilmente responsivi.
Citazione: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Parole chiave: cancro ovarico, metastasi, autofagia, ULK1, terapia mirata