Clear Sky Science · it
Associazione tra retinoidi, recettori dell’acido retinoico ed epigenetica nel carcinoma mammario
Perché la vitamina A è importante nel carcinoma mammario
La maggior parte delle persone conosce la vitamina A come un nutriente importante per la vista, ma la sua forma attiva nell’organismo, l’acido retinoico, aiuta anche le cellule a decidere se proliferare, specializzarsi o autodistruggersi quando danneggiate. Questo articolo di revisione esamina come l’acido retinoico e le sue “stazioni di ancoraggio” cellulari siano alterati nel carcinoma mammario, perché risultati promettenti in laboratorio non si sono ancora tradotti in farmaci efficaci per i pazienti e come nuove conoscenze sul “software” delle cellule tumorali — il loro codice epigenetico — possano rilanciare questa strategia terapeutica.
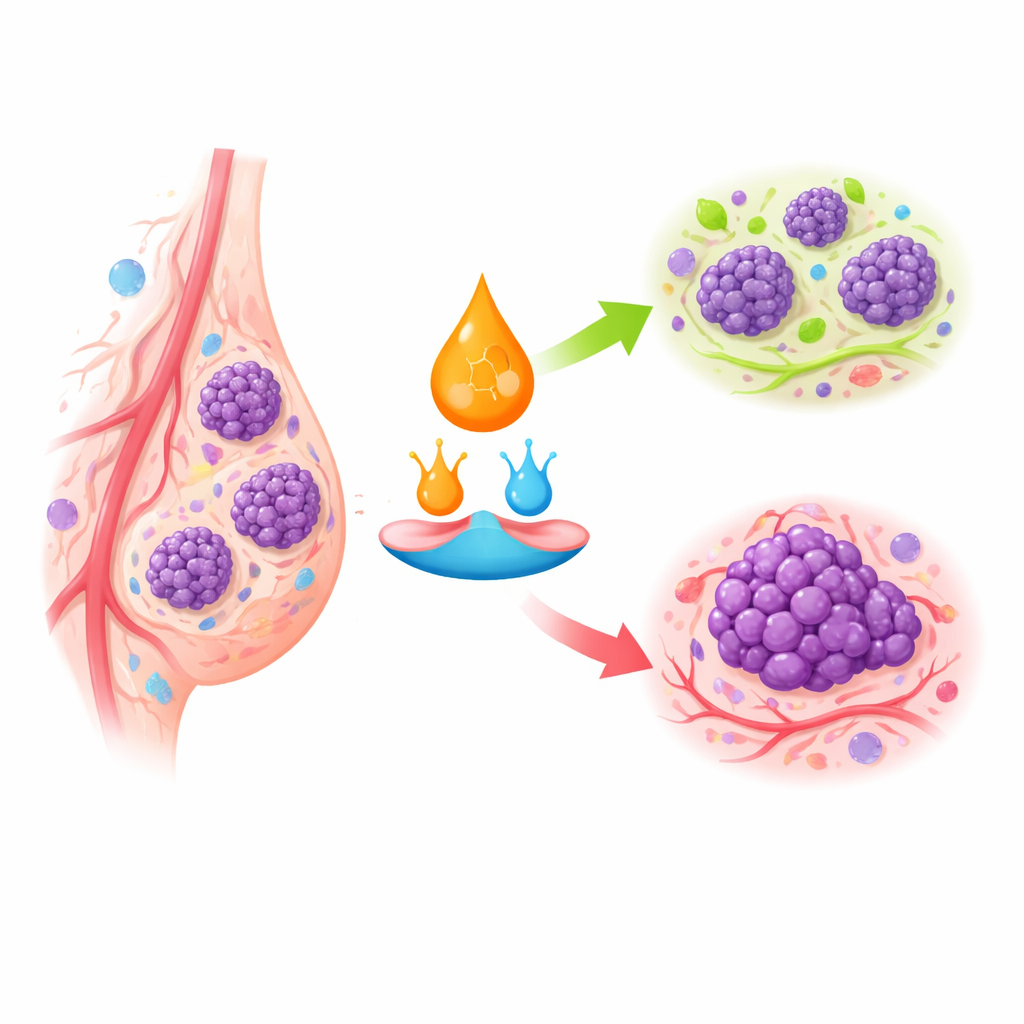
Semafori cellulari per crescita e autodistruzione
L’acido retinoico agisce legandosi a recettori specifici all’interno delle cellule, che a loro volta attivano o disattivano interi gruppi di geni. Nel tessuto mammario sano, questo sistema incoraggia le cellule a interrompere la divisione, maturare in forme stabili o morire se diventano anomale. Nel carcinoma mammario, specialmente nei sottotipi più aggressivi, recettori chiave sono assenti o silenziati e il trasporto interno dell’acido retinoico viene deviato. Invece di essere consegnato a recettori che rallentano la crescita, può essere indirizzato verso vie che favoriscono la sopravvivenza e la proliferazione. Questo aiuta a spiegare perché alcuni tumori mammari rispondono poco ai farmaci retinoidi nonostante gli stessi farmaci siano altamente efficaci in alcuni tumori del sangue.
Interruttori nascosti nel software della cellula tumorale
Gli autori si concentrano sull’epigenetica — marcatori chimici sul DNA e sulle proteine che lo avvolgono che funzionano come impostazioni software per il genoma. In molti carcinomi mammari, questi marcatori bloccano importanti recettori dell’acido retinoico, in particolare uno chiamato RARβ2, in una posizione “off” senza alterare la sequenza di DNA sottostante. Gruppi metile in eccesso sul DNA e il restringimento del nucleo proteico circostante spengono questo recettore, mentre altri enzimi rimodellano il paesaggio della cromatina a favore della crescita e della migrazione. RNA non codificanti, che non producono proteine ma influenzano l’attività genica, spostano ulteriormente i segnali lontano dalla morte cellulare e dalla differenziazione. Insieme, questi cambiamenti conferiscono alle cellule tumorali la flessibilità per resistere ai trattamenti e adattarsi allo stress.
Riprogrammare le vie di segnale
È importante che questi blocchi epigenetici siano reversibili. Nei modelli di laboratorio, farmaci che rimuovono la metilazione del DNA o allentano la cromatina possono ripristinare RARβ2 e altri componenti della via dell’acido retinoico. Quando combinati con l’acido retinoico stesso e la chemioterapia standard, questi agenti «priming» riducono i tumori in modo più efficace e diminuiscono la riserva di cellule di tipo staminale ritenute responsabili delle recidive. Anche il modo in cui l’acido retinoico viene trasportato all’interno della cellula è determinante: una proteina trasportatrice lo guida verso recettori che sopprimono la crescita, mentre un’altra lo indirizza verso vie pro‑crescita. Modulare l’equilibrio tra questi vettori può trasformare l’acido retinoico da fertilizzante a freno.
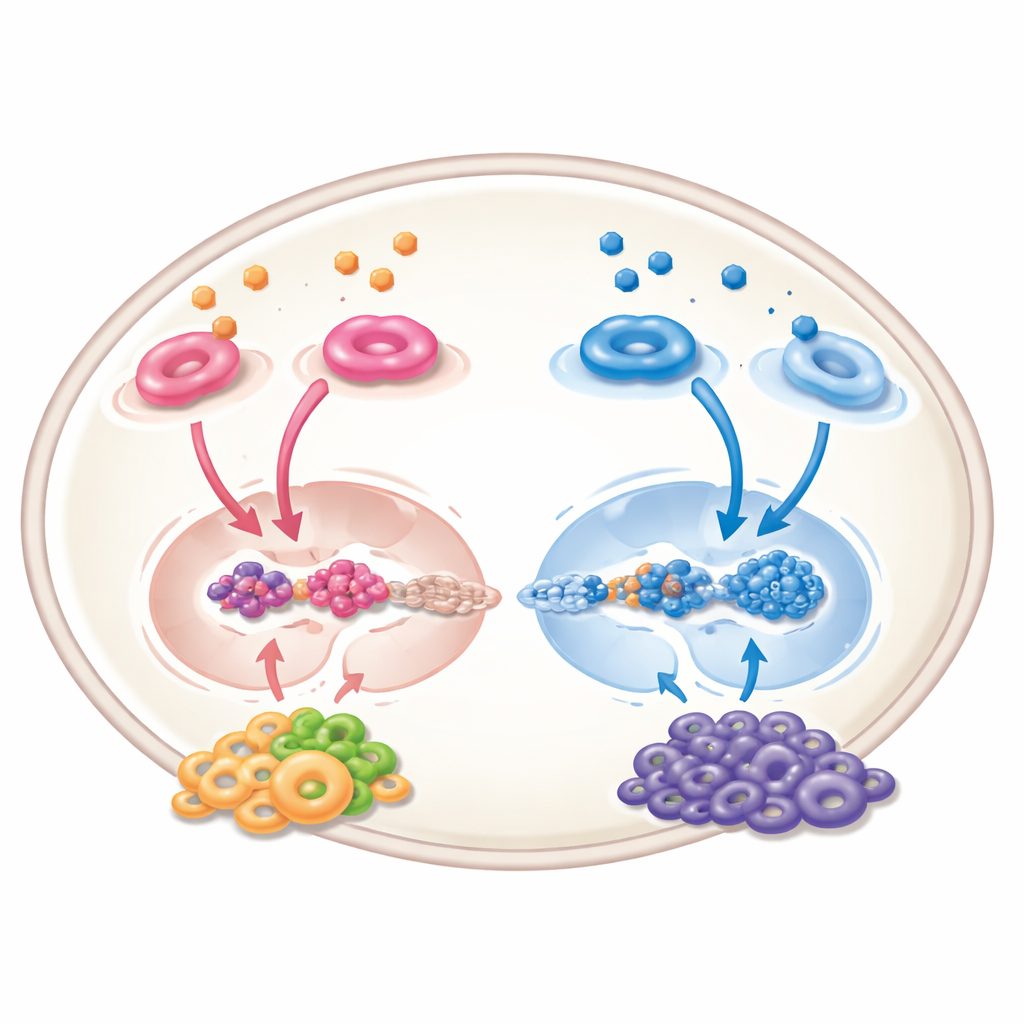
Oltre il tumore: l’effetto del quartiere
L’acido retinoico non agisce solo sulle cellule tumorali; rimodella anche il «quartiere» che circonda il tumore fatto di vasi sanguigni, cellule immunitarie e cellule di supporto. Nei sistemi sperimentali può ridurre la neoangiogenesi, indirizzare le cellule immunitarie verso uno stato più attivo e anti‑tumorale e limitare le cellule soppressive che normalmente attenuano le difese dell’organismo. Tuttavia la storia non è interamente positiva: in certi tipi di cellule stromali che circondano il tumore, l’attivazione della segnalazione dell’acido retinoico può effettivamente promuovere la crescita tumorale rafforzando i canali di comunicazione chimica che attraggono e sostengono le cellule maligne. Questi effetti opposti implicano che qualsiasi futura terapia dovrà essere calibrata con attenzione per colpire i tipi cellulari giusti nel modo giusto.
Progettare studi clinici più intelligenti per il futuro
I primi studi clinici sui retinoidi nel carcinoma mammario sono in gran parte falliti, ma sono stati condotti prima della comprensione odierna dei sottotipi, dei biomarcatori e della farmacologia complessa. Gli autori sostengono che i nuovi trial dovrebbero selezionare pazienti i cui tumori mostrano i segni molecolari di sensibilità ai retinoidi, come l’espressione conservata dei recettori o specifici pattern di metilazione del DNA, e dovrebbero associare i retinoidi a farmaci che sbloccano i blocchi epigenetici, colpiscono le vie di crescita o potenziano l’attacco immunitario. Formulazioni migliorate che mantengano livelli farmacologici stabili nell’organismo, insieme a un monitoraggio accurato sia del tumore sia del tessuto circostante, saranno cruciali. Se questi ostacoli potranno essere superati, i trattamenti a base di acido retinoico potrebbero ancora trovare posto come strumenti di precisione contro forme selezionate di carcinoma mammario.
Citazione: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Parole chiave: acido retinoico, carcinoma mammario, epigenetica, terapia della differenziazione, microambiente tumorale