Clear Sky Science · it
Modellare il dialogo tessuto adiposo-cancro: una prospettiva tridimensionale
Perché grasso e cancro sono più vicini di quanto si pensi
La maggior parte di noi considera il grasso corporeo come un’imbottitura in eccesso o come riserva di energia, ma la ricerca rivela oggi che è un organo attivo e comunicativo che può influenzare la nostra salute in modi sorprendenti. Questa rassegna esplora come il tessuto adiposo e le cellule tumorali comunicano e come nuovi modelli di laboratorio tridimensionali (3D) aiutino gli scienziati a riprodurre quel dialogo in modo più realistico che mai. Comprendere questa conversazione nascosta potrebbe migliorare la prevenzione del cancro, i test farmacologici e i trattamenti, specialmente in un mondo sempre più sovrappeso. 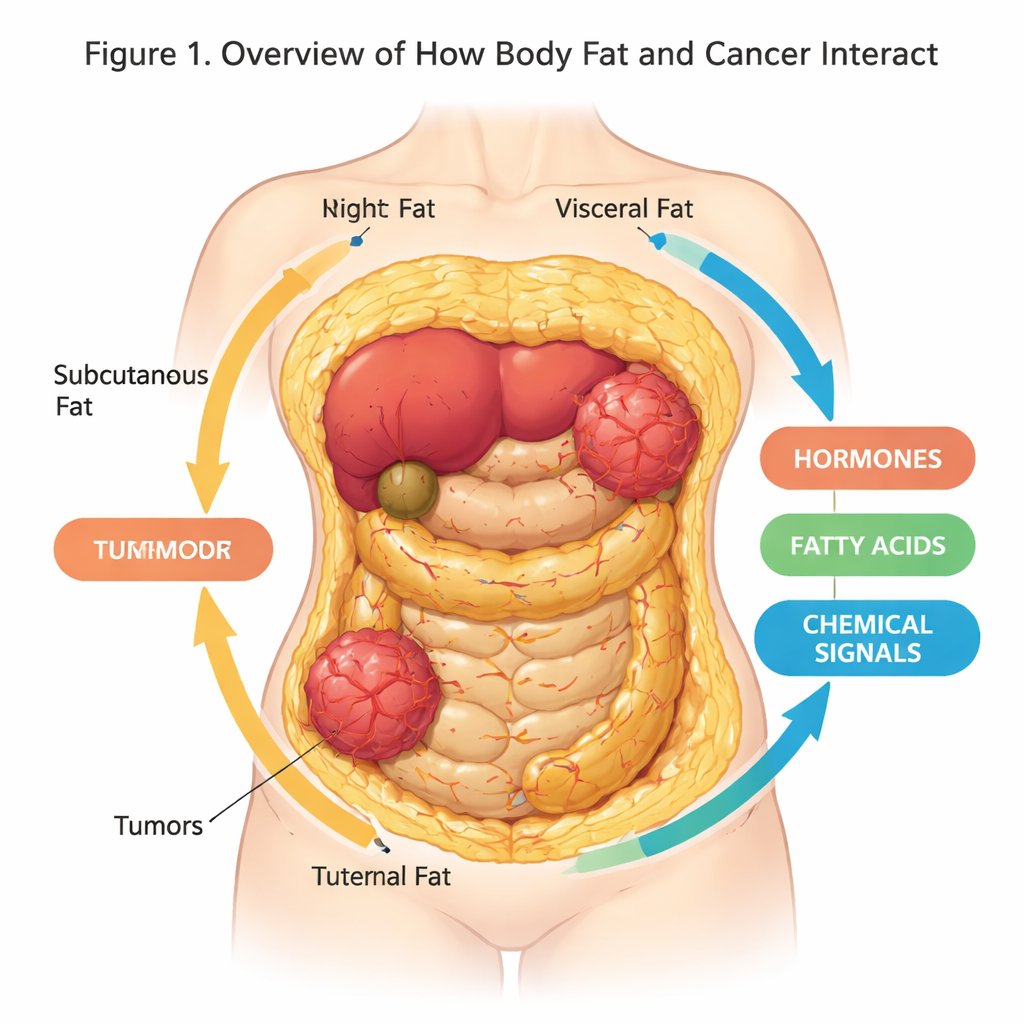
Il grasso come organo vivente e comunicante
Il tessuto adiposo—il nostro grasso corporeo—non è solo un deposito passivo. È un organo complesso composto da adipociti, cellule immunitarie, vasi sanguigni e cellule di supporto, tutti immersi in una rete strutturale nota come matrice extracellulare. Esistono diversi tipi di grasso in sedi diverse: il grasso sottocutaneo sotto la pelle, il grasso viscerale intorno agli organi interni, e adipociti bianchi, bruni e beige che variano nel modo in cui immagazzinano energia o la dissipano come calore. Queste cellule rilasciano costantemente un cocktail di ormoni, acidi grassi e proteine segnale che influenzano metabolismo, infiammazione e, come sappiamo ora, il rischio e il comportamento del cancro.
Obesità, infiammazione e rischio di cancro
Quando acquistiamo troppo peso, gli adipociti bianchi aumentano di dimensione e numero e il tessuto subisce stress e infiammazione. Questo grasso “non sano” rilascia più molecole infiammatorie e acidi grassi nel circolo sanguigno, gestendo meno efficacemente zuccheri e lipidi. Ampi studi epidemiologici hanno collegato l’obesità a un rischio maggiore e a esiti peggiori per molti tumori, inclusi quelli al seno, al colon, al pancreas e all’utero. La rassegna spiega come il grasso disfunzionale possa nutrire i tumori con carburante extra, irrigidire il tessuto circostante e reclutare altri tipi cellulari che insieme creano un ambiente più favorevole al cancro.
Una conversazione bidirezionale tra grasso e tumori
Il cancro è oggi visto come una malattia di un intero ecosistema, non solo di cellule fuori controllo. Le cellule tumorali attingono al grasso vicino per ottenere sostegno, riprogrammando adipociti, cellule immunitarie e fibroblasti per aiutarle a crescere e diffondersi. In cambio, gli adipociti rispondono degradando i lipidi immagazzinati e rilasciando acidi grassi e ormoni che le cellule tumorali possono utilizzare facilmente. Questo scambio può avvenire a distanza tramite segnali circolanti, o localmente dove i tumori crescono accanto al grasso, come nel seno o nell’addome. Le cellule tumorali possono persino indurre gli adipociti a perdere la loro identità originale e a diventare più simili a cellule che formano cicatrici o a cellule di tipo immunitario che rimodellano il tessuto e favoriscono l’invasione. 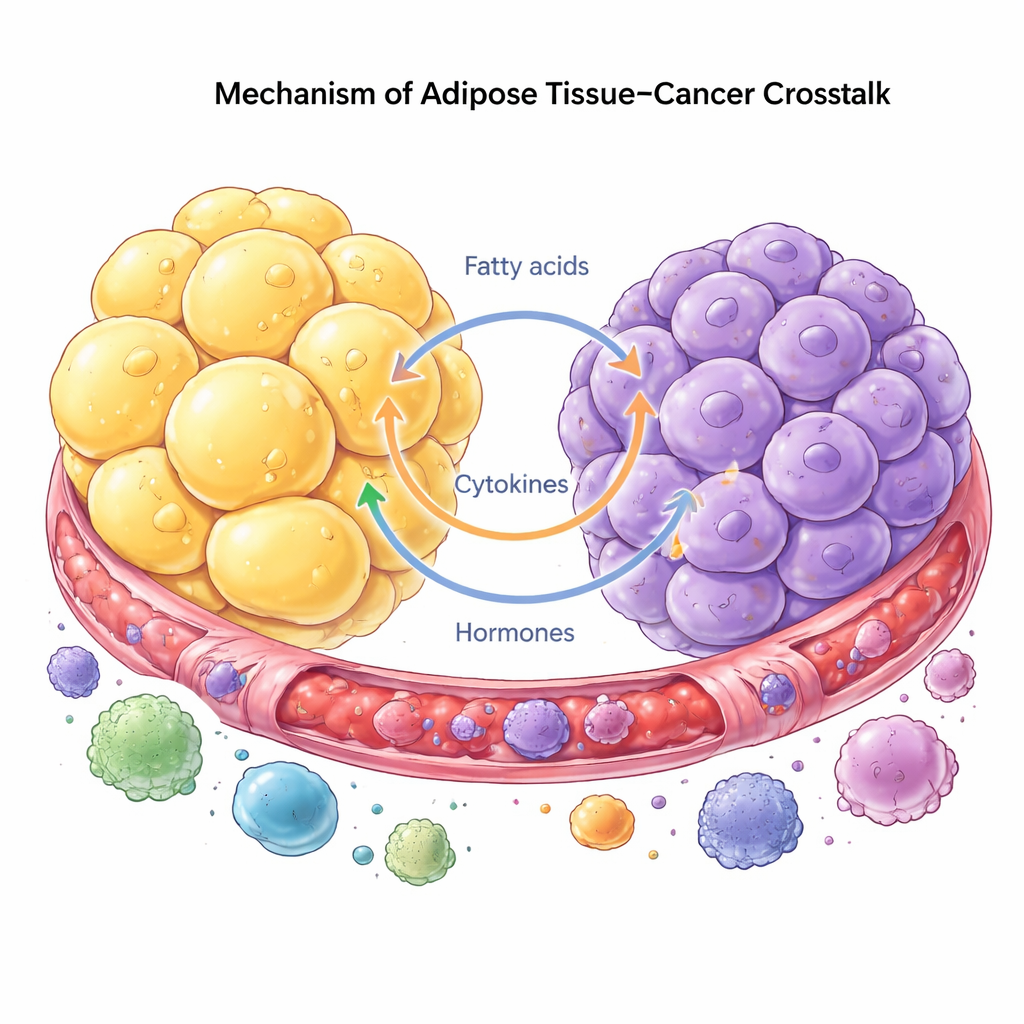
Costruire mini-tessuti in 3D
Le tradizionali colture cellulari piatte (2D) e i modelli animali spesso non riescono a catturare queste interazioni complesse. Gli autori descrivono una nuova generazione di sistemi 3D che somigliano meglio ai tessuti reali. Gli sferoidi sono semplici aggregati cellulari che si auto-assemblano in piccole sfere; gli scaffold sono materiali ingegnerizzati che forniscono un supporto tridimensionale per la crescita cellulare; gli organoidi sono versioni in miniatura e auto-organizzanti dei tessuti; e gli assembloidi combinano più organoidi o sferoidi in «mini-organi» compositi. I ricercatori stanno ora usando questi approcci 3D per co-coltivare adipociti e cellule tumorali, studiare come condizioni simili all’obesità ne modifichino il comportamento e testare come i farmaci possano interrompere il dialogo dannoso tra di loro.
Promesse e lacune attuali
Ogni modello presenta compromessi. Gli sferoidi sono economici e adatti ad alti volumi ma relativamente semplici. Gli scaffold consentono un controllo accurato delle proprietà fisiche come la rigidità, che può influenzare la diffusione del cancro, ma sono più complessi da realizzare. Organoidi e assembloidi catturano il livello più alto di realismo, con molteplici tipi cellulari in interazione, tuttavia sono costosi, difficili da standardizzare e spesso privi di reti vascolari complete o componenti immunitarie. La rassegna sottolinea che i sistemi attuali sono ancora lontani dal riprodurre perfettamente il tessuto adiposo e tumorale umano, in particolare nel replicare la matrice extracellulare completa, adipociti maturi e la partecipazione delle cellule immunitarie.
Dove sta andando questa ricerca
Gli autori concludono che migliorare i modelli 3D delle interazioni grasso–cancro è essenziale per test farmacologici più accurati e per scoprire come l’obesità promuova il cancro. Man mano che questi «mini-tessuti» diventano più realistici—combinando grasso realistico, cellule tumorali, vasi sanguigni e cellule immunitarie—potrebbero aiutare i ricercatori a predire quali trattamenti funzioneranno in pazienti specifici, progettare strategie migliori per bloccare l’uso del grasso corporeo come combustibile da parte del cancro e, in ultima analisi, guidare terapie che mirino non solo ai tumori ma anche agli ambienti non sani che ne favoriscono la crescita.
Citazione: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Parole chiave: tessuto adiposo, obesità, microambiente tumorale, coltura cellulare 3D, metabolismo tumorale