Clear Sky Science · it
POM121 O-GlcNAcilazione facilita la metastasi ossea nel carcinoma polmonare non a piccole cellule attraverso un aumentato trasporto nucleare di c-MYC e il riprogrammamento della matrice extracellulare
Perché questa ricerca è importante
Quando il cancro ai polmoni si diffonde alle ossa provoca dolore pungente, fratture e una riduzione marcata della sopravvivenza, eppure i medici dispongono ancora di pochi strumenti per arrestare questo passaggio letale. Questo studio esplora i meccanismi interni delle cellule tumorali polmonari per capire come alcune di esse acquisiscano un vantaggio che permette loro di migrare dal polmone all’osso e prosperare lì. Tracciando il processo fino a piccole modifiche su una singola proteina guardiana al confine del nucleo cellulare, gli autori identificano una nuova catena di eventi che potrebbe essere sfruttata per prevedere, prevenire o trattare meglio le metastasi ossee nei pazienti con carcinoma polmonare non a piccole cellule.
Un’etichetta zuccherina che cambia il comportamento del cancro
I ricercatori si sono concentrati sulle modificazioni post-traduzionali, piccoli cambi chimici che le proteine acquisiscono dopo la loro sintesi. Una di queste modifiche, chiamata O-GlcNAcilazione, è l’attacco di un piccolo zucchero in posizioni specifiche delle proteine. Utilizzando linee cellulari di cancro polmonare e modelli murini, il gruppo ha confrontato cellule tumorali ordinarie con sottopopolazioni selezionate ripetutamente per la loro capacità di colonizzare l’osso. Hanno scoperto che queste cellule con predilezione per l’osso presentavano livelli complessivi di O-GlcNAcilazione molto più alti, guidati da una maggiore attività dell’enzima OGT, che installa l’etichetta zuccherina. Tra centinaia di proteine modificate, una è emersa in particolare: POM121, un componente centrale del poro nucleare, la struttura che controlla il traffico dentro e fuori dal nucleo cellulare.
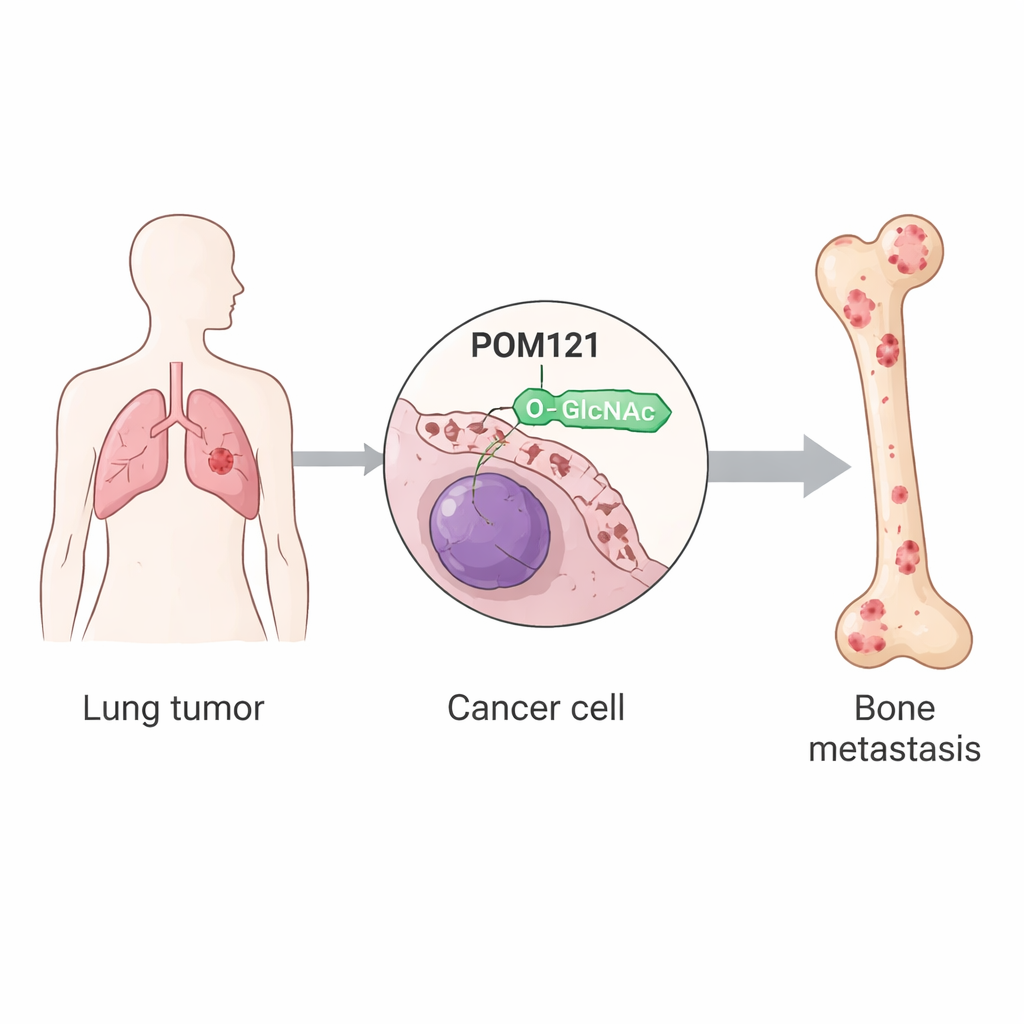
Il guardiano nucleare POM121 viene stabilizzato
POM121 si trova nella membrana che circonda il nucleo, formando parte del canale attraverso cui devono passare molte proteine di segnalazione. Nelle cellule di carcinoma polmonare metastatiche all’osso, POM121 portava un carico elevato di O-GlcNAc in una singola posizione amminoacidica chiamata serina 199. Quando questo sito veniva modificato in modo da non poter più essere O-GlcNAcilato, la proteina diventava instabile ed veniva rapidamente degradata dai meccanismi cellulari di smaltimento. Lo studio mostra che l’etichetta zuccherina protegge POM121 dall’essere contrassegnato per la distruzione da un enzima chiamato TRIM21, che normalmente attacca etichette di ubiquitina come segnali di smaltimento. Con l’O-GlcNAc presente, TRIM21 non si lega efficacemente, l’ubiquitinazione diminuisce e POM121 si accumula al poro nucleare senza cambiare la sua localizzazione.
Aprire la porta a un potente promotore tumorale
Che effetto ha un POM121 più stabile? La chiave sta in una famosa proteina promotrice del cancro, il fattore di trascrizione c-MYC. c-MYC deve entrare nel nucleo per attivare i geni, ma il suo passaggio dipende da componenti del poro nucleare come POM121. Gli autori hanno mostrato che quando POM121 era abbondante e O-GlcNAcilato, più c-MYC si trovava all’interno del nucleo; quando i livelli di POM121 venivano ridotti o la sua etichetta zuccherina rimossa, l’importazione nucleare di c-MYC calava bruscamente. Nei topi, le cellule di carcinoma polmonare portatrici del mutante di POM121 non modificabile formarono molte meno e più piccole metastasi ossee, mentre il ripristino di c-MYC in cellule carenti di POM121 recuperò gran parte della loro capacità di colonizzazione ossea. Ciò colloca POM121 a monte di c-MYC in una via metastatica critica.
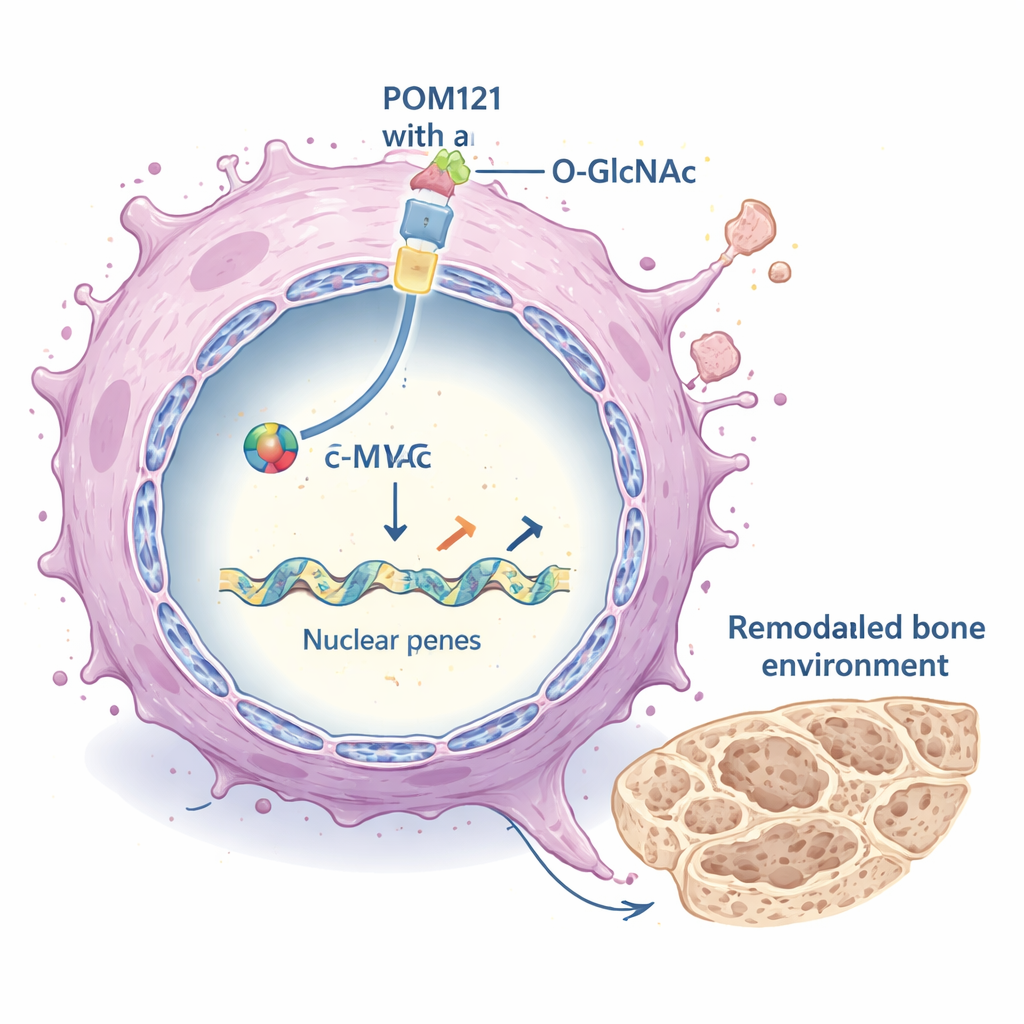
Riprogrammare l’ambiente tumorale
Una volta nel nucleo, c-MYC agisce come un interruttore maestro per molti geni. Qui è stato trovato come forte attivatore di un insieme di geni che modellano la matrice extracellulare (ECM) – l’impalcatura di proteine che circonda le cellule. Questi geni dell’ECM, che includono vari collageni ed enzimi che rimodellano la struttura tessutale, venivano repressi quando POM121 o c-MYC venivano bloccati e attivati quando O-GlcNAcilazione e POM121 erano elevati. L’ECM alterata a sua volta potenziava importanti vie di crescita all’interno delle cellule tumorali, in particolare la cascata di segnalazione PI3K–AKT–mTOR, che sostiene la sopravvivenza, la crescita e la diffusione. Schemi simili apparivano in diversi modelli di carcinoma polmonare, suggerendo che questo meccanismo non è limitato a una singola linea cellulare.
Dalla scoperta in laboratorio all’impatto sui pazienti
Analizzando i dati dei pazienti, i ricercatori hanno riscontrato che livelli elevati di OGT, POM121 e c-MYC, così come dei geni ECM da loro regolati, erano associati a esiti peggiori e a tumori polmonari che avevano già metastatizzato alle ossa. Nel complesso, il lavoro delinea un asse OGT–POM121–c-MYC–ECM: un’eccessiva O-GlcNAcilazione stabilizza il guardiano nucleare POM121, che trasporta più c-MYC nel nucleo, il quale poi riprogramma lo scaffold tissutale e i segnali di crescita a favore della metastasi ossea. Per i pazienti, questo suggerisce nuovi tipi di biomarcatori per identificare chi è a rischio di diffusione ossea e nuovi approcci terapeutici – dal bloccare l’attività di OGT o POM121 all’attenuare c-MYC o il rimodellamento dell’ECM – che un giorno potrebbero aiutare a impedire al cancro polmonare di raggiungere lo scheletro.
Citazione: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Parole chiave: metastasi ossea carcinoma polmonare, POM121, O-GlcNAcilazione, c-MYC, matrice extracellulare