Clear Sky Science · it
La sortilina mostra unʼattività simile a un soppressore tumorale limitando la funzione di trasduzione di EGFR
Perché questo è importante per la cura del cancro
Il cancro ai polmoni è la principale causa di decessi per tumore nel mondo, e molti farmaci moderni prendono di mira una proteina chiamata EGFR che guida la crescita tumorale. Questi farmaci funzionano spesso bene allʼinizio, ma i tumori diventano comunemente resistenti. Questo studio scopre un “freno” naturale allʼinterno delle cellule del cancro polmonare—un ruolo inatteso per una proteina chiamata sortilina—che può attenuare i segnali pro‑tumorali di EGFR. Comprendere questa relazione potrebbe aiutare a spiegare perché alcuni pazienti rispondono meglio alle terapie mirate contro EGFR e suggerire nuovi modi per prolungarne lʼefficacia. 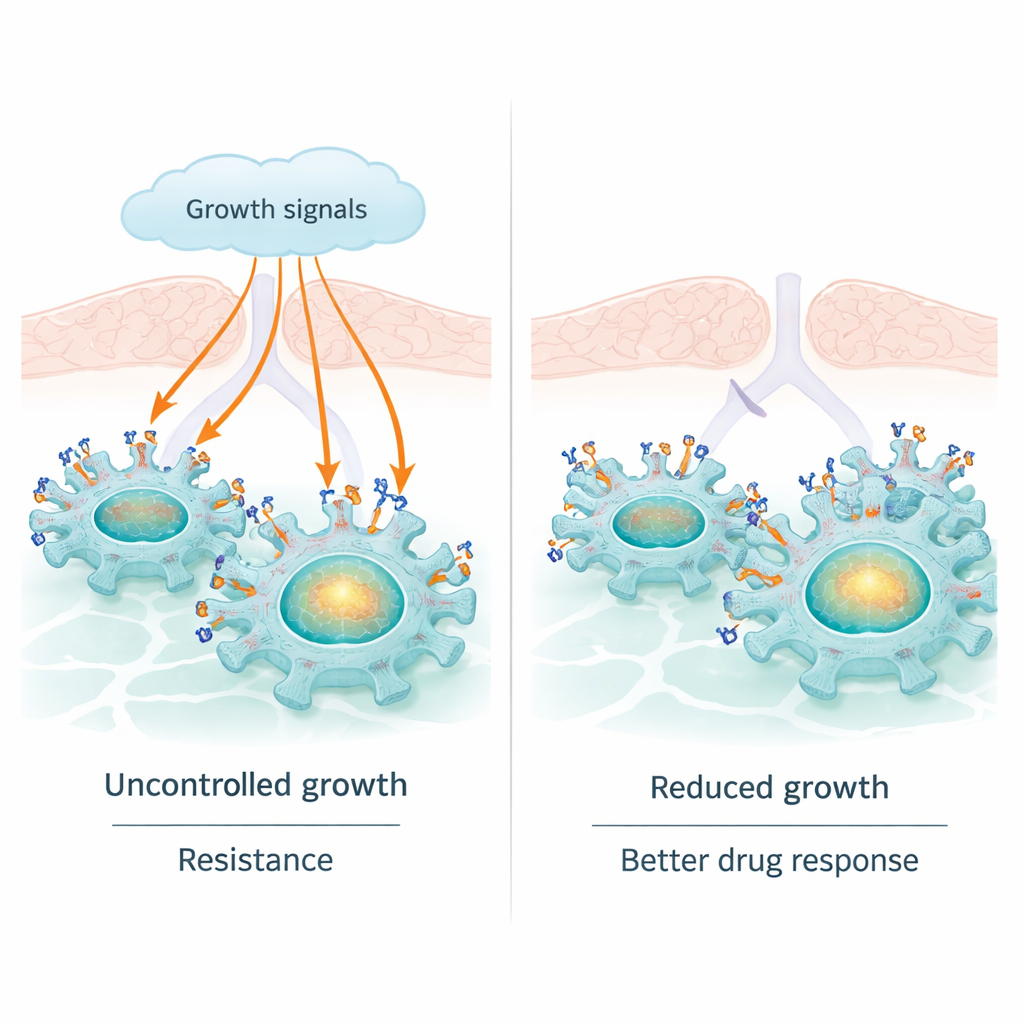
Un interruttore di crescita andato in sovra‑regime
EGFR è un recettore presente sulla superficie di molte cellule, dove rileva segnali di crescita dallʼambiente. In una larga parte degli adenocarcinomi polmonari, EGFR è alterato in modo tale da restare permanentemente attivato. Questo alimenta una crescita e divisione costanti, ed è il motivo per cui le pillole che bloccano EGFR, chiamate inibitori della tirosina chinasi, possono ridurre i tumori. Ma EGFR ha un altro aspetto, meno considerato: può spostarsi nel nucleo della cellula e agire direttamente sul DNA, attivando geni come cMYC e CCND1 che potenziano ulteriormente crescita, sopravvivenza e resistenza alle terapie. Questo ruolo nucleare di EGFR può aiutare i tumori a sfuggire anche quando la sua attività di superficie è chimicamente bloccata.
La sortilina entra nel nucleo
La sortilina era nota principalmente come una proteina di smistamento che favorisce lʼinternalizzazione di EGFR dalla superficie cellulare e il suo invio verso la degradazione, indebolendo così i suoi segnali di crescita. In questo lavoro, gli autori mostrano che la sortilina segue anche EGFR nel nucleo quando le cellule del cancro polmonare sono stimolate. Utilizzando microscopia ad alta risoluzione e frazionamento biochimico, hanno osservato complessi di EGFR e sortilina formarsi allʼinterno dei nuclei poco dopo lʼattivazione. Importante, quando EGFR non poteva entrare nel nucleo, anche la sortilina restava fuori, indicando che EGFR funge da “pass” per la sortilina in questo compartimento. Una volta lì, i complessi EGFR–sortilina sono stati trovati legati a tratti di DNA vicini ai siti di inizio di geni chiave per il controllo della crescita, inclusi cMYC e CCND1.
Un freno integrato sui geni del cancro
Per capire cosa fanno questi complessi, i ricercatori hanno mappato il loro legame in tutto il genoma e misurato i cambiamenti nellʼattività genica. Hanno scoperto che EGFR da solo tende a promuovere lʼattivazione dei geni legati alla crescita, mentre la presenza della sortilina nelle stesse regioni di DNA attenua questo effetto. Quando i livelli di sortilina venivano ridotti artificialmente, il legame di EGFR sui geni bersaglio aumentava e geni onco‑guidanti come cMYC e CCND1 diventavano più attivi. Al contrario, aumentare i livelli di sortilina aveva lʼeffetto opposto: il legame di EGFR al DNA si allentava, il reclutamento della macchina trascrizionale diminuiva e lʼespressione di questi geni oncogeni calava. In modelli murini, i tumori polmonari ingegnerizzati per sovraprodurre sortilina crescevano più lentamente e mostravano livelli ridotti di cMYC e CCND1. 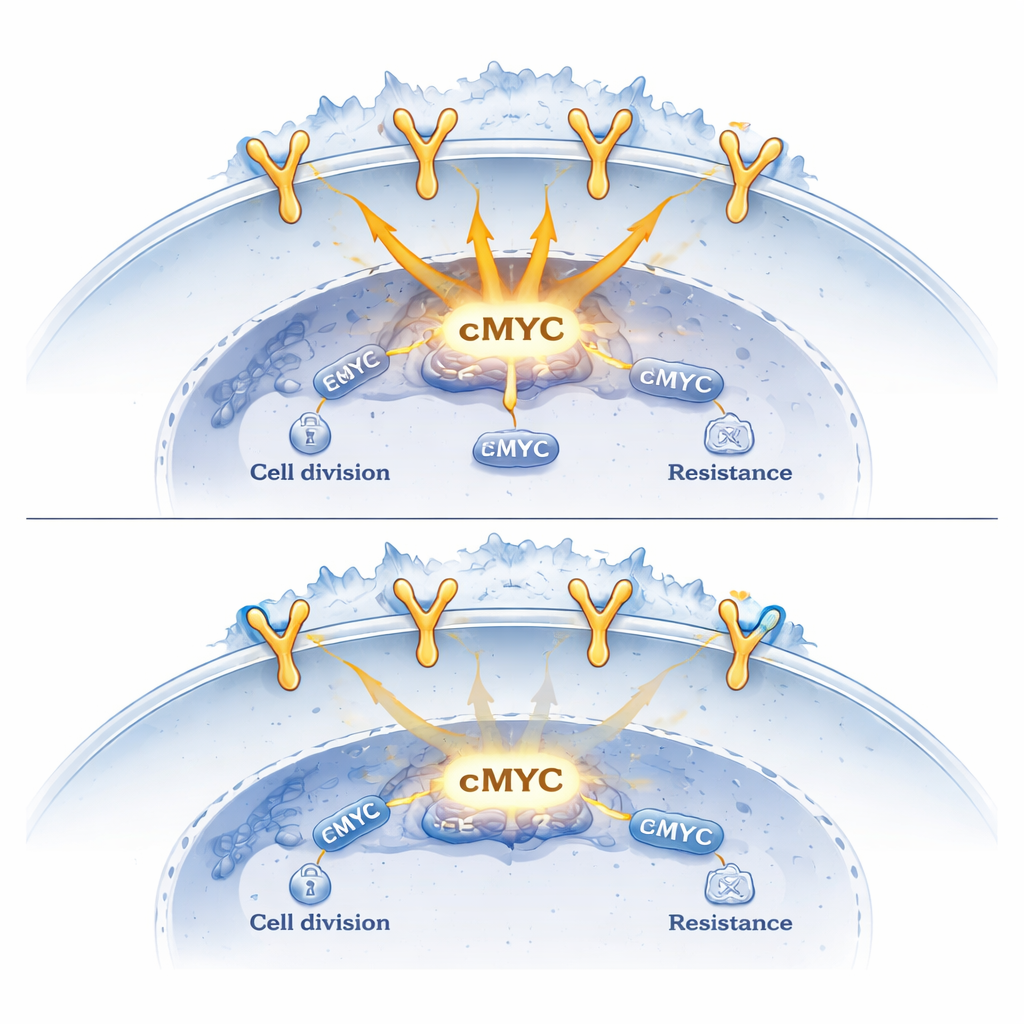
Interazione con i farmaci contro EGFR
Lo studio ha anche esplorato come questo meccanismo interagisca con osimertinib, un farmaco ampiamente usato che prende di mira EGFR e serve a bloccare le mutazioni problematiche di EGFR. Sorprendentemente, anche quando osimertinib spegneva lʼattività enzimatica di EGFR, il recettore continuava a spostarsi nel nucleo. Lì, continuava a legare il DNA, in particolare vicino al gene cMYC. La sortilina, tuttavia, si accumulava anchʼessa nel nucleo in queste condizioni. Quando la sortilina era abbondante, i livelli di cMYC diminuivano in modo più marcato in risposta a osimertinib e le cellule tumorali risultavano meno vitali. Lʼanalisi di tumori di pazienti e di grandi dataset pubblici sul cancro ha mostrato che i livelli di sortilina sono spesso più bassi negli adenocarcinomi polmonari rispetto al tessuto polmonare normale, e che unʼespressione più alta di sortilina è costantemente associata a livelli più bassi di cMYC.
Cosa significa per i pazienti
Considerati nel loro insieme, i risultati ritraggono la sortilina come una sorta di partner con funzione simile a un soppressore tumorale che accompagna EGFR nel nucleo e poi lo frena. Limitando la capacità di EGFR di attivare potenti geni della crescita come cMYC, la sortilina può rallentare la progressione tumorale e potenziare lʼeffetto dei farmaci che bloccano EGFR. Poiché molti tumori polmonari presentano livelli ridotti di sortilina, potrebbero mancare di questo freno interno, il che aiuta a spiegare perché alcuni tumori sono particolarmente aggressivi o diventano rapidamente resistenti ai farmaci. Misurare i livelli di sortilina nei tumori potrebbe aiutare a prevedere quanto bene un paziente risponderà alle terapie mirate contro EGFR, e strategie che aumentino lʼattività della sortilina potrebbero offrire un nuovo modo per mantenere sotto controllo a lungo termine i tumori guidati da EGFR.
Citazione: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
Parole chiave: cancro polmonare, EGFR, sortilina, cMYC, resistenza alle terapie mirate