Clear Sky Science · it
RO4938581, un modulatore allosterico negativo di GABAA-α5 ha risolto i fenotipi comportamentali ed EEG di un modello murino della sindrome Dup15q
Perché questa ricerca sul cervello è importante
La sindrome Dup15q è una rara condizione genetica che spesso provoca autismo, crisi epilettiche e gravi difficoltà di apprendimento. Le famiglie dispongono di poche opzioni oltre alla cura di supporto e non esiste una terapia che affronti la biologia alla radice. Questo studio ha utilizzato topi portatori dello stesso segmento di DNA in più presente nelle persone con Dup15q per indagare cosa va storto nel cervello — e per verificare se un farmaco sperimentale altamente mirato possa attenuare quel problema. Il lavoro mette in luce un tipo specifico di recettore cerebrale come un bersaglio promettente e verificabile per future terapie di precisione.
Troppo freno nel cervello
I nostri cervelli si basano su un delicato equilibrio tra segnali «vai» che eccitano i neuroni e segnali «fermati» che li smorzano. Nella sindrome Dup15q, un tratto del cromosoma 15 è duplicato. Quella regione include tre geni che costruiscono parti di un recettore chiave per il «freno» nel cervello, chiamato recettore GABAA, in particolare una versione contenente un componente denominato alfa-5. I ricercatori hanno ingegnerizzato topi con lo stesso tipo di duplicazione e hanno scoperto che questi animali producevano circa il 50% in più di recettori contenenti alfa-5 in aree cerebrali importanti per memoria, emozione e movimento, inclusi l'ippocampo e la corteccia. Metodi multipli — dall'espressione genica all'imaging dei recettori — convergono sulla stessa conclusione: questo particolare sistema di freno è sovracostruito nel modello Dup15q.
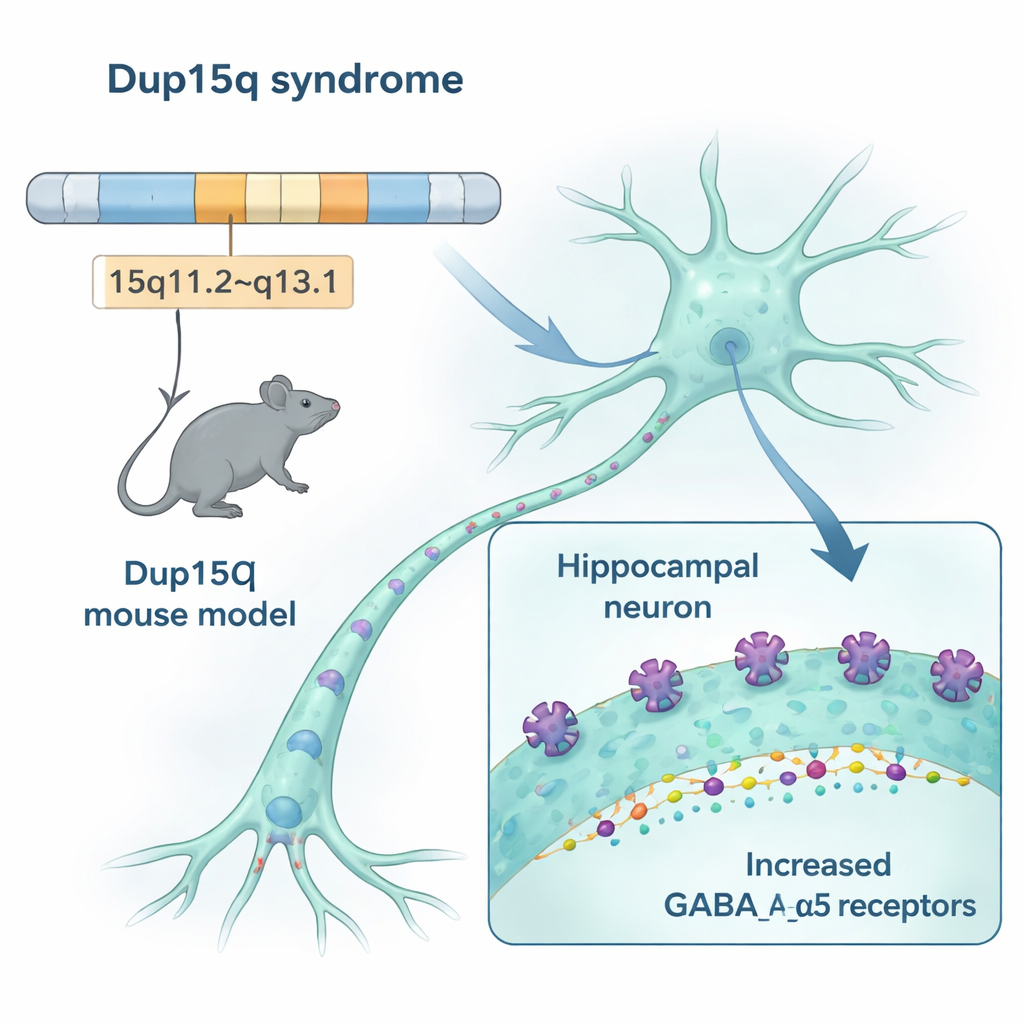
Come i recettori in eccesso modificano i segnali cerebrali
Avere più recettori frenanti è rilevante solo se cambia effettivamente il modo in cui i circuiti si attivano. in fette sottili di cervello dall'ippocampo, il team ha misurato le piccole correnti elettriche che i neuroni inibitori inviano alle altre cellule. Nei topi Dup15q, queste correnti inibitorie si verificavano più spesso, suggerendo che i neuroni subivano un freno continuo più forte, anche se l'entità di ciascun segnale individuale non era cambiata. Un test separato del comportamento dei circuiti, chiamato inibizione a doppio impulso (paired-pulse inhibition), ha mostrato anch'esso che le reti in questi topi erano più fortemente smorzate rispetto ai loro fratelli sani. Nel complesso, i dati indicano che i recettori in eccesso rendono i circuiti inibitori più dominanti, spostando l'equilibrio lontano da un'elaborazione delle informazioni flessibile.
Comportamento e onde cerebrali nei topi affetti
Gli scienziati hanno quindi verificato se questo wiring alterato si traduceva in comportamenti che richiamano i sintomi umani. In una serie di test, i topi Dup15q hanno mostrato indizi di differenze sociali e comunicative e, in modo più evidente, difficoltà nella flessibilità cognitiva. In un compito del labirinto d'acqua, sia i topi normali sia quelli Dup15q hanno imparato dove si trovava una piattaforma nascosta. Ma quando la piattaforma è stata spostata, gli animali Dup15q sono stati lenti ad abbandonare la vecchia posizione e ad adattarsi a quella nuova — un parallelo da laboratorio delle routine rigide spesso osservate nell'autismo. Il team ha anche registrato segnali elettroencefalografici (EEG), i ritmi sommati di molti neuroni. Come nelle persone con Dup15q, i topi mostravano un'attività anormalmente forte nella banda beta, un ritmo veloce spesso aumentato da farmaci che potenziano i recettori GABAA, rafforzando l'idea che il loro sistema inibitorio fosse iperattivo.
Un farmaco mirato che allenta il freno
Per vedere se potevano normalizzare questo eccesso di freno, i ricercatori si sono rivolti a RO4938581, un composto sperimentale che indebolisce selettivamente i recettori GABAA di tipo alfa-5 senza influenzare altre forme. Nelle fette ippocampali, il farmaco ha ridotto la quantità di trasferimento di carica inibitoria nei neuroni Dup15q, contrastando l'eccesso di freno. Somministrato per via orale ogni giorno per diverse settimane, lo stesso composto ha migliorato la performance degli animali nella fase di inversione del labirinto d'acqua, permettendo loro di adattarsi alla piattaforma spostata in modo più simile ai topi sani. Ha anche avvicinato le loro interazioni sociali a livelli più normali. Nelle registrazioni EEG, una dose acuta ha ridotto parzialmente la potenza beta esagerata nei topi Dup15q, spostando i loro ritmi cerebrali verso il modello tipico.
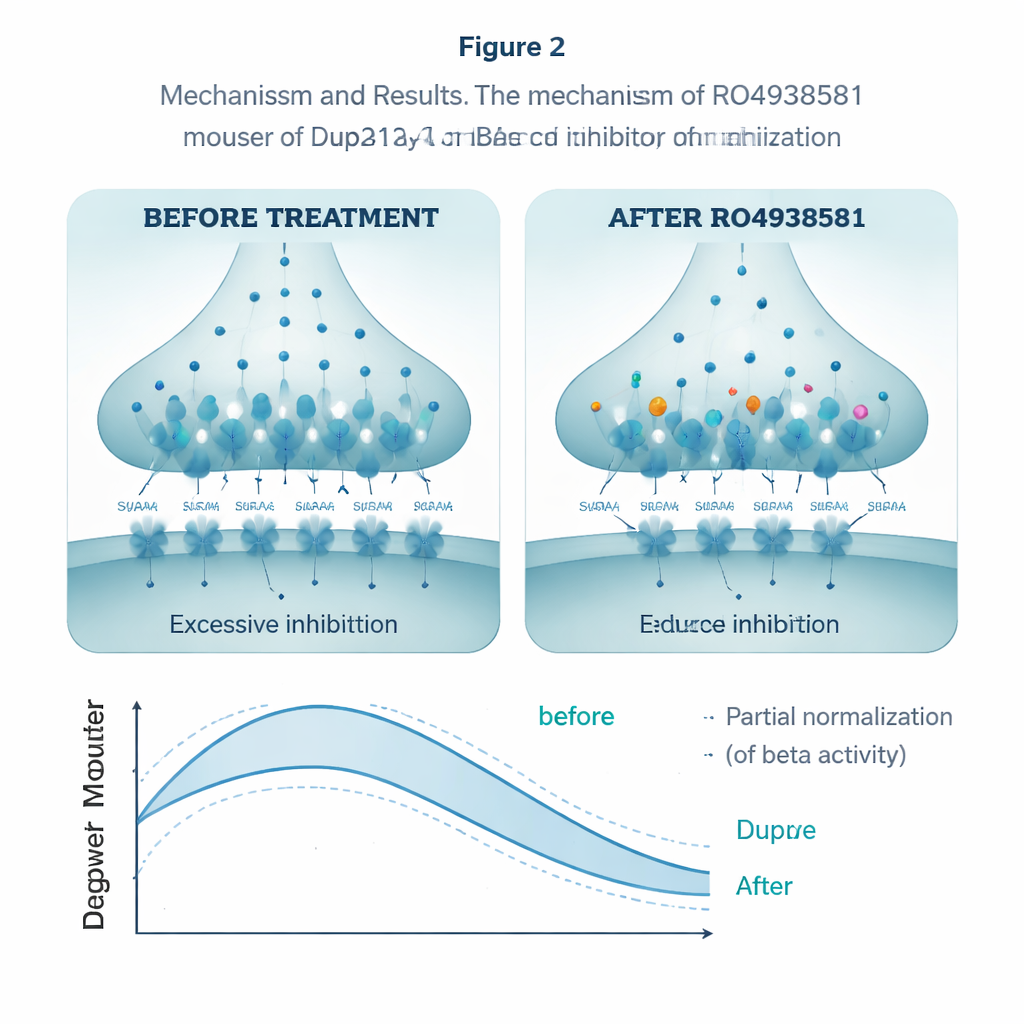
Cosa potrebbe significare per i trattamenti futuri
Per le famiglie che vivono con la sindrome Dup15q, questi risultati non rappresentano una cura immediata, ma offrono un'indicazione concreta. Il lavoro individua un particolare sottotipo di recettore — i recettori GABAA contenenti l'unità alfa-5 — sia sovraprodotto sia funzionalmente importante in un modello animale rilevante. Ridurre moderatamente questo recettore con un modulatore negativo come RO4938581 non ha risolto tutto, ma ha migliorato l'apprendimento flessibile, il comportamento sociale e una firma EEG chiave. Questa combinazione di cambiamenti a livello cerebrale, comportamentale e di biomarcatore rafforza il caso per testare farmaci più sicuri e pronti per l'uomo che colpiscano l'alfa-5 come trattamenti di precisione per Dup15q e, potenzialmente, per condizioni neuroevolutive correlate.
Citazione: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Parole chiave: sindrome Dup15q, recettore GABAA alfa-5, disturbo dello sviluppo neurologico, potenza EEG beta, modello murino