Clear Sky Science · it
Microfluidica inerziale a cascata per l’arricchimento ad alto rendimento e su più scale di cellule tumorali e aggregati intatti verso una diagnosi di malignità potenziata
Perché è importante selezionare le cellule tumorali nei fluidi
Quando il cancro si diffonde, le cellule tumorali spesso fuoriescono nei fluidi che bagnano i nostri organi. Nei pazienti con tumore polmonare questo può includere il liquido che si accumula attorno ai polmoni, chiamato versamento pleurico. Nascosti in questo fluido ci sono singole cellule tumorali rare e compatte aggregazioni di cellule. Questi aggregati sono considerati particolarmente pericolosi perché sono fortemente correlati a malattia aggressiva e a esiti peggiori. Tuttavia, i metodi di laboratorio attuali faticano a isolare in modo delicato ed efficiente sia le singole cellule sia gli aggregati da grandi volumi di fluido dei pazienti. Questo studio presenta una nuova tecnologia su chip in grado di ordinare rapidamente e con delicatezza queste cellule dal versamento pleurico, aprendo la strada a diagnosi oncologiche più affidabili e a una migliore comprensione di come i tumori si diffondono.
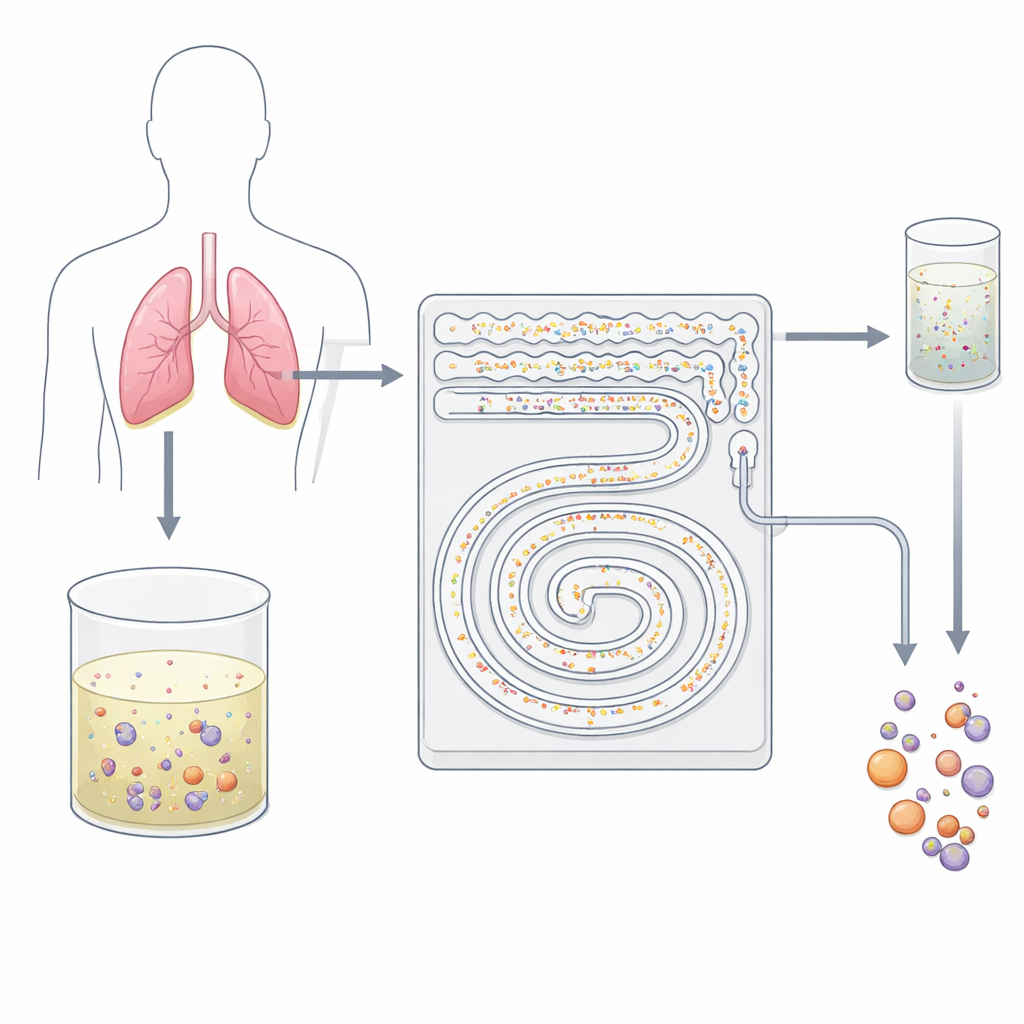
Un setaccio cellulare delicato su chip
I ricercatori hanno progettato un dispositivo delle dimensioni di un palmo, in plastica, inciso con canali minuscoli che funzionano come un filtro intelligente a due stadi. Invece di usare anticorpi adesivi o setacci aggressivi, il chip sfrutta il comportamento delle cellule in liquido ad alta velocità. Mentre il fluido scorre attraverso microcanali curvi, forze invisibili spingono particelle di dimensioni diverse in linee di flusso differenti. Il team ha sfruttato questo effetto, noto in generale come microfluidica inerziale, per separare le piccole cellule del sangue di sfondo dalle cellule tumorali più grandi e dai loro aggregati senza etichettarli o toccarli. Poiché tutto avviene in un flusso continuo e chiuso, il dispositivo può trattare decine di millilitri di fluido in pochi minuti—cosa che la citologia tradizionale su vetrino non può ottenere facilmente.
Primo stadio: sgombrare la folla
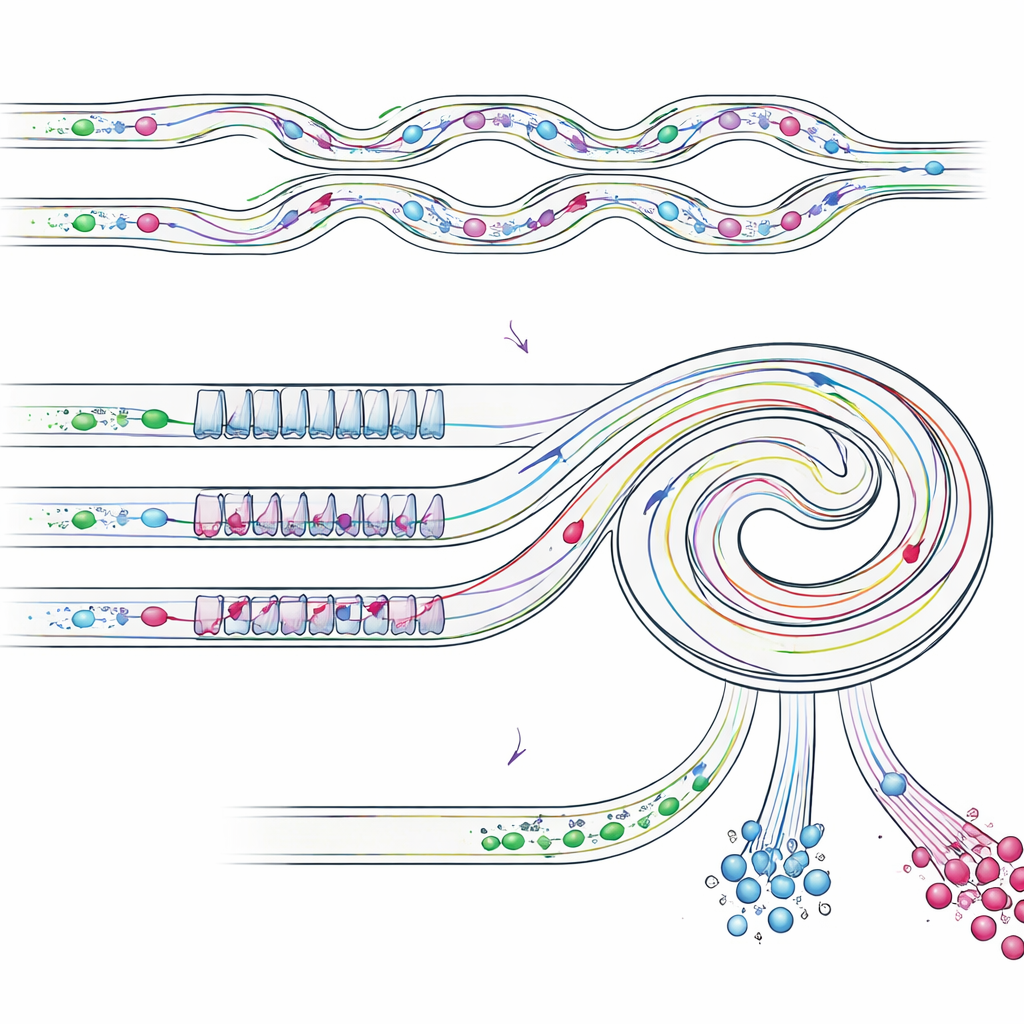
Nel primo stadio del dispositivo, il versamento pleurico—dopo aver eliminato il liquido in eccesso e aver riossospeso le cellule—viene fatto scorrere attraverso una rete di canali serpentina paralleli. Qui, il flusso curvo genera vortici che spingono le piccole cellule bianche verso le pareti del canale, mentre le cellule tumorali più grandi e gli aggregati restano vicino al centro dello stream. Le piccole cellule vengono indirizzate verso uscite di scarto, diluendo drasticamente il fondo. Questo stadio ad alto rendimento può operare a circa 8 millilitri al minuto, il che significa che un tipico campione clinico da 50 millilitri può essere processato in circa sei minuti e mezzo senza intasarsi. Ciò che esce da questo primo stadio è una miscela molto più pulita, arricchita in cellule potenzialmente maligne e pronta per una separazione più fine.
Secondo stadio: separare singole cellule e aggregati
Il campione parzialmente arricchito entra poi in un canale a spirale inclinata che include un pattern ripetuto di sezioni strette e larghe. In questo stadio, diverse forze di flusso si bilanciano in modo differente per oggetti di dimensioni diverse, convogliandoli in corsie distinte vicino alla parete interna o esterna della spirale. Le singole cellule di tipo tumorale, più piccole, si allineano in una posizione laterale, mentre gli aggregati più voluminosi migrano verso una posizione diversa, più vicina alla parete interna. Posizionando uscite nei punti giusti, il chip divide fisicamente questi stream: un’uscita raccoglie principalmente cellule tumorali singole, un’altra raccoglie aggregati intatti, e altre uscite rimuovono le rimanenti piccole cellule. È importante che gli aggregati restino integri, evitando il danneggiamento e la frammentazione spesso osservati con i metodi di filtrazione tradizionali.
Mettere il dispositivo alla prova
Per verificare l’efficacia del loro progetto, il team ha prima usato sfere di plastica di dimensioni note per mimare cellule del sangue, singole cellule tumorali e aggregati. Hanno dimostrato che il chip a cascata recuperava più dell’87% delle sfere “a singola cellula” e circa il 92% delle sfere “aggregato”, rimuovendo nel contempo la maggior parte delle sfere più piccole rappresentanti le “cellule del sangue”. Successivamente hanno testato cellule reali di cancro polmonare (cellule A549) miscelate con globuli bianchi. In questi test, il dispositivo ha recuperato circa l’82% delle cellule tumorali complessive, con una purezza di circa il 76% nella frazione arricchita e quasi l’80% di purezza per gli aggregati cellulari. Infine hanno processato campioni reali di versamento pleurico provenienti da tre pazienti con cancro polmonare. Partendo da fluidi in cui cellule tumorali e aggregati rappresentavano meno dell’1% di tutte le cellule, il chip ha prodotto frazioni in cui le singole cellule maligne raggiungevano circa il 68% del totale cellulare, e gli aggregati costituivano circa il 35% delle cellule in uno stream dedicato di uscita.
Cosa potrebbe significare per i pazienti
Usando solo il flusso del liquido e la geometria dei canali, questo dispositivo può rapidamente e con delicatezza estrarre sia le singole cellule tumorali sia gli aggregati intatti da grandi volumi di fluido del paziente senza etichette chimiche o strumenti complessi. Le cellule arricchite rimangono adatte a test standard come colorazioni immunofluorescenti e microscopia, integrandosi agevolmente nei flussi di lavoro ospedalieri esistenti. Sebbene lo studio attuale abbia coinvolto un numero limitato di pazienti e richieda trial più ampi per dimostrare il suo impatto su diagnosi e prognosi, il lavoro dimostra un concetto potente: un “concentratore cellulare” veloce e senza etichetta che rivela sia il numero sia lo stato di aggregazione delle cellule tumorali nei versamenti pleurici. A lungo termine, strumenti di questo tipo potrebbero affinare la valutazione della malignità, guidare scelte terapeutiche personalizzate e offrire una finestra più chiara su come i tumori metastatizzano.
Citazione: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Parole chiave: biopsia liquida, separazione cellulare microfluidica, aggregati di cellule tumorali, versamento pleurico, diagnosi del cancro