Clear Sky Science · it
Progettazione di un sistema automatizzato di microiniezione a lotti per cellule basato su pinzette magnetiche per embrioni di zebrafish
Perché le piccole uova di pesce contano
Prima che nuovi farmaci o terapie geniche arrivino alle persone, gli scienziati li testano spesso su animali piccoli e a crescita rapida. Gli embrioni di zebrafish sono molto usati perché sono trasparenti e si sviluppano velocemente, permettendo ai ricercatori di osservare la formazione degli organi in tempo reale. Per modificare i loro geni o somministrare farmaci, però, è necessario iniettare ogni delicata uova con un ago microscopico, un compito che di solito è lento, faticoso e fortemente dipendente dall’abilità umana. Questo articolo presenta un nuovo sistema robotico che può iniettare automaticamente lotti di embrioni di zebrafish più velocemente, con maggiore delicatezza e affidabilità rispetto a un operatore umano, aprendo la strada a esperimenti più ampi e più coerenti.
Un nuovo modo di gestire cellule fragili
La microiniezione tradizionale richiede un operatore esperto per guidare un ago di vetro al microscopio, individuare ogni embrione, ruotarlo nella giusta orientazione e penetrarlo senza danneggiare strutture vitali. Questo è particolarmente complicato perché gli embrioni sono sfere morbide con regioni importanti da evitare per mantenerli in vita. I sistemi robotici esistenti hanno aiutato ad automatizzare il trasporto e la perforazione, ma di solito non riescono a controllare la rotazione di ogni embrione nelle tre dimensioni. Di conseguenza, l’ago può entrare con un angolo rischioso, riducendo i tassi di sopravvivenza e limitando il numero di embrioni che si possono elaborare in modo affidabile. Il team dietro questo studio si è posto l’obiettivo di costruire una piattaforma completamente integrata che possa trasportare, ruotare, iniettare e rilasciare gli embrioni in una sequenza fluida, senza continui cambi di lente o aggiustamenti manuali.
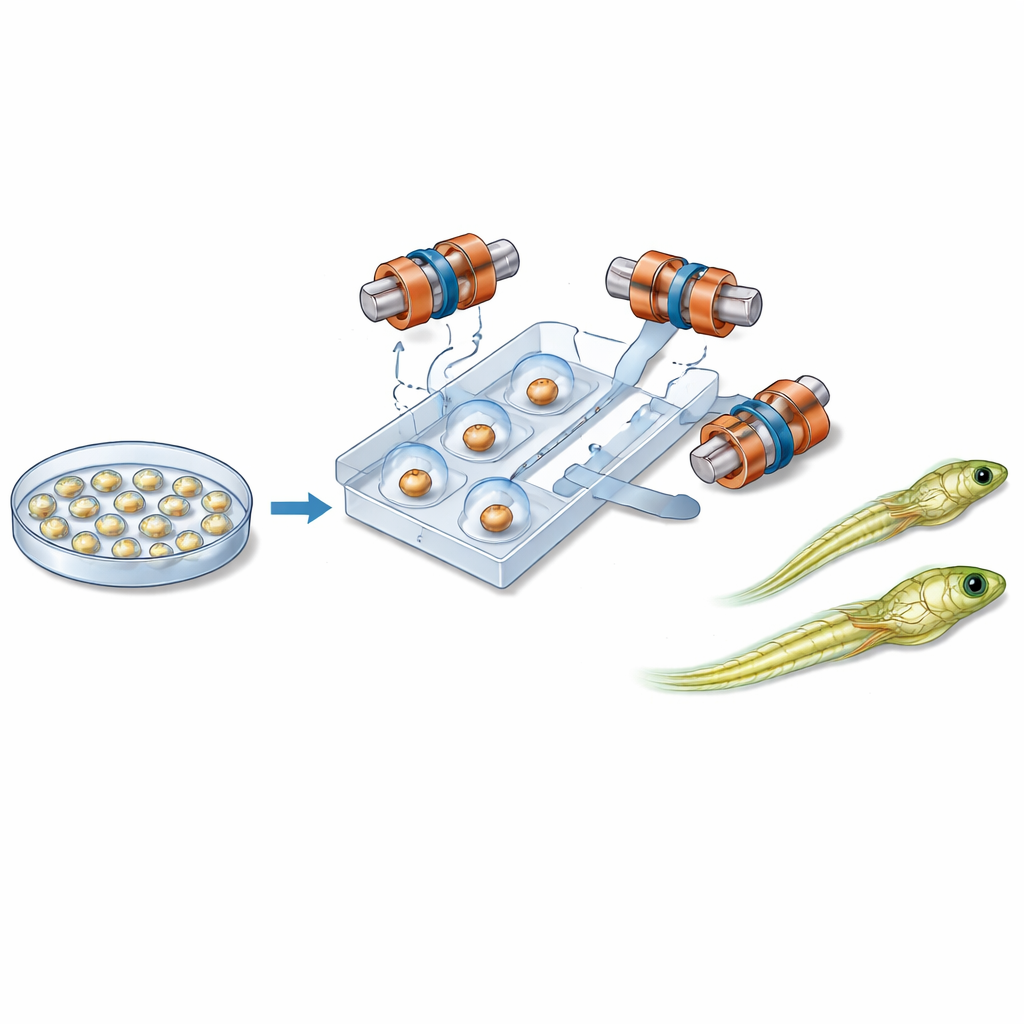
Magneti, microcanali e controllo delicato
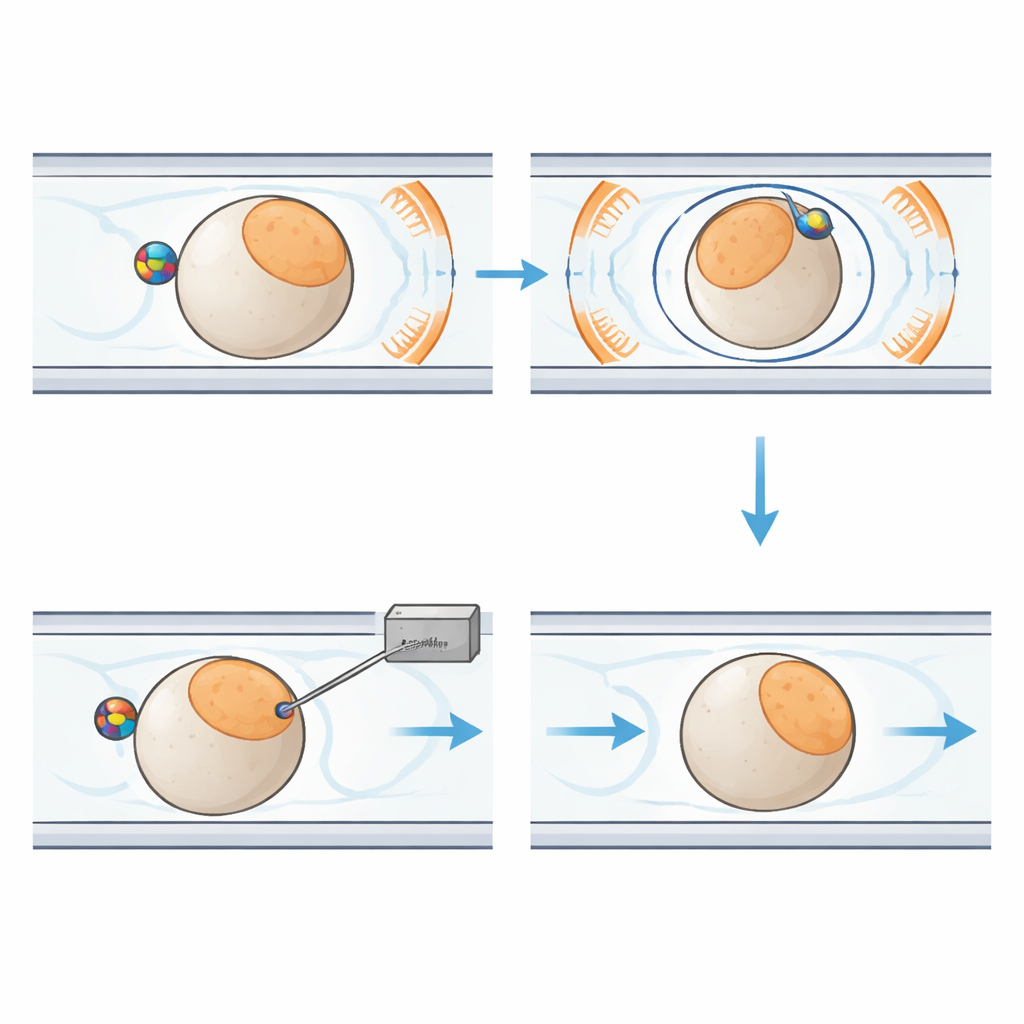
Al centro del nuovo sistema c’è una piastrina di plastica grande quanto il palmo contenente canali stretti che guidano gli embrioni individuali lungo un percorso fisso. Vicino a ciascun embrione si trova una piccola sfera magnetica. Intorno alla piastrina, sei bobine disposte con cura generano un campo magnetico uniforme nelle tre dimensioni. Modificando nel tempo la direzione di questo campo, il sistema fa ruotare la sfera. Grazie all’attrito tra la sfera e la superficie dell’embrione, l’intera cellula si muove con essa, come due ingranaggi ingranati. Ciò consente al robot di inclinare l’embrione fuori dal piano di imaging o di farlo ruotare nel piano finché la regione sensibile non è posizionata in modo sicuro lontano dall’ago in arrivo. Liquidi e leggere pressioni d’aria muovono e mantengono gli embrioni in posizione, mentre un modulo separato controlla l’ago di iniezione e il flusso minore del materiale genetico.
Vedere chiaramente in un campo visivo minuscolo
Per rendere possibile questa coreografia precisa, i ricercatori hanno anche progettato un avanzato sistema di visione artificiale, chiamato microscopic manipulation perception network. Analizza le immagini dalla camera del microscopio in tempo reale per individuare ogni embrione, rilevare la punta sottile dell’ago e distinguere i due “poli” opposti dell’uovo dove si trovano le strutture chiave dello sviluppo. La rete utilizza tecniche moderne di deep learning — come percorsi doppi di estrazione delle caratteristiche, moduli di attenzione che evidenziano dettagli importanti e fusione multiscala delle informazioni d’immagine — per gestire il mondo affollato e scarsamente illuminato all’interno di una chip microfluidica. Nei test su migliaia di immagini, ha rilevato correttamente gli oggetti e segmentato le regioni dell’embrione con un’accuratezza di circa il 98–99%, fornendo il feedback affidabile necessario per guidare sia la rotazione magnetica sia il posizionamento dell’ago.
Dimostrare che funziona su zebrafish vivi
Il team ha confrontato il loro sistema automatizzato con operatori umani esperti usando 100 embrioni di zebrafish ciascuno. Il robot ha completato le iniezioni in circa 33,8 secondi per embrione, più del doppio della velocità del lavoro manuale, e ha perforato con successo ogni cellula. Ha anche orientato ogni embrione con un errore angolare medio di appena 2,1 gradi, circa la metà dell’errore degli operatori umani. Ancora più importante, l’88% degli embrioni iniettati dal robot è sopravvissuto fino all’eclosione come larve, rispetto al 66% dopo iniezione manuale. Al microscopio a fluorescenza, le larve provenienti dal sistema automatizzato emanavano una compatta fluorescenza verde, mostrando che il materiale genetico introdotto era stato acquisito ed espresso come previsto. Ruotando gli embrioni magneticamente invece di comprimerli con strumenti meccanici, il sistema ha minimizzato deformazioni e danni mantenendo un’elevata produttività.
Cosa significa per studi futuri
In termini semplici, questo lavoro dimostra che una combinazione ben ingegnerizzata di microcanali, controllo magnetico e analisi intelligente delle immagini può iniettare embrioni di pesce fragili più rapidamente e con maggiore sopravvivenza rispetto a un operatore esperto che usa strumenti tradizionali. Poiché il zebrafish è una piattaforma chiave per studiare lo sviluppo, le malattie e gli effetti dei farmaci, un iniettore affidabile ad alto rendimento potrebbe accelerare grandi screening genetici e studi biologici a lungo termine che in passato erano limitati dal lavoro manuale. Con opportune modifiche al design della piastrina e alle impostazioni di controllo, la stessa strategia potrebbe essere adattata ad altri tipi di cellule e piccoli organismi, contribuendo a trasformare la chirurgia cellulare delicata da un’arte praticata da pochi specialisti in un processo automatizzato e standardizzato.
Citazione: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Parole chiave: embrioni di zebrafish, microiniezione, pinzette magnetiche, microfluidica, manipolazione robotica delle cellule