Clear Sky Science · it
Fogli ibridi nanoscalari di WS2 drogati con Cu e PEGilati per una terapia multimodale mirata del cancro
Perché contano terapie oncologiche più intelligenti
Molte persone con cancro al seno affrontano ancora trattamenti pesanti che possono danneggiare i tessuti sani senza eliminare completamente il tumore. Questo studio descrive un nuovo tipo di sottilissimo foglio ingegnerizzato, troppo piccolo per essere visto a occhio nudo, progettato per viaggiare nell’organismo, localizzare i tumori mammari e attaccarli in più modi coordinati contemporaneamente. Combinando calore, chimica e un farmaco chemioterapico classico in un unico pacchetto mirato, i ricercatori mirano a rendere la terapia sia più efficace sia meno dannosa per il resto del corpo. 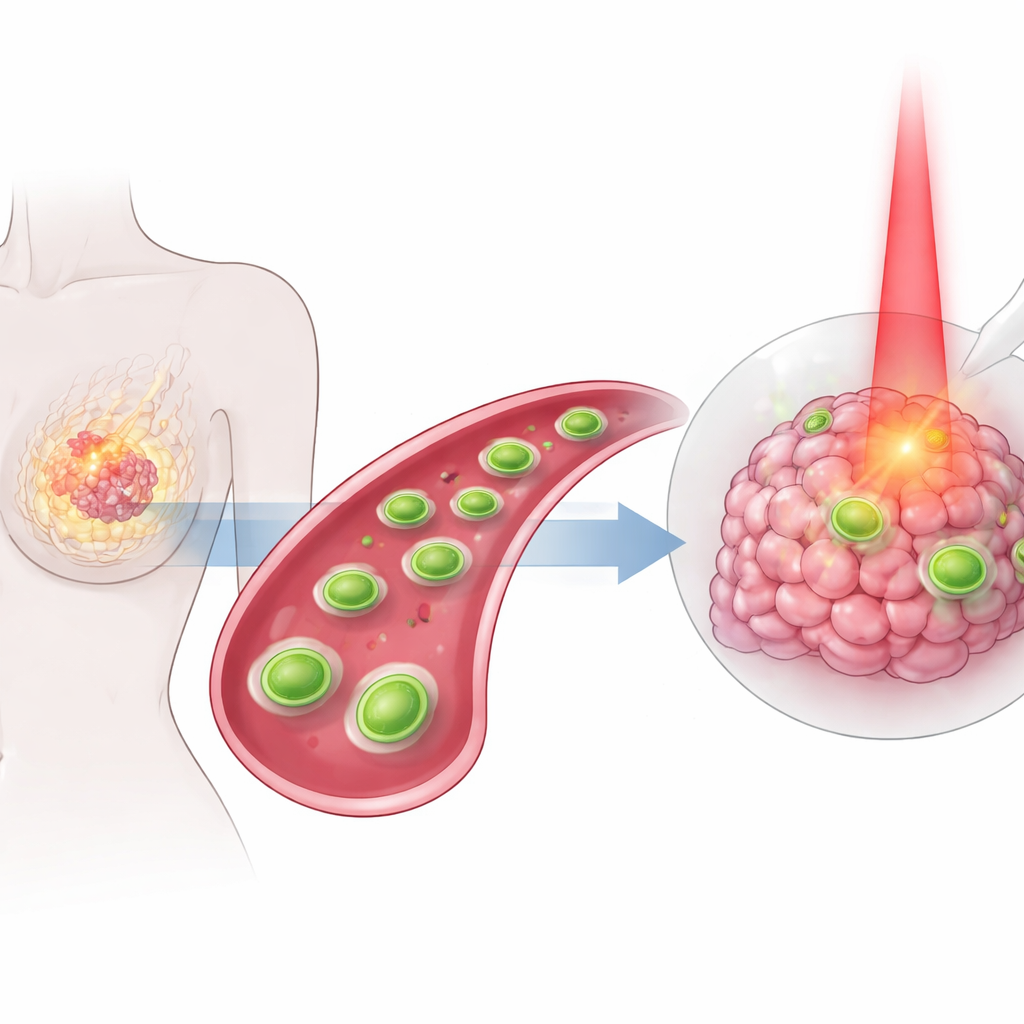
Fogli minuscoli progettati per trasportare e somministrare il trattamento
Il cuore dell’approccio è un materiale ultrafine a base di tungsteno e zolfo, modellato in fogli nanoscalari. Questi fogli assorbono naturalmente la luce nel vicino infrarosso e la trasformano in calore. Il gruppo ha prima sintetizzato questi fogli e poi ne ha irruvidito attentamente la superficie in modo da poter ospitare altri componenti utili. Atomi di rame sono stati ancorati in modo altamente disperso sui fogli e è stato aggiunto un rivestimento morbido e flessibile simile a un “impermeabile” molecolare per favorire la dispersione nei fluidi corporei e prevenire l’aggregazione. Infine è stata collegata l’acido folico — una vitamina che molte cellule tumorali assorbono avidamente — come dispositivo di richiamo, e il comune chemioterapico doxorubicina è stato caricato sulla superficie. Il risultato finale è una piattaforma minuscola e stratificata che può circolare nel sangue, riconoscere le cellule tumorali e portare un carico consistente di terapia.
Come luce, chimica e farmaco lavorano insieme
Una volta che queste particelle raggiungono il tumore, avvengono più processi in concerto. Quando l’area tumorale viene illuminata con un laser rosso delicato, i fogli di tungsteno‑zolfo si riscaldano in modo efficiente, aumentando la temperatura locale quanto basta per stressare e danneggiare le cellule tumorali senza surriscaldare il resto del corpo. Contemporaneamente, gli atomi di rame sui fogli reagiscono con le molecole di perossido naturalmente presenti a livelli più elevati all’interno dei tumori. Questa reazione trasforma il perossido in ossidanti molto reattivi e di breve durata che danneggiano componenti cellulari dall’interno. I tumori tendono inoltre ad essere leggermente più acidi dei tessuti sani; in questo ambiente più acido, e sotto il riscaldamento indotto dal laser, il legame tra il foglio e la doxorubicina si indebolisce, permettendo il rilascio di una maggiore quantità di farmaco proprio dove è necessario. Questi tre effetti — calore, attacco chimico e chemioterapia mirata — sono progettati per potenziarsi a vicenda. 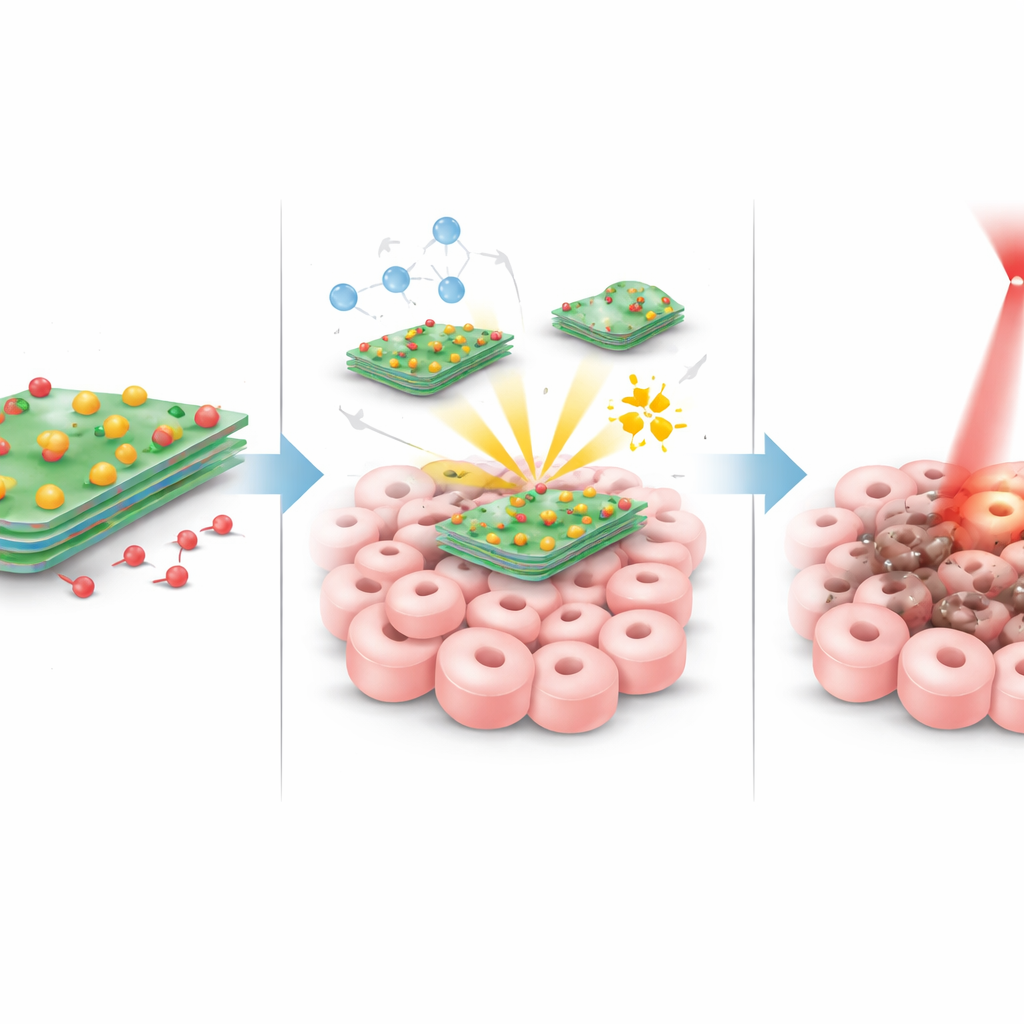
Prove da cellule e modelli murini portatori di tumore
In colture cellulari, i fogli rivestiti da soli hanno mostrato scarsi effetti dannosi sulle cellule normali, suggerendo una buona sicurezza di base. Ma quando caricati con doxorubicina ed esposti al laser in presenza di perossido, hanno indotto una forte morte delle cellule di carcinoma mammario, molto più pronunciata rispetto a qualsiasi singolo trattamento. I ricercatori hanno inoltre dimostrato che le particelle generano un’ondata di ossidanti reattivi all’interno delle cellule tumorali, confermando l’attività della chimica del rame. Nei topi portatori di tumori mammari, le particelle con il rivestimento a base di acido folico si sono accumulate molto più intensamente e per periodi più lunghi nel tessuto tumorale rispetto alle particelle non mirate. Quando i topi hanno ricevuto la combinazione completa — particelle mirate più esposizione alla luce rossa — i loro tumori si sono ridotti drasticamente, la sopravvivenza è aumentata e il peso corporeo e la salute degli organi sono rimasti in gran parte normali, indicando effetti collaterali limitati rispetto al trattamento farmacologico standard.
Cosa potrebbe significare per la cura del cancro in futuro
Nel complesso, i risultati suggeriscono che questi fogli ingegnerizzati funzionano come un coltellino svizzero per il trattamento del cancro: cercano i tumori, li riscaldano, li avvelenano dall’interno tramite reazioni chimiche reattive e rilasciano un farmaco consolidato in modo più preciso, il tutto risparmiando gran parte del resto dell’organismo. Il lavoro è ancora a livello di studi su animali e restano questioni importanti sulla sicurezza a lungo termine, sul degrado e su come produrre al meglio tali particelle per uso umano. Tuttavia, il progetto mostra come combinare più interventi moderati in un unico pacchetto intelligente, tarato sull’ambiente tumorale, possa produrre un effetto complessivo molto più potente. Se studi futuri ne confermeranno sicurezza ed efficacia, tali nanoplatform multifunzionali potrebbero contribuire a rendere la terapia del cancro al seno più mirata, più efficiente e meno gravosa per i pazienti.
Citazione: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Parole chiave: terapia del cancro al seno, nanomedicina, trattamento fototermico, consegna mirata del farmaco, terapia chemodinamica