Clear Sky Science · it
Dispositivo microfluidico monostrato a produzione rapida e costo ridotto per un focalizzazione idrodinamica tridimensionale ad alto rendimento
Perché ridurre i flussi microscopici è importante
La medicina moderna dipende sempre più dall’osservare una grande quantità di singole cellule, una per una, per esempio per individuare cellule tumorali nelle urine o nel sangue. Per farlo in modo rapido ed economico, le cellule vengono spesso convogliate attraverso canali sottilissimi su microchip, dove laser o telecamere le ispezionano. Ma per ottenere immagini nitide e affidabili a velocità estreme, ogni cellula deve passare quasi esattamente nello stesso punto microscopico. Questo articolo presenta un nuovo modo di costruire tali chip in modo che possano convogliare strettamente le cellule in un fluido tridimensionale sottile, anche a velocità molto elevate, usando un dispositivo più rapido e meno costoso da realizzare rispetto ai sistemi standard attuali.
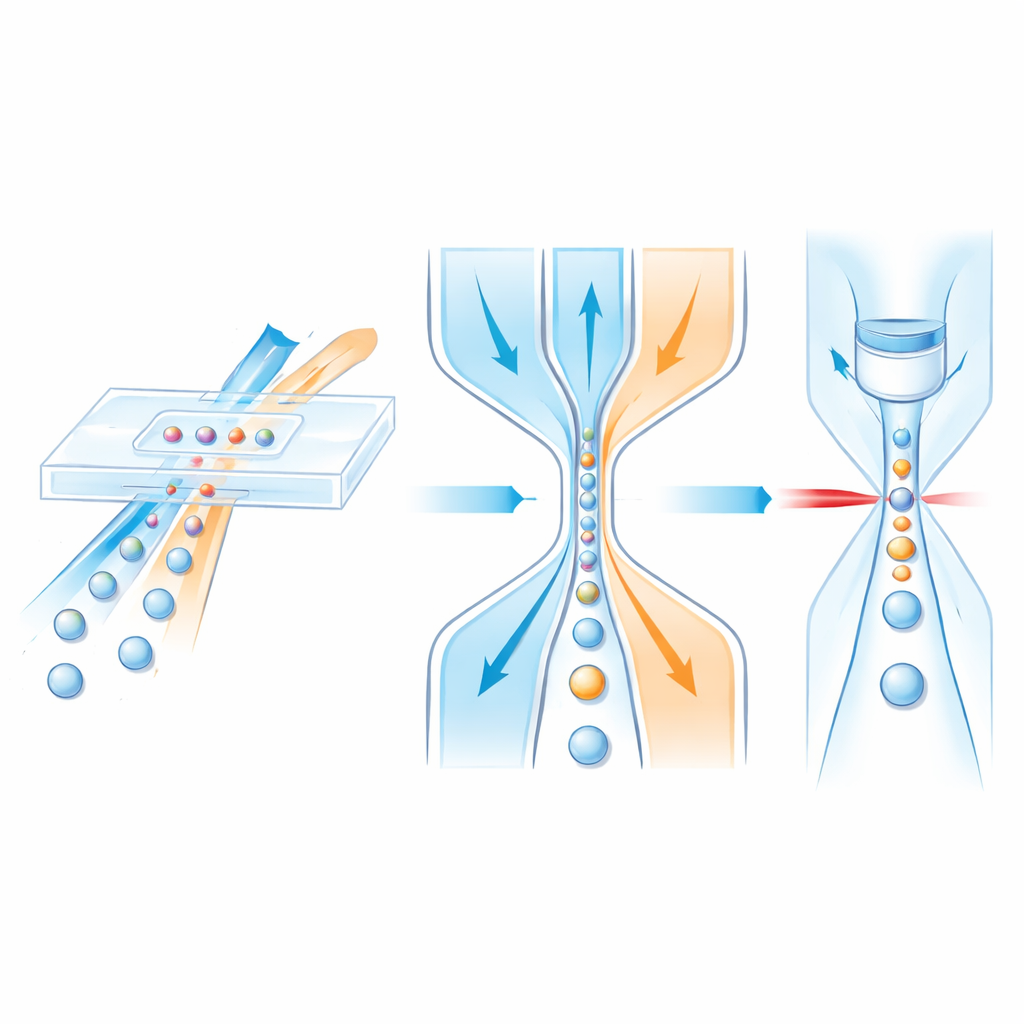
Guidare le cellule con “corsie” fluide
All’interno di un chip microfluidico, le cellule viaggiano in un flusso centrale di liquido mentre fluidi «mantello» circostanti fungono da protezioni invisibili, spingendo delicatamente il campione verso il centro. I progetti precedenti potevano solitamente focalizzare le cellule solo lateralmente, non in altezza, oppure si affidavano a strutture complesse a più strati che sono lente e costose da produrre. Gli autori invece progettano un canale monostrato che ottiene comunque il controllo tridimensionale completo. Innanzitutto il campione si unisce a un flusso mantello verticale in una giunzione a T angolata che si restringe lungo la sua lunghezza. A causa della forma del canale e dell’inerzia dei liquidi a velocità più elevate, il flusso del campione viene spinto verso la metà superiore del canale. Successivamente, due mantelli laterali corrispondenti più a valle comprimono ulteriormente da sinistra e da destra, pizzicando il campione già sollevato in un sottile filamento centrale che attraversa una finestra di rilevamento.
Costruire chip migliori in minuti, non ore
La maggior parte dei chip microfluidici di ricerca oggi sono realizzati in silicone morbido (PDMS) mediante soft lithography, un processo che richiede molteplici passaggi di riscaldamento e polimerizzazione e può richiedere un’ora o più per dispositivo. Il PDMS è facile da modellare ma si deforma sotto alta pressione, facendo rigonfiare i canali e disperdere il flusso focalizzato. Il nuovo dispositivo utilizza una plastica rigida chiamata acrilato di poliuretano (PUA), sagomata tramite un processo di «doppio trasferimento». Prima si ottiene uno stampo riutilizzabile in PDMS con rilievi delle caratteristiche dei canali colato a partire da un master in silicio. Il PUA liquido viene quindi versato nello stampo, polimerizzato con luce ultravioletta e scollato per formare lo strato dei canali. Un vetrino separato rivestito di PUA serve come base. Le due superfici in PUA vengono allineate, pressate insieme e legate con un’altra breve esposizione ai raggi UV. Poiché ogni fase di polimerizzazione richiede solo secondi e non è necessaria una lunga cottura, un chip completo può essere prodotto in circa cinque minuti, all’incirca dieci volte più velocemente rispetto ai metodi tradizionali.
Testare il flusso e domare la deformazione
Per comprendere quanto bene funzioni il progetto, il team combina simulazioni al computer con esperimenti. Prima simulano come la variazione delle portate dei flussi di campione e mantello influenzi la forma del nucleo focalizzato. I risultati mostrano che aumentare sia i flussi mantello verticali sia quelli laterali aiuta a ridurre l’altezza e la larghezza del campione, e che velocità complessive più elevate (numero di Reynolds maggiore) migliorano ulteriormente la focalizzazione. Simulano poi come si deformano le pareti dei canali quando sono realizzate in PDMS morbido rispetto al PUA rigido. In condizioni realistiche ad alta velocità, le pareti in PDMS si gonfiano di oltre centinaia di micrometri, quanto basta a deformare il flusso così gravemente che il campione si divide e devia verso gli angoli. Al contrario, il PUA si deforma di meno di cento nanometri—effectivamente rigido a questa scala—così il flusso focalizzato rimane centrato e compatto anche ad alta pressione.
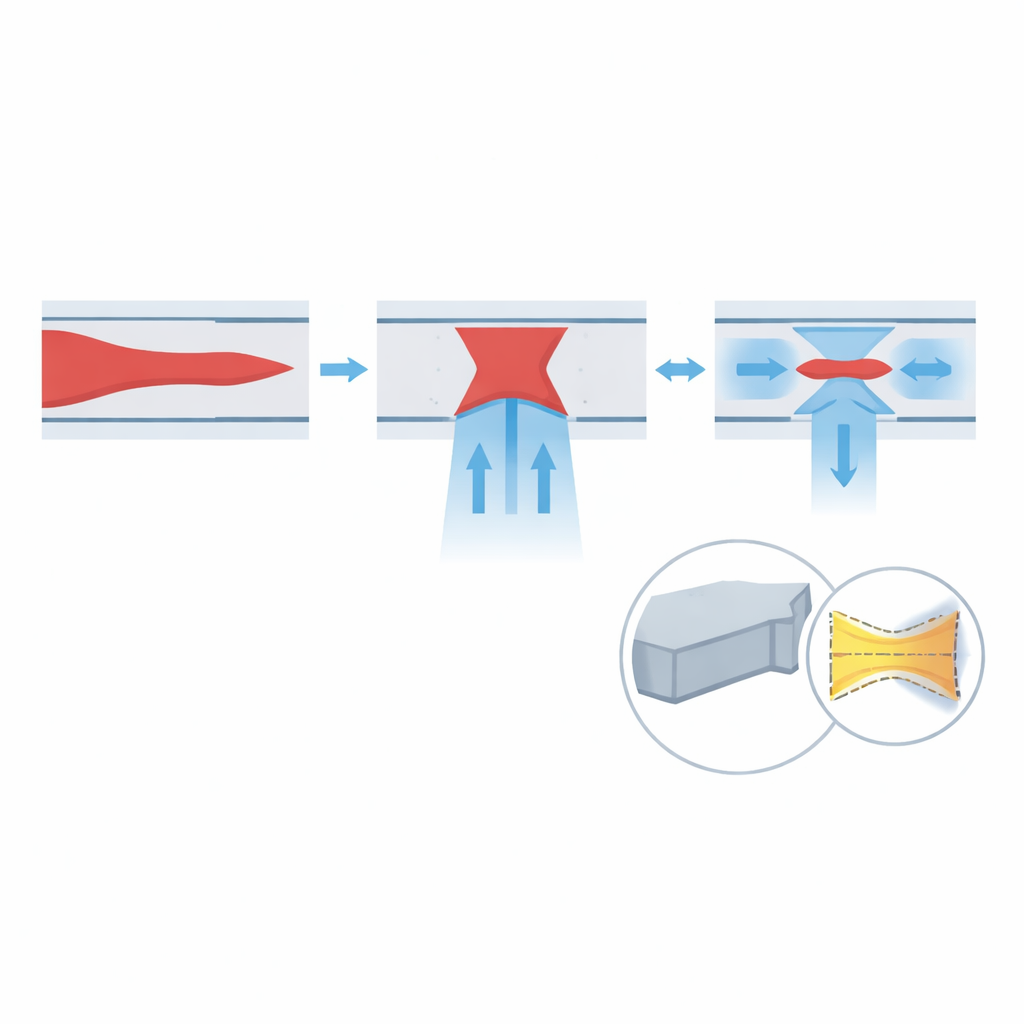
Osservare cellule reali a velocità estreme
Oltre ai test con coloranti, gli autori valutano il dispositivo usando la microscopia ottica time-stretch (OTS), una tecnica che converte impulsi laser ultraveloci in rapide scansioni lineari, consentendo milioni di linee immagine al secondo. Inviano campioni di urine trattate di pazienti con tumore alla vescica attraverso il chip a portate crescenti, mentre l’OTS registra immagini bidimensionali di ogni cellula che passa. Poiché il sistema ottico ha una regione focale molto sottile, qualsiasi cellula che si discosti in verticale appare sfocata, fornendo una misura diretta della focalizzazione verticale. A velocità comprese tra 3,3 e 16,7 metri al secondo, la frazione di immagini ben focalizzate aumenta, raggiungendo il 98,4% alla massima velocità testata. La focalizzazione laterale viene valutata misurando quanto i centri delle cellule deviano dal punto medio del canale; questo scostamento diminuisce con la velocità, corrispondendo a circa il 95,0% di efficienza di focalizzazione laterale a 16,7 metri al secondo.
Cosa significa per l’analisi cellulare futura
In termini semplici, i ricercatori dimostrano che un chip plastico monostrato, semplice da realizzare, può condurre in modo affidabile le cellule in un flusso stretto e ben controllato in tutte le direzioni, anche alle condizioni esigenti richieste per l’imaging ultraveloce. Accoppiando un materiale resistente alla deformazione con un intelligente schema di flussi mantello, evitano i limiti meccanici dei dispositivi in silicone morbido riducendo drasticamente i tempi di fabbricazione. Questo rende più semplice produrre molti chip identici per uso clinico e industriale e condurre test su larga scala ad alto rendimento su campioni di pazienti reali. Di conseguenza, la tecnologia offre una strada pratica verso strumenti di screening cellulare più rapidi e precisi che potrebbero avvantaggiare la diagnostica, il monitoraggio del cancro e altre applicazioni che dipendono dall’esaminare da vicino un gran numero di singole cellule.
Citazione: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Parole chiave: citoscopia a flusso microfluidica, focalizzazione idrodinamica 3D, analisi cellulare ad alto rendimento su singola cellula, chip microfluidici in acrilato di poliuretano, microscopia ottica time-stretch