Clear Sky Science · it
Sistema robotico per il trasporto cellulare basato sulla modellazione della resistenza del micropipetta
Spostare cellule minuscole senza un microscopio
La biologia moderna spesso dipende da un compito sorprendentemente semplice: raccogliere una singola cellula con un tubicino di vetro e posarla altrove. Questo è essenziale per i trattamenti di fertilità, il congelamento degli embrioni, le terapie a base di cellule e la ricerca di base. Tuttavia oggi quasi sempre richiede un ingombrante microscopio e un operatore altamente qualificato che osservi ogni mossa. Questo articolo descrive un nuovo sistema robotico in grado di trasferire singole cellule tra gocce di liquido senza alcuna visione microscopica, aprendo la strada a “fabbriche di cellule” completamente chiuse e automatizzate che possono lavorare più velocemente, a costi inferiori e con meno danni per le cellule delicate.
Perché il trasferimento cellulare ha bisogno di una revisione
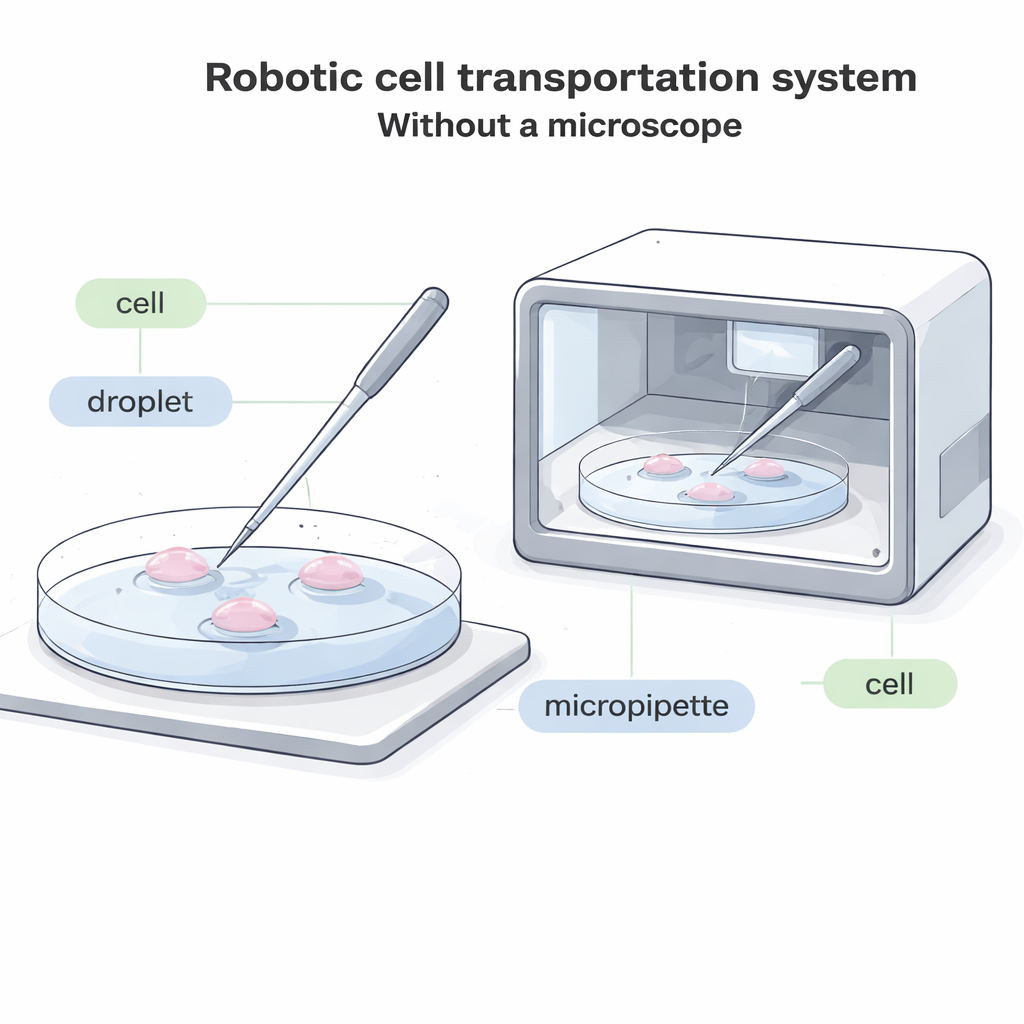
Nei laboratori attuali, un operatore guarda attraverso un microscopio e usa un sottile tubicino di vetro, chiamato micropipetta, per appoggiare la punta sul fondo di una piastra, aspirare delicatamente una cellula, spostarla in una nuova goccia di fluido e quindi espellerla. Questo processo è lento, richiede grande concentrazione visiva ed è difficile da automatizzare. In molti sistemi futuri — come dispositivi compatti e sigillati che coltivano embrioni o altre cellule all’interno di una scatola — semplicemente non c’è spazio per un microscopio tradizionale. In altri casi, le cellule sono marcate con coloranti fluorescenti che possono sbiadire o essere danneggiati dalla luce, quindi minimizzare l’osservazione microscopica intensa è importante. I sistemi “ciechi” esistenti, che non si basano su immagini, funzionano solo con cellule insolitamente grandi, lasciando la maggior parte dei tipi cellulari comuni senza una buona soluzione automatizzata.
Una cannuccia speciale con un fermo incorporato
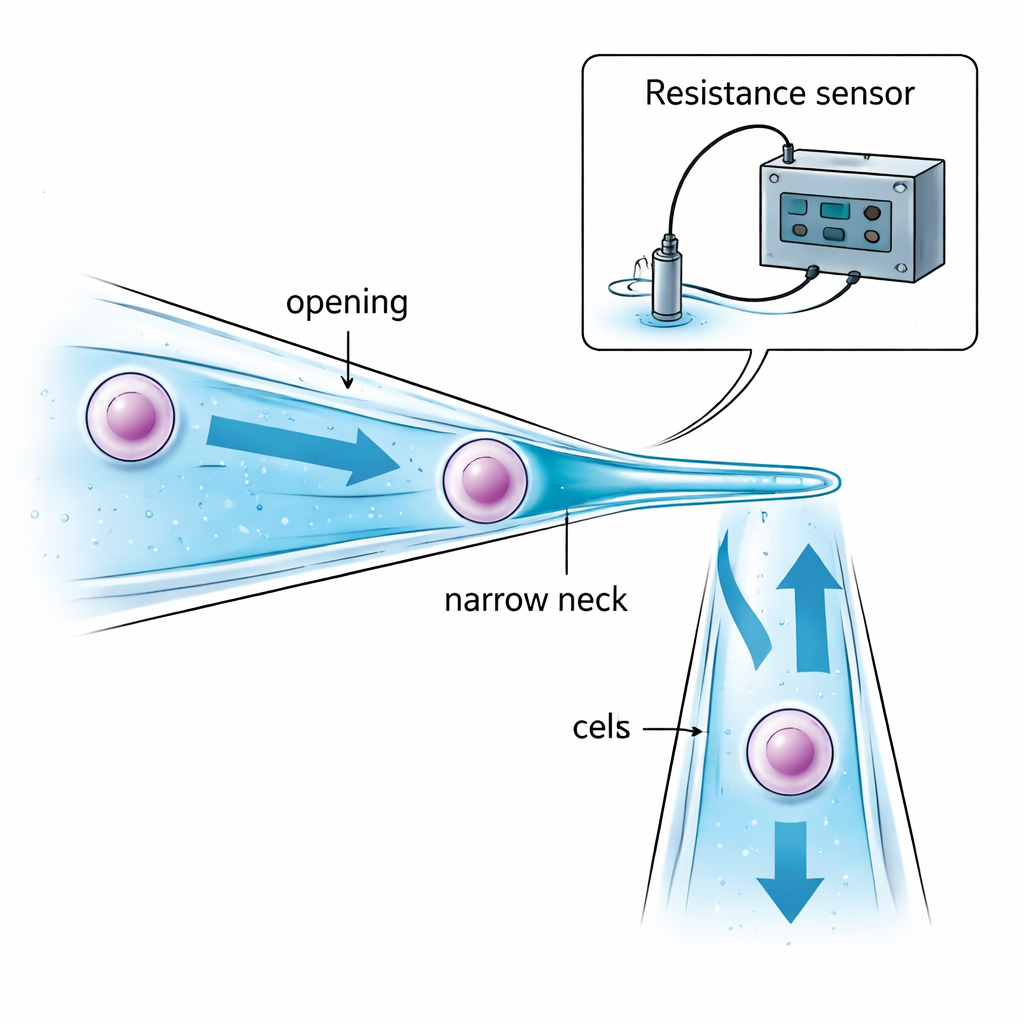
Gli autori affrontano il problema riprogettando la micropipetta stessa. Invece di un tubo di vetro dritto con lo stesso diametro ovunque, hanno creato una micropipetta a collo stretto. L’apertura è leggermente più ampia della cellula bersaglio in modo che la cellula possa essere aspirata all’interno. Più in profondità, il tubo si restringe dolcemente fino a un “collo” più piccolo della cellula. Quando l’aspirazione porta la cellula verso questa strozzatura, la cellula viene fermata e trattenuta all’interno del tubo — invece di rimanere sospesa sulla punta ed essere esposta a olio o aria tra le gocce. Una scelta accurata del diametro dell’apertura, del diametro del collo e della distanza tra essi assicura che la cellula possa essere catturata in modo sicuro senza essere eccessivamente schiacciata, e che venga trasportata solo una piccola quantità di liquido da una goccia all’altra, riducendo la contaminazione.
Ascoltare segnali elettrici invece di guardare
Senza un microscopio, il robot deve comunque sapere tre cose: quando la punta di vetro è abbastanza vicina al fondo della piastra, quando la cellula è stata catturata con successo al collo, e quando è stata completamente rilasciata nella nuova goccia. Il team risolve questo monitorando piccole variazioni della resistenza elettrica nel liquido dentro e attorno alla micropipetta. Man mano che la pipetta inclinata si avvicina al fondo della piastra, il sottile strato di liquido tra loro si assottiglia e la resistenza elettrica aumenta in modo prevedibile, segnalando un atterraggio sicuro poco prima del contatto. Quando una cellula ostruisce il collo stretto, il percorso elettrico attraverso il liquido si contrae e la resistenza sale repentinamente; quando la cellula viene spinta fuori, la resistenza diminuisce altrettanto bruscamente. Modelli matematici di queste resistenze di “gap”, “aspirazione” e “iniezione” permettono a un computer di interpretare questi segnali in tempo reale e di decidere quando interrompere aspirazione o pressione, tutto senza retroazione visiva.
Mettere alla prova il robot
Per verificare se questo approccio funziona nella pratica, i ricercatori hanno costruito un sistema robotico completo che combina controllo di movimento, controllo della pressione, rilevamento della resistenza e un computer host. Lo hanno testato su piccole cellule tumorali note come cellule HeLa (circa 10 micrometri di diametro) e su uova suine molto più grandi (circa 150 micrometri). Il sistema è stato in grado di rilevare in modo affidabile atterraggio, cattura e rilascio esclusivamente dai segnali di resistenza su una vasta gamma di dimensioni di pipetta. In confronti diretti, il robot ha trasferito cellule HeLa con un tasso di successo del 90% — migliore di un metodo automatizzato basato sulla visione precedente — e ha trasportato uova suine con un tasso di successo del 95%, superiore a un approccio microscopico standard. I tempi di operazione per cellula erano simili o più rapidi rispetto ai metodi controllati dall’uomo, soprattutto perché il collo stretto elimina la necessità di continue regolazioni fini dell’aspirazione per posizionare la cellula.
Mantenere le cellule vive e aumentare la scala
Qualsiasi aiuto robotico in laboratorio deve evitare di danneggiare le cellule che manipola. Dopo il trasporto con il nuovo sistema, sia le cellule HeLa sia le uova suine sono state coltivate per un giorno e colorate con un colorante che si illumina solo nelle cellule viventi. I tassi di sopravvivenza del nuovo metodo corrispondevano o si avvicinavano a quelli ottenuti con il trasferimento guidato al microscopio e con le cellule di controllo non manipolate, indicando che la lieve compressione meccanica al collo stretto non riduce in modo significativo la vitalità cellulare quando le soglie sono impostate correttamente. Guardando avanti, gli autori suggeriscono che lo stesso rilevamento basato sulla resistenza e il controllo della pressione possano essere integrati in chip microfluidici compatti. Ciò permetterebbe a molti canali di operare in parallelo, abilitando sistemi di manipolazione cellulare completamente chiusi e ad alta produttività adatti alla medicina riproduttiva automatizzata, alle terapie cellulari e ai dispositivi di coltura cellulare a lungo termine dove i microscopi non sono facilmente collocabili.
Cosa significa per il lavoro cellulare futuro
Per i non specialisti, il messaggio principale è che spostare singole cellule non deve più dipendere da una persona che guarda attraverso un microscopio. Modellando con cura un tubicino di vetro e “ascoltando” come scorre l’elettricità attraverso il liquido circostante, un robot può percepire quando ha toccato, afferrato una cellula e quando l’ha rilasciata — tutto al buio e in spazi ristretti. Questo rende molto più pratico progettare sistemi di coltura cellulare chiusi e autonomi che proteggono campioni fragili, semplificano i flussi clinici e avvicinano la manipolazione cellulare di qualità di laboratorio a operazioni automatizzate simili a quelle di una fabbrica.
Citazione: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Parole chiave: manipolazione cellulare, micropipetta, robotica, microfluidica, automazione