Clear Sky Science · it
Strategie per controllare l’organizzazione spaziale cellulare nei sistemi microfisiologici
Costruire piccoli tessuti in laboratorio
I nostri organi funzionano così bene perché le loro cellule non sono sparse a caso: sono disposte nello spazio con cura. Questo articolo esplora come gli scienziati stanno imparando a ricreare quell’ordine intricato all’interno degli “organi su chip” e di altri tessuti miniaturizzati coltivati in laboratorio. Guidando la posizione delle diverse cellule e il modo in cui interagiscono, i ricercatori possono costruire modelli più realistici di cuore, cervello, intestino, vasi sanguigni e persino di ecosistemi umano–microbici. Questi sistemi avanzati promettono test farmacologici più sicuri, meno esperimenti su animali e strumenti migliori per studiare le malattie e sviluppare terapie personalizzate.
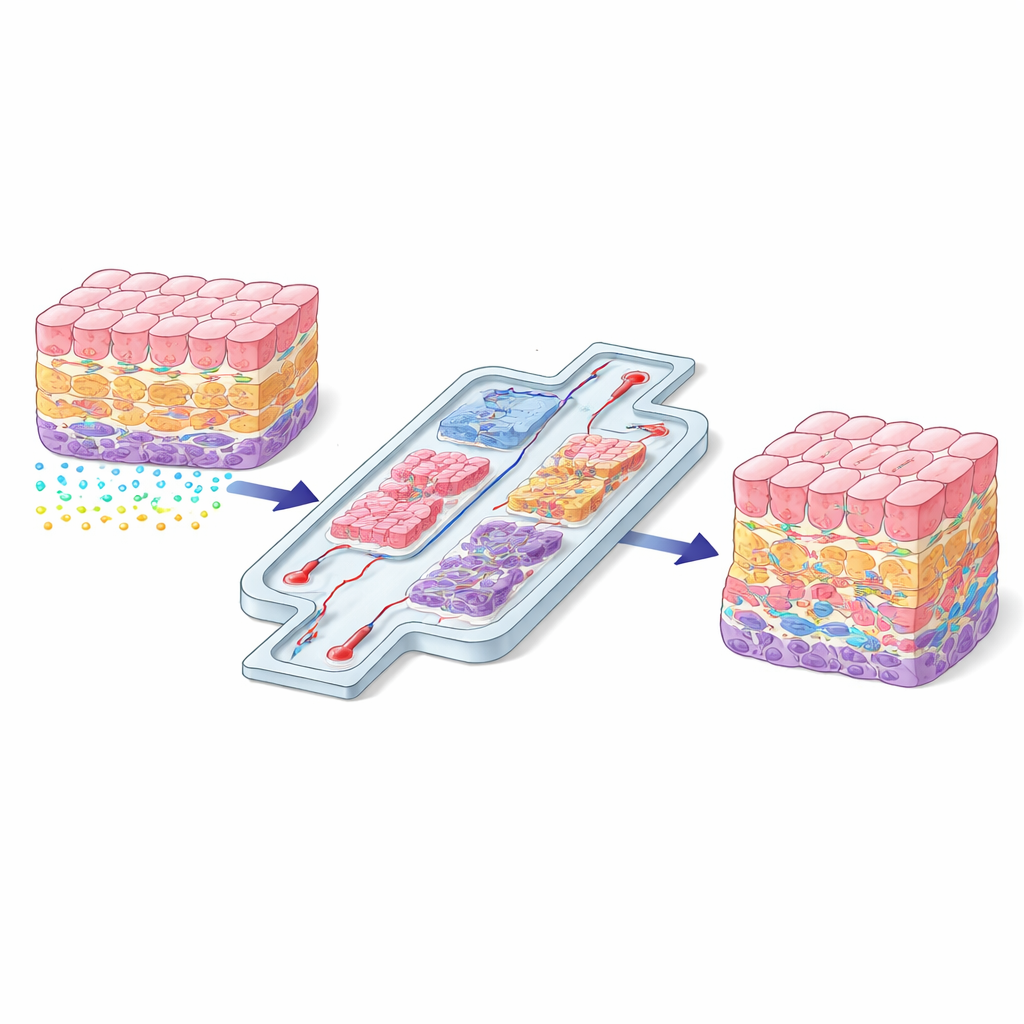
Perché la posizione delle cellule è importante
Nel corpo, ogni cellula vive in un quartiere specifico con la sua miscela di strutture di supporto, segnali chimici e forze fisiche. Una cellula epatica vicino a un vaso sanguigno percepisce stimoli molto diversi rispetto a una cellula sepolta in profondità nell’organo. Queste differenze di posizione contribuiscono a determinare come le cellule crescono, in cosa si differenziano e come rispondono a lesioni o farmaci. Quando gli scienziati coltivano cellule su piastre plastiche piatte, quella “conversazione” spaziale viene in gran parte persa e le cellule spesso si comportano in modo innaturale. L’articolo sostiene che ricreare un’organizzazione spaziale realistica non è un semplice miglioramento facoltativo, ma un requisito di base perché i tessuti coltivati in laboratorio imitino gli organi reali.
Due modalità principali per disporre le cellule
Gli autori raggruppano le strategie attuali in due famiglie ampie: controllo diretto e indiretto. I metodi diretti collocano fisicamente le cellule o i compartimenti esattamente dove servono. Esempi includono la bio-stampa 3D, che deposita strati di cellule e gel morbidi come una stampante 3D biologica; i chip microfluidici che modellano i tessuti in camere e canali connessi; e i metodi di intrappolamento fisico che spingono le cellule in posizione usando luce, suono, magneti o campi elettrici. Questi approcci sono particolarmente efficaci quando è cruciale una geometria precisa—ad esempio per ricreare una barriera emato-encefalica, una parete vascolare stratificata o il percorso di flusso dall’intestino al fegato.
Lasciare che le cellule leggano il loro ambiente
I metodi indiretti invece rimodellano l’ambiente e lasciano che siano le cellule a fare il resto. Qui gli scienziati regolano il “paesaggio” che le cellule percepiscono: la composizione del gel circostante, la rigidità e la texture delle superfici, e i gradienti di sostanze disciolte come fattori di crescita o farmaci. Molecole di supporto disposte con cura possono indurre determinati tipi cellulari a stabilirsi in regioni specifiche. Idrogeli intelligenti che si ammorbidiscono o rilasciano segnali quando le cellule li rimodellano favoriscono strutture auto-organizzate come reti vascolari o cripte e villi simili a quelli intestinali. I dispositivi microfluidici possono generare gradienti chimici stabili che determinano come le cellule staminali assumono identità diverse lungo un canale, o come cellule tumorali e cellule immunitarie migrano in zone distinte, rivelando come le malattie si espandono.
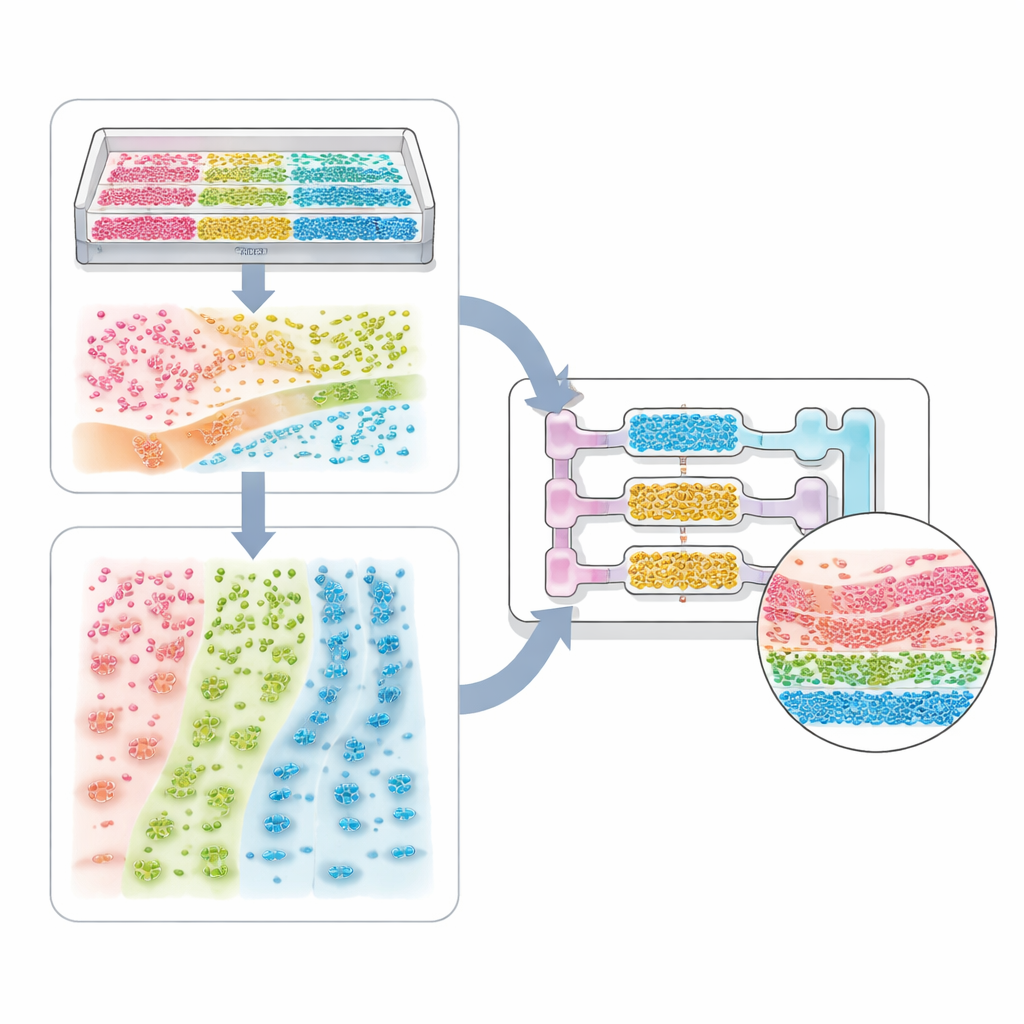
Dai sistemi a cellula singola ai modelli di organismo intero
La review percorre uno spettro di applicazioni. All’estremità più semplice ci sono i sistemi a cellula singola, dove scanalature patternizzate o gradienti di rigidità possono far battere all’unisono le cellule cardiache o indurre i neuroni ad estendere fibre allineate. I modelli tissutali più complessi mescolano più tipi cellulari—come cellule tumorali, cellule di supporto e cellule endoteliali—per formare sferoidi e organoidi con nucleo e corteccia interni. I microcanali e la bio-stampa aggiungono poi confini e flusso, permettendo di ricreare sacchi d’aria polmonari, filtri renali, zone epatiche e circuiti multi-organo che tracciano come un farmaco viene assorbito, trasformato ed eliminato. Le stesse idee si estendono ai sistemi ospite–microbi, dove l’assetto spaziale dei batteri lungo la parete intestinale, o attraverso uno strato di muco, può determinare se essi proteggono o danneggiano l’ospite.
Verificare che i pattern siano reali
Poiché questi sistemi diventano più intricati, gli scienziati hanno bisogno di modi affidabili per confermare che le cellule finiscano dove dovrebbero e si comportino come previsto. L’articolo evidenzia metodi di imaging che possono osservare le cellule vive muoversi e cambiare nel tempo, oltre a tecniche avanzate di colorazione e sequenziamento che mappano quali geni, proteine e metaboliti sono presenti in ciascuna posizione. Sensori integrati nei chip possono monitorare ossigeno, nutrienti, acidi e forze meccaniche, collegando le condizioni locali alle risposte cellulari. Insieme, questi strumenti aiutano i ricercatori a verificare che un progetto non sia solo convincente dal punto di vista visivo, ma fedelmente funzionale rispetto al tessuto reale.
Dove sta andando questo lavoro
Gli autori concludono che i sistemi più potenti fonderanno strategie dirette e indirette: usando chip e bio-stampanti per definire la disposizione generale, quindi sovrapponendo gel, texture e gradienti regolabili che permettano ai tessuti di maturare e rimodellarsi nel tempo. Notano anche ostacoli pratici—come la scalabilità della fabbricazione, la riduzione della variabilità tra laboratori e le questioni etiche legate a modelli tessutali umani complessi. Tuttavia, il messaggio è chiaro: padroneggiare l’organizzazione spaziale è la chiave per trasformare i sistemi microfisiologici in sostituti affidabili degli organi umani, aprendo nuove strade per studiare lo sviluppo, testare terapie e personalizzare la medicina per i singoli pazienti.
Citazione: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Parole chiave: organ-on-a-chip, organizzazione spaziale delle cellule, bio-stampa 3D, modelli tissutali microfluidici, sistemi microfisiologici