Clear Sky Science · it
Piattaforma CRISPR one‑pot per punti di cura per la rilevazione rapida, specifica e sensibile di HPV 16 senza pre‑amplificazione
Perché rilevare un singolo tipo virale è davvero importante
Il cancro cervicale è spesso associato all’infezione da papillomavirus umano (HPV), ma non tutti i tipi di HPV comportano lo stesso rischio. I medici hanno quindi bisogno di test in grado di distinguere in modo affidabile questi virus molto simili, in particolare il tipo ad alto rischio chiamato HPV16. La difficoltà è che i test genetici attuali possono talvolta confondere stretti parenti, provocando falsi allarmi o casi non rilevati. Questo studio presenta un nuovo metodo di test che migliora in modo netto sia l’accuratezza sia la praticità, con l’obiettivo di portare la sottotipizzazione precisa di HPV nelle cliniche e nei contesti point‑of‑care.
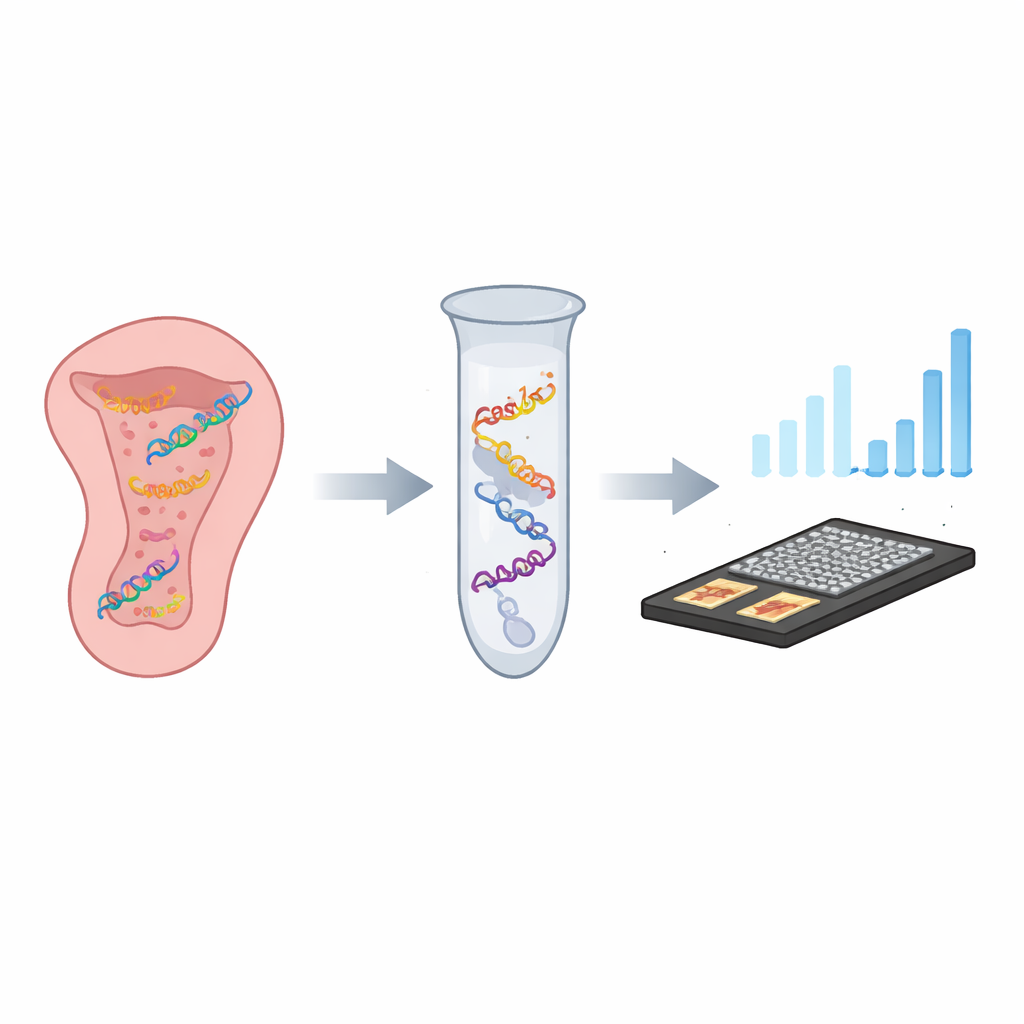
Una serratura e una chiave molecolare intelligenti
I ricercatori hanno sviluppato un test in una singola provetta chiamato CASTSA che combina due idee potenti: la precisione del sistema CRISPR, un sistema di riconoscimento genico adattato dai batteri, e la capacità di amplificazione della PCR, il metodo standard per copiare il DNA. In CASTSA, una proteina CRISPR chiamata Cas12a è guidata verso la sequenza genetica di HPV16 da un breve RNA “chiave”. Quando trova la corrispondenza esatta e un breve motivo adiacente che richiede, Cas12a taglia il DNA virale in un punto prevedibile. Questo taglio crea un estremo libero caratteristico su un filamento di DNA che funge da punto di partenza unico per l’amplificazione. Altri tipi di HPV, anche con sequenze molto simili, non vengono tagliati o non generano il corretto punto di partenza, quindi non vengono amplificati.
Trasformare un piccolo taglio in un segnale forte
Per convertire il taglio mediato da CRISPR in un segnale rilevabile, il team ha progettato un primer speciale chiamato primer terminale‑specifico. Questo primer si lega correttamente solo al filamento prodotto dal taglio di Cas12a, poi si ripiega su se stesso come un forcina e contribuisce a costruire un template stabile per la PCR. Sequenze primer “universali” aggiuntive si ancorano quindi e alimentano una convenzionale reazione di PCR in tempo reale. Fondamentalmente, l’amplificazione avviene solo se Cas12a ha prima svolto il suo compito e se il primer si è ripiegato correttamente, creando due livelli di controllo. Questa architettura riduce nettamente la probabilità che DNA parzialmente corrispondente e non bersaglio venga amplificato accidentalmente, affrontando una debolezza comune dei precedenti test basati su CRISPR che si appoggiavano a un passaggio di pre‑amplificazione separato.
Tutto in un’unica provetta, con meno errori
Un progresso pratico chiave è che il taglio CRISPR e l’amplificazione PCR avvengono insieme nella stessa provetta sigillata, evitando la necessità di aprire le provette tra le fasi — una fonte principale di contaminazione in molti flussi di lavoro di laboratorio. Gli autori hanno accuratamente ottimizzato le condizioni di reazione, in particolare i livelli di magnesio, in modo che sia Cas12a sia l’enzima che copia il DNA lavorino bene senza favorire reazioni spurie. Hanno dimostrato che il loro allestimento one‑pot può distinguere fedelmente HPV16 da diversi altri tipi ad alto rischio, inclusi HPV18, 33, 45 e 52, nonostante questi virus condividano regioni genetiche altamente conservate. Rispetto alla sola PCR in tempo reale standard, o ai test CRISPR che prima amplificano il DNA e poi eseguono la rilevazione CRISPR, CASTSA ha prodotto molti meno segnali fuorvianti da tipi di HPV non bersaglio.
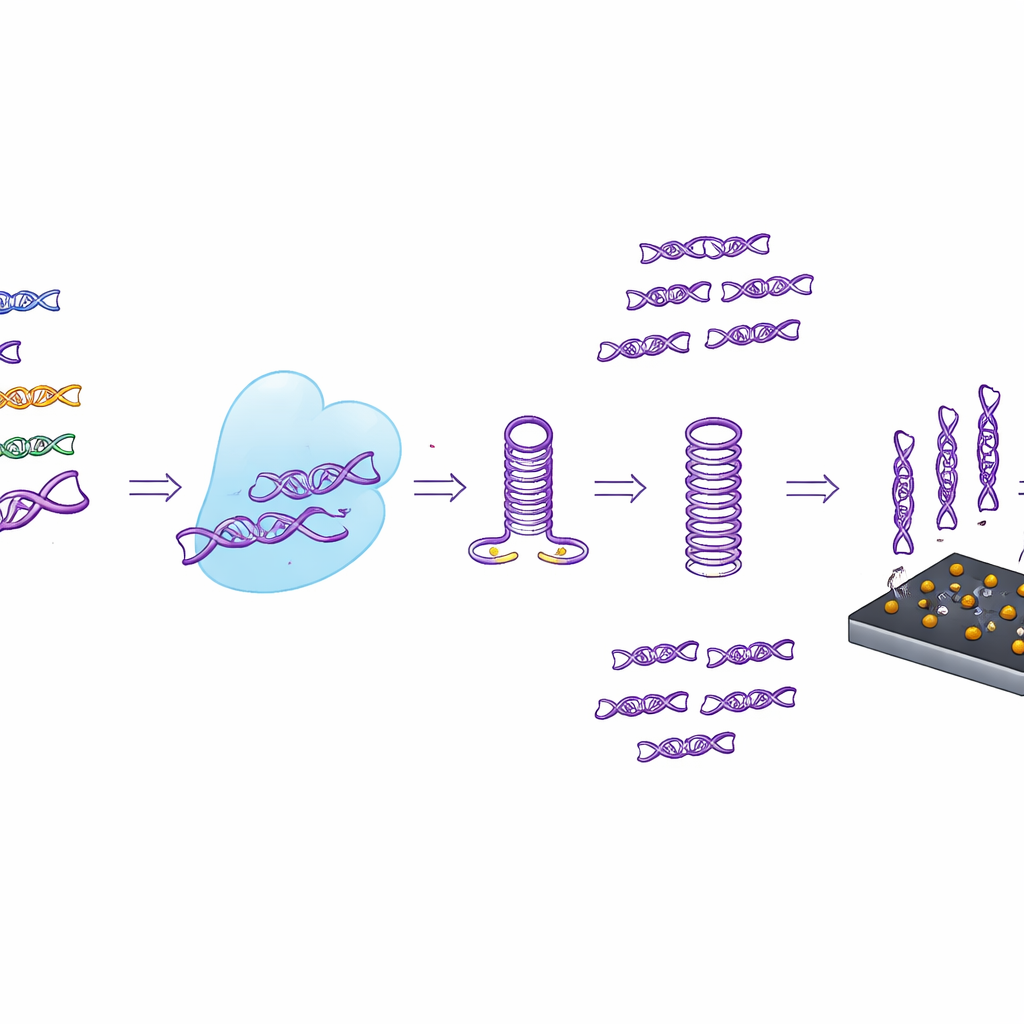
Dalla provetta al sensore portatile
Invece di affidarsi esclusivamente a letture fluorescenti, i ricercatori hanno anche collegato CASTSA a un sensore elettrochimico compatto realizzato con grafene indotto da laser. Questa superficie carboniosa porosa e altamente conduttiva è decorata con nanoparticelle d’oro che portano filamenti di cattura progettati per legarsi solo ai prodotti di amplificazione CASTSA specifici per HPV16. Quando questi prodotti si attaccano, la corrente elettrica attraverso il sensore cambia in modo misurabile. Utilizzando una matrice a quattro elettrodi — tre punti di misura e un controllo di background integrato — il dispositivo può sottrarre il rumore dovuto ad adesioni non specifiche. Nei test, questo sistema integrato ha rilevato fino a 18 copie del target HPV16 per reazione, superando la sensibilità della sola fluorescenza e mantenendo un’eccellente ripetibilità.
Come questo potrebbe trasformare i test per HPV
Per valutare il funzionamento nella pratica clinica, il team ha testato 20 campioni clinici noti per contenere HPV16 e 10 campioni da donatori sani. CASTSA, sia nella versione con lettura fluorescente sia abbinata al sensore a base di grafene, ha concordato completamente con i test PCR ospedalieri standard. Allo stesso tempo, ha mostrato una superiore capacità di ignorare altri tipi di HPV ad alto rischio che spesso generano confusione. Per i pazienti, questo potrebbe tradursi in meno risultati ambigui e decisioni più sicure riguardo follow‑up e trattamento. Più in generale, la strategia CASTSA — riconoscimento CRISPR prima, amplificazione dopo, tutto in una provetta sigillata — offre uno schema per test genetici altamente specifici e a bassa contaminazione che potrebbero essere adattati a molti patogeni e mutazioni, specialmente in contesti che richiedono risposte rapide e affidabili.
Citazione: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Parole chiave: Rilevazione HPV16, Diagnostica CRISPR, Test basati su PCR, Biosensore elettrochimico, Test point‑of‑care