Clear Sky Science · it
Microscopia a scansione per immagini interferometriche per imaging senza marcatori a risoluzione laterale di 120 nm all'interno di cellule vive
Osservare cellule vive senza coloranti aggiunti
La biologia moderna si affida spesso a etichette fluorescenti per rivelare l'architettura nascosta all'interno delle cellule. Tuttavia questi marcatori possono stressare le cellule, modificare il loro comportamento e a volte non sono utilizzabili in campioni fragili o difficili da modificare geneticamente. Questo articolo introduce un nuovo modo di osservare i processi nelle cellule vive con grande dettaglio—senza aggiungere coloranti o tag genetici—promettendo osservazioni più delicate, prolungate e più naturali di come le cellule funzionano realmente.
Guardare le cellule attraverso la luce che diffondono
Il metodo si basa su una famiglia di tecniche che non dipendono dalla fluorescenza, ma misurano come piccole strutture diffondono la luce. Una di queste tecniche, la microscopia a scattering interferometrico (iSCAT), combina la luce diffusa da un oggetto nanoscopico con un riflesso di riferimento da una superficie di vetro. Il pattern d'interferenza risultante è estremamente sensibile a particelle molto piccole come proteine, virus o vescicole. iSCAT ha funzionato finora meglio su campioni semplici e puliti, come particelle isolate su vetro. Applicarlo in profondità all'interno di cellule vive è stato però difficile perché le cellule sono affollate e disordinate: molti eventi di scattering sovrapposti producono uno sfondo puntinato che nasconde i dettagli fini.
Combinare due idee per imaging più nitido e più delicato
Per superare questi limiti, gli autori hanno combinato iSCAT con una potente strategia di imaging chiamata image scanning microscopy (ISM). In ISM, il campione viene scandito punto per punto con un fascio focalizzato e, invece di usare un singolo rivelatore, un array di pixel registra molte viste leggermente spostate di ciascun punto. Riallineando e combinando astutamente queste viste, è possibile rendere più nitida l'immagine finale senza sprecare fotoni preziosi. La nuova tecnica—microscopia a scansione per immagini interferometriche, o iISM—adatta questa idea ai segnali più complessi e sensibili alla fase dello scattering interferometrico. Il microscopio impiega un laser blu, ottiche speciali per rendere simmetrica la polarizzazione della luce e una camera sensibile per registrare la luce diffusa e riflessa a ogni posizione di scansione. Un flusso di lavoro computazionale su misura rialloca quindi le informazioni dei pixel in modo che rispetti la natura ondulatoria del segnale, producendo immagini con una risoluzione laterale di circa 120 nanometri, approssimativamente il doppio più fine rispetto all'ottica limitata dalla diffrazione standard.
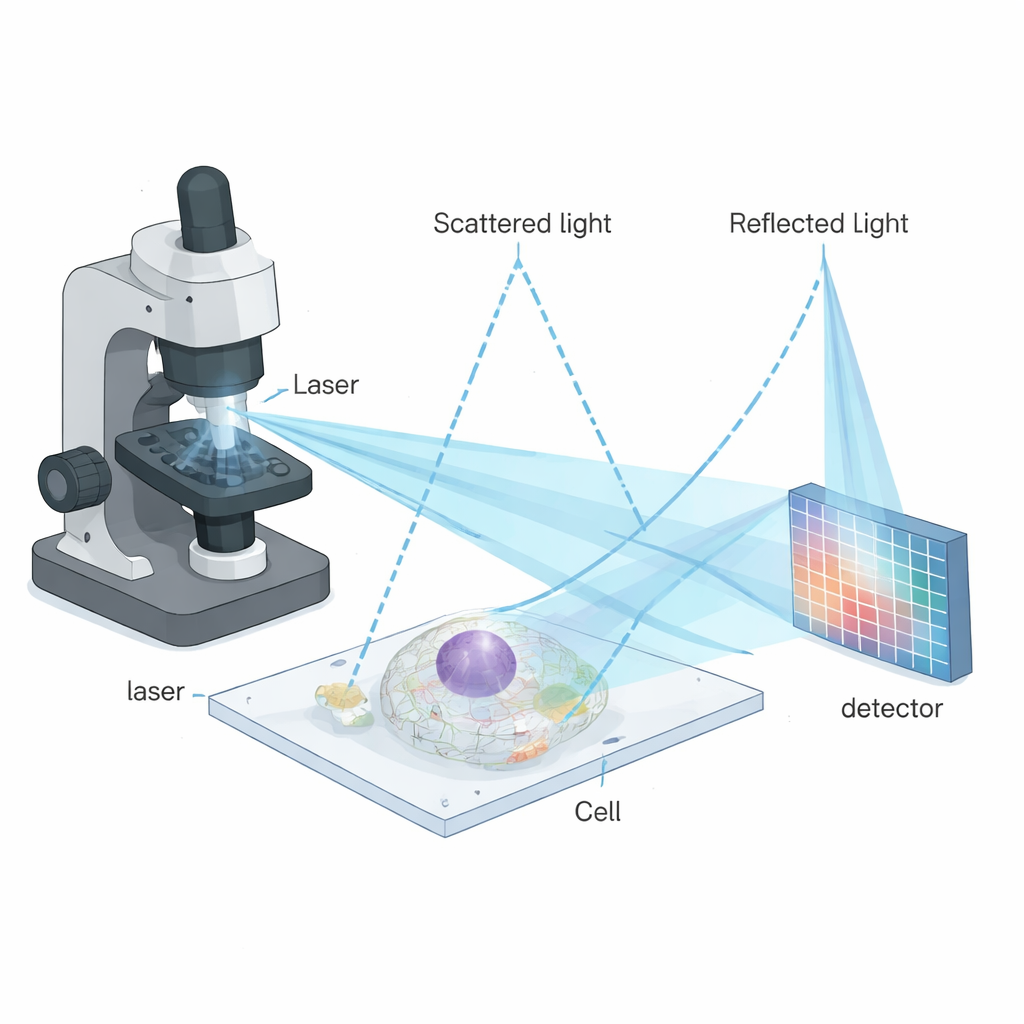
Algoritmi intelligenti trasformano pattern rumorosi in immagini nitide
Poiché i segnali interferometrici contengono sia informazioni di intensità sia di fase, i consueti trucchi di elaborazione usati per la fluorescenza non sono sufficienti. Gli autori hanno progettato una procedura di riallocazione adattiva dei pixel (APR) studiata per luce coerente. Per prima cosa trasformano ciascun piccolo pattern interferometrico in una mappa di “varianza radiale” che evidenzia i centri di simmetria senza preoccuparsi se il segnale sia positivo o negativo. Questo passaggio converte efficacemente frange d'interferenza complesse in immagini che si comportano più come normali immagini di intensità. Poi, utilizzando software open source, determinano di quanto l'immagine di ciascun pixel del rivelatore è spostata rispetto al centro e le riallineano prima di sommarle. Questo affinamento concentra il segnale utile mentre media il rumore, aumentando il rapporto contrasto/rumore di circa un fattore quattro rispetto a un'immagine confocale iSCAT con foro molto stretto, tutto allo stesso livello di luce.
Osservare organelli e citoscheletri in azione
Con questi progressi tecnici, il gruppo ha testato iISM su cellule COS-7 vive per valutare le prestazioni nella pratica. Con potenze di illuminazione molto basse—circa dieci volte inferiori per punto focalizzato rispetto a quelle tipicamente usate nei microscopi confocali convenzionali—sono riusciti a distinguere chiaramente organelli chiave: il reticolo endoplasmatico, i mitocondri, le vescicole, il citoscheletro di actina, la membrana plasmatica e sottili strutture di bordo chiamate lamellipodi. Poiché il contrasto interferometrico dipende sensibile dalla posizione verticale, organelli simili possono apparire con contrasto positivo o negativo, rivelando differenze di altezza sottili di poche centinaia di nanometri. Registrando sequenze time-lapse, hanno seguito vescicole in movimento e il rimodellamento dei tubuli del reticolo endoplasmatico per molti minuti, senza evidenti fotodanni e senza segni che l'imaging stesse perturbando il comportamento cellulare.
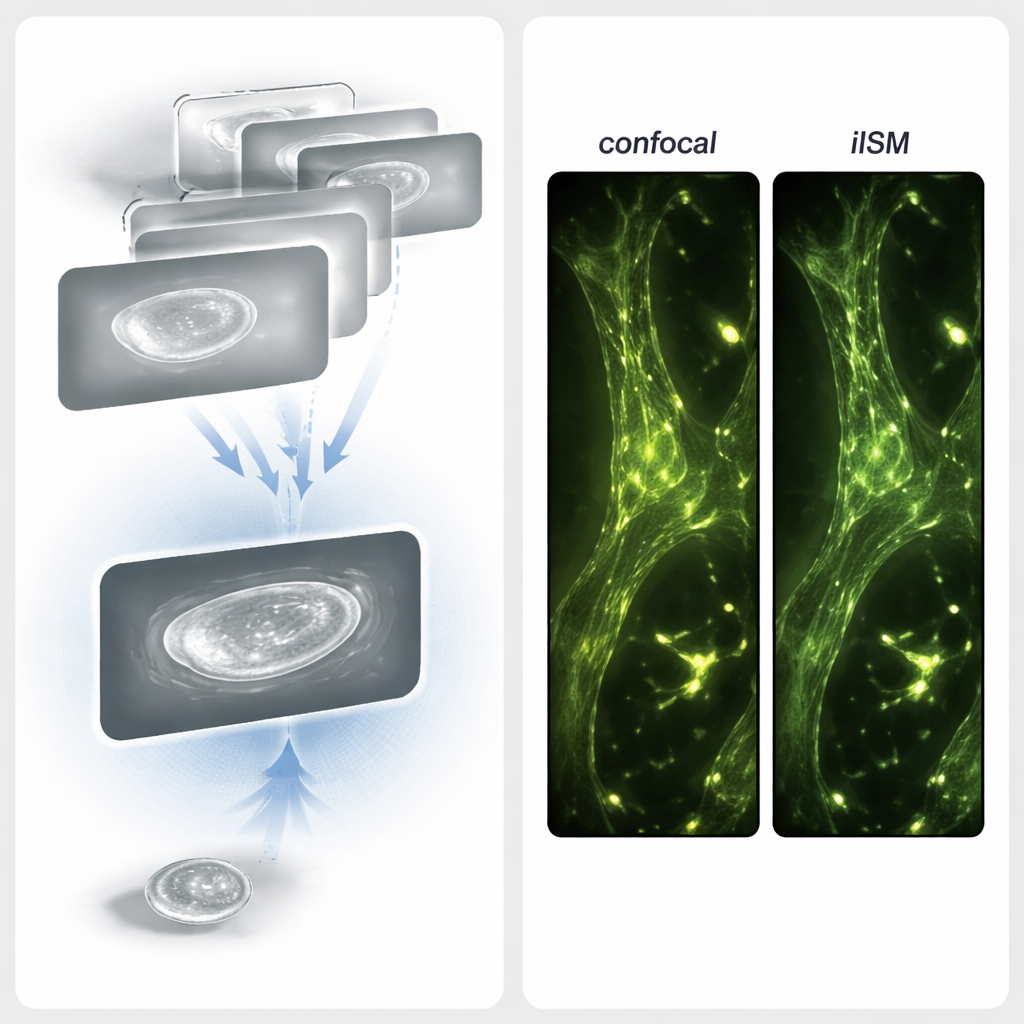
Accoppiare viste senza marcatori con mappe fluorescenti
Per verificare che le immagini senza marcatori riflettessero realmente le strutture cellulari, i ricercatori hanno eseguito misurazioni combinate iISM e ISM a fluorescenza su cellule fissate. Hanno colorato il citoscheletro di actina con un colorante fluorescente rosso e registrato immagini fluorescenti super-risolte insieme alle immagini iISM senza marcatori della stessa regione. Sovrapponendo le due immagini, i filamenti di actina luminosi nel canale di fluorescenza si sono allineati strettamente con le caratteristiche filamentose nelle immagini iISM. In alcune regioni, iISM ha anche rivelato dettagli di scattering aggiuntivi—come variazioni lungo i filamenti o strutture vicine non marcate come le adesioni focali—that erano invisibili nel canale di fluorescenza. Nel complesso, questi risultati mostrano che iISM può sia confermare strutture note sia scoprire informazioni supplementari sull'ambiente non marcato.
Una nuova finestra sulle cellule, con meno disturbo
Per i non specialisti, il messaggio chiave è che iISM offre un modo per vedere dettagli fini all'interno di cellule vive senza renderle artificialmente fluorescenti. Combina la sensibilità dello scattering interferometrico con il potenziamento della nitidezza dell'image scanning, raggiungendo circa 120 nanometri di risoluzione laterale usando molto meno luce rispetto a molti microscopi esistenti. Poiché è costruito con componenti già comuni nei sistemi confocali avanzati, in linea di principio può essere aggiunto a strumenti commerciali. In futuro, iISM potrebbe essere abbinato alla fluorescenza tradizionale, a rivelatori veloci o persino a “colorazioni virtuali” basate sull'apprendimento automatico per seguire infezioni, trasporto di carico o riorganizzazioni del citoscheletro in condizioni più vicine allo stato naturale e non perturbato delle cellule.
Citazione: Küppers, M., Moerner, W.E. Interferometric Image Scanning Microscopy for label-free imaging at 120 nm lateral resolution inside live cells. Light Sci Appl 15, 129 (2026). https://doi.org/10.1038/s41377-026-02210-y
Parole chiave: imaging senza marcatori, microscopia su cellule vive, scattering interferometrico, super-risoluzione, organelli cellulari