Clear Sky Science · it
Letalità sintetica dell’inibizione di MCL-1 e della terapia CAR-T nei linfomi B aggressivi
Perché conta per il trattamento del cancro
I linfomi B aggressivi sono tumori del sangue a crescita rapida che spesso recidivano dopo il trattamento. Anche approcci innovativi e potenti come la terapia CAR-T, che riprogramma le cellule immunitarie del paziente per attaccare il cancro, falliscono in circa la metà dei pazienti nel tempo. Questo studio esplora un modo per trasformare quella debolezza in un punto di forza: usare un farmaco che prende di mira una proteina chiave per la sopravvivenza delle cellule del linfoma per uccidere i tumori e rendere le cellule residue più facili da eliminare con le cellule CAR-T.
Il problema delle cellule di linfoma ostinate
I linfomi B aggressivi sono frequentemente guidati da un’attività eccessiva del gene MYC, che spinge le cellule a dividersi rapidamente e le aiuta anche a nascondersi dal sistema immunitario. I trattamenti standard e persino la terapia CAR-T possono lasciare dietro di sé piccole sacche di cellule linfomatose che tollerano i farmaci e causano recidive in seguito. Queste cellule “persister” e resistenti vivono in un quartiere tumorale affollato di cellule immunitarie soppressive che tengono a bada le cellule T assassine. Gli autori si sono chiesti se bloccare MCL-1, una proteina da cui le cellule del linfoma dipendono per evitare l’autodistruzione, potesse rivelare una debolezza nascosta in questo sistema.
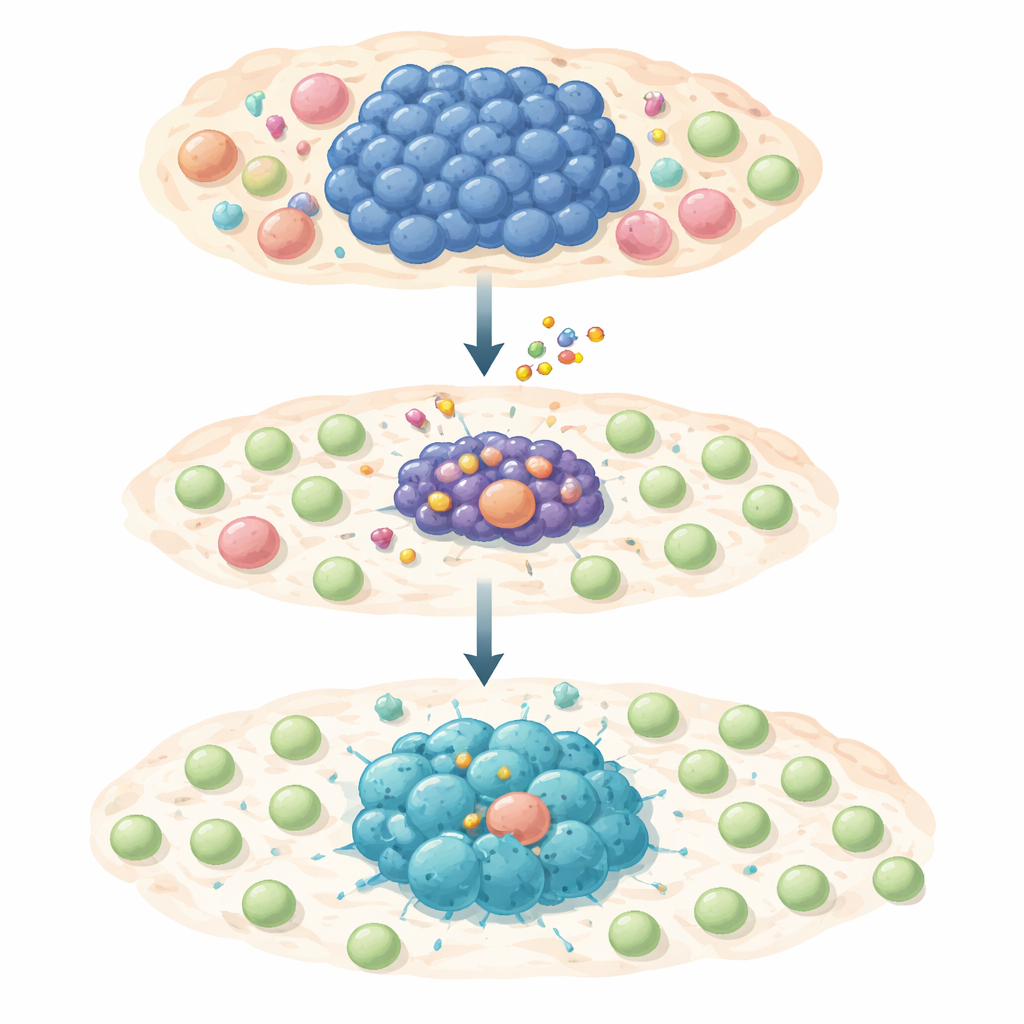
Un attacco in due fasi contro la sopravvivenza e la capacità di occultamento del tumore
Il team ha testato un farmaco selettivo che blocca MCL-1, S63845, su un ampio pannello di linee cellulari di linfoma umano dipendenti da MYC. La maggior parte di queste cellule tumorali era altamente sensibile al farmaco e subiva morte programmata quando MCL-1 veniva inibito. Tuttavia, una piccola frazione sopravviveva all’esposizione a breve o lungo termine e diventava tollerante al farmaco o completamente resistente. Quando i ricercatori hanno esaminato questi sopravvissuti in dettaglio, hanno scoperto che l’attività di MYC era attenuata mentre un’altra molecola, STAT1, e la sua via di allarme interferon associata erano attivate. Questo cambiamento accendeva geni che guidano segnali infiammatori e chemochine—“flares” molecolari che possono richiamare cellule T nell’area tumorale.
Riattivare il quartiere immunitario
Per capire come ciò si manifestasse in un organismo vivente, gli autori hanno trattato topi portatori di linfomi guidati da MYC con una dose bassa dell’inibitore di MCL-1. Il farmaco ha ridotto il carico tumorale pur risparmiando le cellule B normali, ma il suo impatto andava oltre il semplice ridimensionamento. I tumori trattati mostravano più cellule T CD4 e CD8, meno cellule T esauste, meno cellule T regolatorie e meno cellule mieloidi soppressive, tutti segni di un ambiente più favorevole all’immunità. Il sequenziamento dell’RNA a singola cellula delle cellule tumorali e circostanti ha confermato che le cellule linfomatose residue avevano MYC ridotto, STAT1 aumentato e segnali interferon e infiammatori più forti, mentre i tessuti circostanti si ripopolavano di cellule T e cellule natural killer attive piuttosto che di cellule soppressive.
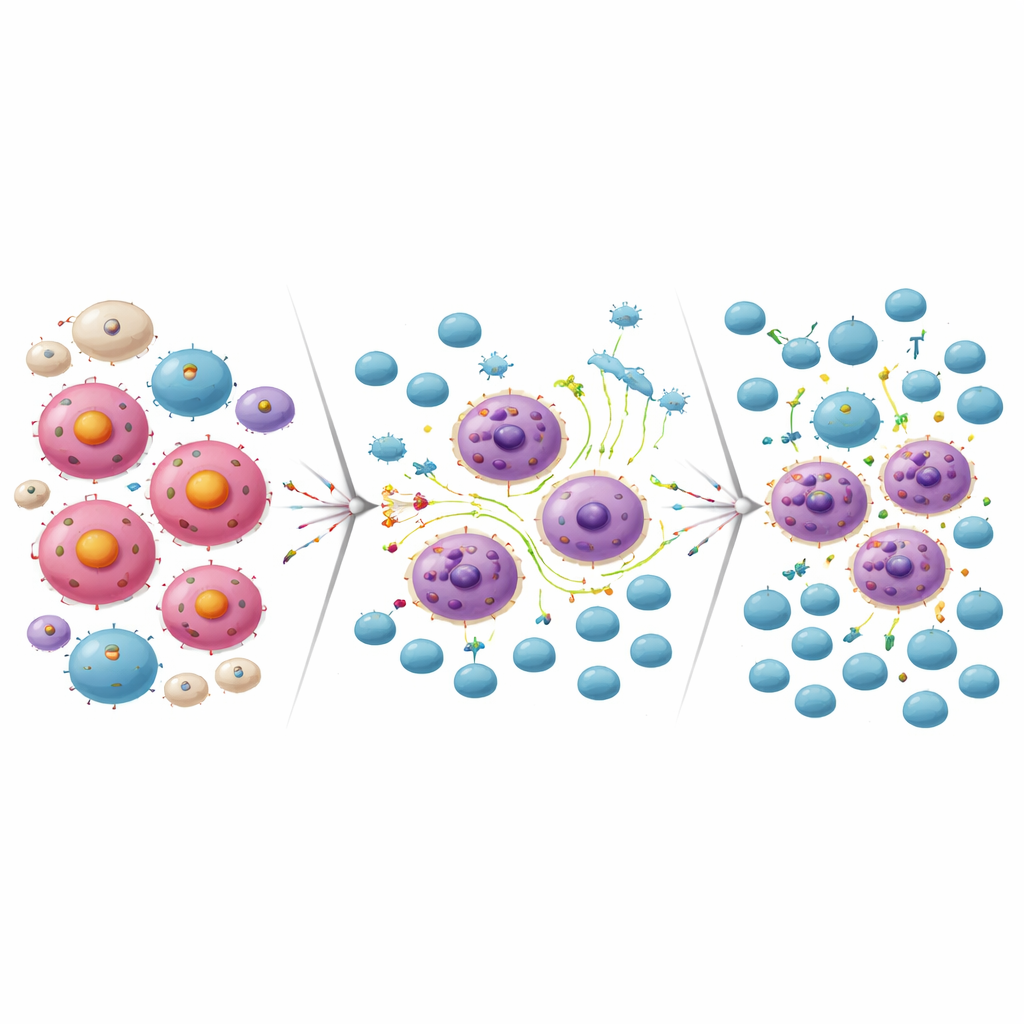
Trasformare la resistenza in un’apertura per le cellule CAR-T
La stessa riprogrammazione infiammatoria che ha aiutato alcune cellule di linfoma a sopravvivere al blocco di MCL-1 le ha anche rese più vulnerabili all’attacco immunitario. In laboratorio, le cellule CAR-T dirette contro CD19 hanno eliminato efficacemente le cellule di linfoma che erano diventate resistenti al farmaco MCL-1. Al contrario, le cellule di linfoma rese resistenti alla terapia CAR-T anti-CD19 erano altamente sensibili all’inibitore di MCL-1. Quando i ricercatori hanno combinato una dose subletale del farmaco MCL-1 con cellule CAR-T in coltura cellulare, i due trattamenti insieme hanno eliminato molte più cellule di linfoma rispetto a ciascuno singolarmente. Nei modelli murini, somministrare l’inibitore di MCL-1 seguito da cellule CAR-T anti-CD19 ha portato a una quasi completa eliminazione del tumore e a una sopravvivenza significativamente più lunga rispetto ai singoli trattamenti.
Un duplice colpo con potenziale curativo
In termini semplici, lo studio suggerisce una strategia a “colpo doppio”. Primo, un farmaco che blocca MCL-1 abbatte la maggior parte del linfoma e costringe le cellule tumorali sopravvissute in uno stato infiammato e altamente visibile che attira le cellule T e spoglia gli scudi immunitari protettivi. Secondo, le cellule CAR-T anti-CD19 sfruttano questa debolezza appena esposta per eradicare la malattia residua. Colpendo sia il cablaggio interno della sopravvivenza del tumore sia il suo quartiere protettivo, questo approccio combinato potrebbe ridurre le recidive e avvicinare i linfomi B aggressivi a una remissione di lunga durata.
Citazione: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Parole chiave: Linfoma B, Terapia CAR-T, Inibizione di MCL-1, Microambiente tumorale, Resistenza ai farmaci