Clear Sky Science · it
La repressione di miR-29 tramite MYC porta a un aumento della segnalazione CD40 nel linfoma follicolare trasformato
Quando il dialogo cellula‑cellula diventa pericoloso
Il linfoma follicolare è un tumore del sangue a crescita lenta che può covare per anni, ma in alcuni pazienti cambia improvvisamente ritmo e diventa una malattia rapida e potenzialmente letale. Questo studio pone una domanda semplice ma cruciale: cosa cambia all’interno di queste cellule tumorali, e nel loro vicinato cellulare, per far scattare questo interruttore? Seguendo sia i geni delle cellule tumorali sia i piccoli regolatori a RNA durante questa transizione, i ricercatori scoprono un circuito di controllo nascosto che modula quanto intensamente le cellule tumorali rispondono all’aiuto delle cellule immunitarie vicine — e mostrano che quando questo circuito viene meno, il cancro diventa più difficile da trattare.
Un cancro silenzioso che a volte accelera
Il linfoma follicolare deriva dalle cellule B, le cellule del sistema immunitario che normalmente producono anticorpi. La maggior parte dei pazienti convive con una forma indolente, o lenta, della malattia, ma ogni anno una frazione dei casi si trasforma in un linfoma aggressivo che si comporta più come un linfoma diffuso a grandi cellule B. Mutazioni genetiche erano state associate a questo cambiamento, ma non spiegavano tutto. Le cellule tumorali vivono in un microambiente ricco di cellule T helper e altri partner immunitari, scambiando segnali in continuazione. Gli autori hanno sospettato che piccole molecole regolatorie chiamate microRNA, che regolano finemente l’uso dei geni, potessero essere la chiave per capire come le cellule tumorali si adattano a questo vicinato mutevole e compiono il salto verso uno stato più pericoloso.
I freni a RNA piccoli vengono a mancare
Per mettere alla prova questa idea, il gruppo ha effettuato il primo profilo accoppiato di mRNA e microRNA su campioni abbinati prelevati dagli stessi pazienti prima e dopo la trasformazione. Confrontando 11 campioni di linfoma follicolare con i rispettivi 11 controparti trasformate, hanno trovato oltre mille geni e 19 microRNA che cambiavano. È emersa una famiglia in particolare: tutti e tre i membri della famiglia miR‑29 risultavano costantemente ridotti nei tumori trasformati. In lavori precedenti su altri tumori del sangue, miR‑29 aveva agito come un freno alla crescita e alla sopravvivenza cellulare. Qui, la sua perdita è emersa come un tratto distintivo della trasformazione, suggerendo che l’abbassamento di questa famiglia di microRNA potrebbe liberare vie promuoventi la crescita nelle cellule del linfoma.
Un segnale potenziato dalle cellule helper
Analizzando i dati di espressione genica, i ricercatori hanno scoperto che i tumori trasformati mostravano un forte aumento dell’attività della via CD40, una via di segnalazione che si attiva quando una cellula T helper interagisce con una cellula B. Nei linfonodi sani e nel linfoma follicolare indolente, questa interazione aiuta le cellule B a crescere e sopravvivere in modo controllato. Sorprendentemente, nei campioni trasformati i geni correlati a CD40 risultavano attivi in circa il 90% dei casi, nonostante il numero complessivo di cellule T nelle aree tumorali fosse in realtà inferiore. Analisi a singola cellula hanno confermato che una sottopopolazione di cellule T forniva ancora il segnale attivante CD40, ma le cellule del linfoma sembravano essere diventate molto più sensibili a quel segnale.
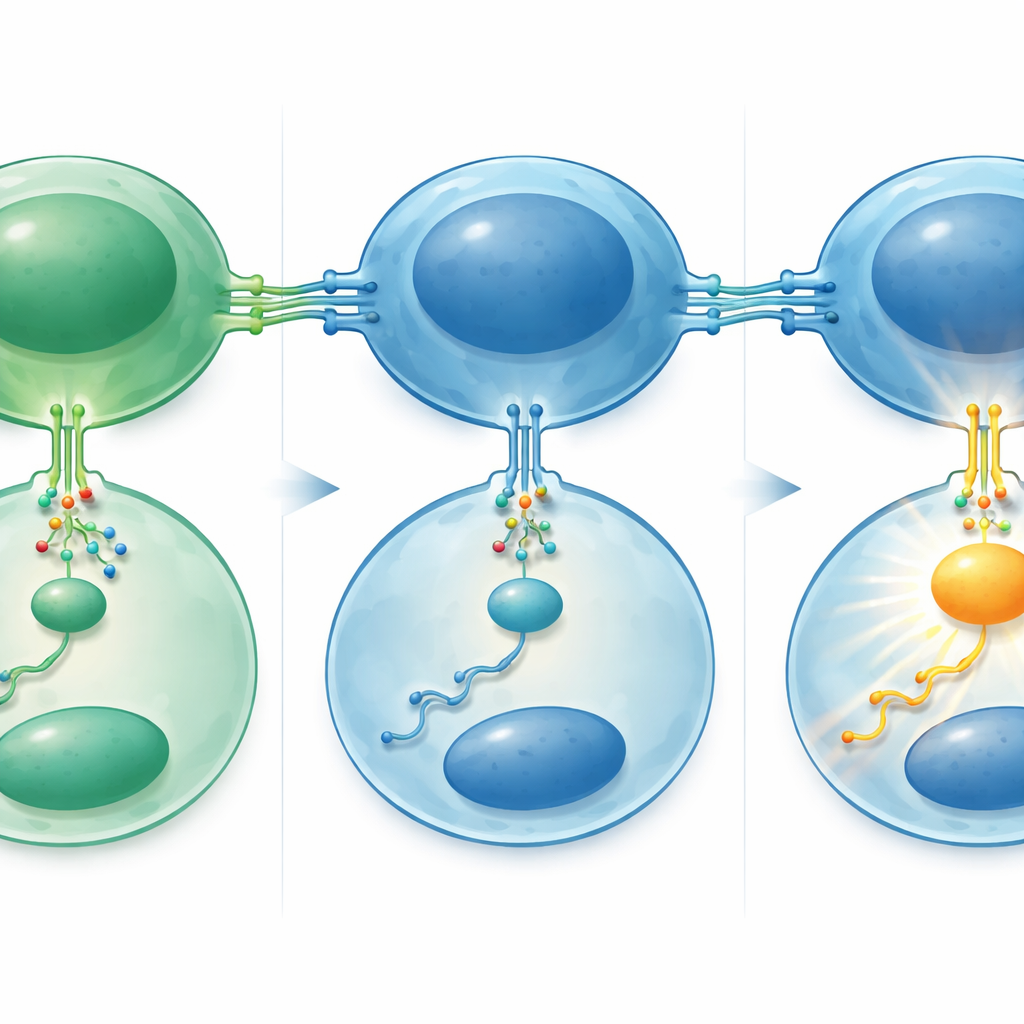
Come un circuito in tre passaggi amplifica la crescita
Gli autori hanno quindi ricostruito il circuito molecolare alla base di questa sensibilità aumentata. Esperimenti di laboratorio hanno mostrato che miR‑29 normalmente mantiene sotto controllo i livelli di una proteina chiamata TRAF4 nelle cellule B; TRAF4 è un adattatore interno che aiuta a trasmettere il segnale CD40 più in profondità nella cellula. Quando i livelli di miR‑29 venivano aumentati sperimentalmente in linee cellulari di linfoma, i livelli di TRAF4 diminuivano e le cellule rispondevano in misura minore alla stimolazione CD40, con una minore attivazione della segnalazione a valle e una proliferazione più lenta. Nei campioni dei pazienti appariva il pattern opposto: i tumori trasformati e i linfomi follicolari di grado più elevato mostravano più TRAF4 e tassi di divisione cellulare più alti. Un altro attore importante, la ben nota proteina promotrice di tumori MYC, stava a monte. I livelli e l’attività di MYC aumentavano durante la trasformazione, e MYC è stato dimostrato legarsi direttamente alle regioni di DNA che controllano miR‑29, agendo come un interruttore che spegne questa famiglia di microRNA.
Cosa significa questo per i pazienti
Mettere insieme questi elementi, lo studio delinea una catena in tre passaggi: l’attivazione di MYC sopprime miR‑29, la perdita di miR‑29 toglie il freno a TRAF4, e l’eccesso di TRAF4 rende le cellule del linfoma iper‑rispondenti ai segnali CD40 provenienti dalle poche cellule T helper rimaste. Questo “aiuto” amplificato guida una crescita e una sopravvivenza più robuste, contribuendo alla trasformazione. Clinicamente, i pazienti i cui tumori presentavano livelli più bassi di miR‑29 — in particolare il membro miR‑29c — tendevano ad avere una sopravvivenza più breve e ricadute più rapide, risultati confermati in uno studio clinico indipendente. Poiché miR‑29 può essere misurato con affidabilità anche in campioni bioptici vecchi e conservati, e poiché farmaci che mimano miR‑29 o bloccano la segnalazione CD40 sono già in fase di esplorazione, questo lavoro indica nuove vie per identificare i pazienti con linfoma follicolare ad alto rischio e per progettare terapie che interrompano la pericolosa conversazione tra cellule tumorali e i loro vicini immunitari.
Citazione: Filip, D., Litzmanova, K., Michaelou, A. et al. Repression of miR-29 via MYC leads to increased CD40 signaling in transformed follicular lymphoma. Leukemia 40, 759–772 (2026). https://doi.org/10.1038/s41375-026-02868-8
Parole chiave: linfoma follicolare, microRNA, segnalazione CD40, MYC, microambiente tumorale