Clear Sky Science · it
JAK2V617F riprogramma il Fattore Inducibile dall'Ipoxia‑1 per indurre un regolone ipossico non canonico nelle neoplasie mieloproliferative
Perché è importante per i tumori del sangue
Alcuni tumori del sangue a crescita lenta, noti come neoplasie mieloproliferative, possono bruciare lentamente per anni prima di trasformarsi improvvisamente in una forma aggressiva di leucemia. Questo studio pone una domanda semplice ma cruciale: come una mutazione oncogenica comune dirotta il sistema intracellulare di rilevazione dell'ossigeno, e si può colpire questa dirotta-ment senza danneggiare le cellule sane? Le risposte potrebbero aprire una nuova via terapeutica per i pazienti ad alto rischio, risparmiando allo stesso tempo i tessuti normali che dipendono anch'essi dai segnali di rilevazione dell'ossigeno.
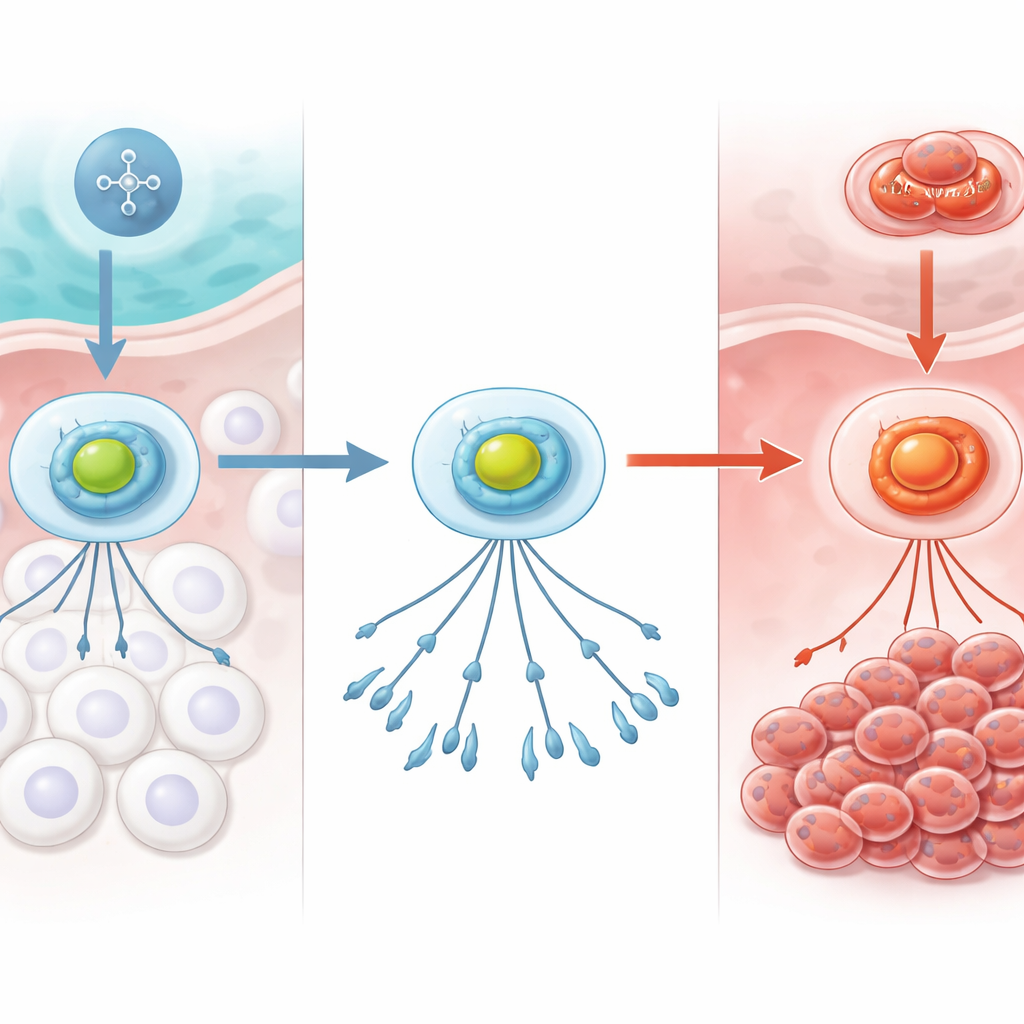
Il sistema d'allarme dell'ossigeno nel corpo
Le cellule monitorano costantemente la disponibilità di ossigeno. Al centro di questo sistema c'è un complesso proteico chiamato HIF‑1, che funziona come un allarme per l'ossigeno. In condizioni normali e ben ossigenate, una subunità di HIF‑1 viene rapidamente degradarta, mantenendo l'allarme spento. Quando l'ossigeno diminuisce, questa degradazione si arresta, HIF‑1 si stabilizza, si sposta sul DNA cellulare e attiva geni che aiutano le cellule ad adattarsi, per esempio cambiando il modo in cui usano l'energia o favorendo la crescita di nuovi vasi sanguigni. Nel cancro, lo stesso sistema può essere sfruttato a vantaggio del tumore, aiutando le cellule maligne a sopravvivere in ambienti stressanti come il midollo osseo a basso ossigeno.
Quando una mutazione ricollega l'allarme
I ricercatori si sono concentrati su una mutazione chiamata JAK2V617F, molto comune nelle neoplasie mieloproliferative. Lavori precedenti avevano mostrato che questa mutazione mantiene l'allarme HIF‑1 acceso anche quando l'ossigeno è abbondante. Usando linee cellulari ingegnerizzate, il gruppo ha confrontato il legame di HIF‑1 al DNA in due condizioni: vera ipossia e ossigeno normale in presenza della mutazione JAK2V617F. Hanno scoperto che nelle cellule mutate HIF‑1 si lega a meno regioni del genoma, è meno sensibile alle variazioni di ossigeno e interagisce con un diverso set di proteine partner, molte delle quali coinvolte nell'elaborazione dell'RNA. In altri termini, la mutazione non si limita a tenere HIF‑1 permanentemente “acceso” — riallinea l'allarme verso un diverso insieme di bersagli.
Un programma genico specifico del cancro
Dagli esperimenti gli autori hanno definito diversi insiemi di geni dipendenti da HIF‑1, incluso quello che chiamano firma ipossica JAK2V617F. Hanno quindi valutato quanto queste firme fossero attivate nelle cellule del sangue di 172 pazienti con neoplasie mieloproliferative positive per JAK2V617F. Sorprendentemente, i canonici programmi genici HIF‑1 associati alla bassa ossigenazione non hanno predetto la gravità della malattia o la sopravvivenza. Al contrario, la firma ipossica specifica della mutazione ha distinto chiaramente i pazienti con malattia più severa ed è risultata associata a una peggiore sopravvivenza complessiva. Molti dei geni in questo insieme erano particolarmente attivi nei progenitori megacariocitari, le cellule del midollo che sovracrescono e guidano la fibrosi in questi disturbi, e alcuni erano implicati nella riparazione del danno al DNA — un processo che può aiutare le cellule tumorali a sopravvivere a stress dannosi.
Indizi per il peggioramento improvviso della malattia
Una paura importante per i pazienti è la trasformazione improvvisa da una malattia cronica a una leucemia aggressiva in “fase blastica”. Analizzando campioni abbinati pre e post trasformazione, il gruppo ha individuato un sottoinsieme ridotto di 13 geni, chiamato firma HIF1‑MPN‑BP, i cui livelli aumentavano o diminuivano con la trasformazione. Questo sottoinsieme è risultato fortemente associato a punteggi di rischio più elevati, peggior sopravvivenza e maggiore fibrosi midollare. È importante che questo pattern sembri specifico per la malattia guidata da JAK2V617F, e non una caratteristica generica di tutte le leucemie. Molti geni di questo sottoinsieme sono plausibili bersagli farmacologici, suggerendo un elenco mirato di candidati per terapie future volte a bloccare la progressione.
Alla ricerca dell'aiutante nascosto della mutazione
Come fa JAK2V617F a mantenere HIF‑1 attivo indipendentemente dall'ossigeno? Attraverso approcci di chimica proteica, gli autori hanno scoperto che nelle cellule mutate HIF‑1 porta due marcature chimiche precedentemente sconosciute (fosforilazioni) in una regione che normalmente controlla la sua degradazione. Hanno ricondotto questi cambiamenti a PIM1, una chinasi attivata a valle della mutazione JAK2. Bloccare PIM1 con farmaci sperimentali ha fatto diminuire i livelli di HIF‑1 nelle cellule mutate, lasciando però in gran parte intatta la risposta normale alla bassa ossigenazione. L'inibizione di PIM1 ha anche ridotto selettivamente l'espressione dei geni rischiosi della firma HIF1‑MPN‑BP e ha spinto le cellule mutate verso la morte cellulare, risparmiando le controparti non mutate.
Cosa significa per i pazienti
Questo lavoro dimostra che lo stesso proteina sensibile all'ossigeno, HIF‑1, si comporta in modo molto diverso a seconda di come viene attivata. Nelle neoplasie mieloproliferative guidate da JAK2V617F, un asse di segnalazione JAK2–PIM1 stabilizza HIF‑1 in modo da svincolarlo dal controllo normale dell'ossigeno e restringerne l'attività a un programma genico che promuove la malattia. Poiché questo programma alterato è strettamente legato alla gravità della malattia e al rischio di trasformazione, e può essere attenuato bloccando PIM1, offre una strada promettente per colpire l'attività maligna di HIF‑1 preservandone il ruolo essenziale nei tessuti sani. Terapie che sfruttino questa differenza potrebbero un giorno aiutare a prevenire che le neoplasie del sangue a lenta evoluzione precipitino in una leucemia potenzialmente letale.
Citazione: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
Parole chiave: neoplasie mieloproliferative, JAK2V617F, HIF-1, chinasi PIM1, trasformazione in fase blastica