Clear Sky Science · it
Un agonista solubile di Notch permette la maturazione degli ameloblasti umani e la formazione di tessuto simile allo smalto per la rigenerazione dentale
Perché riparare lo smalto è così difficile
Lo smalto, la lucida copertura bianca che riveste i nostri denti, è il materiale più duro del corpo umano—ma una volta distrutto, non si rigenera da solo. Più del 90 percento degli adulti presenta qualche perdita o danno dello smalto, eppure i nostri denti non hanno un meccanismo naturale per ricostruire questa armatura protettiva. Questo studio descrive un metodo per coltivare in laboratorio cellule umane produttrici di smalto, farle maturare completamente e persino indurle a depositare materiale minerale simile allo smalto in animali. Il lavoro apre una strada verso terapie future che un giorno potrebbero riparare i denti con tessuto vivente anziché con otturazioni e capsule.
Costruire lo smalto a partire dalle cellule staminali
Lo smalto è prodotto da cellule specializzate chiamate ameloblasti, che però muoiono dopo l’eruzione del dente attraverso le gengive. Senza di esse, i denti dell’adulto non possono formare nuovo smalto. I ricercatori hanno usato cellule staminali pluripotenti indotte umane—cellule adulte riprogrammate in uno stato flessibile e simile all’embrione—per creare “ameloblasti indotti”. In lavori precedenti queste cellule coltivate in laboratorio potevano iniziare ad assomigliare agli ameloblasti naturali ma si bloccavano prima di raggiungere la piena maturità, e funzionavano correttamente solo quando crescevano a stretto contatto con gli odontoblasti, le cellule che formano la dentina sottostante. Questo ha sollevato una domanda cruciale: cosa forniscono esattamente gli odontoblasti che gli ameloblasti necessitano per completare il loro sviluppo?
La conversazione mancante tra le cellule dentali
Per decodificare questo dialogo cellulare, il gruppo ha analizzato mappe di espressione genica a singola cellula provenienti da denti umani e murini in sviluppo. Hanno cercato le vie di segnalazione che sembravano andare specificamente dagli odontoblasti agli ameloblasti durante la finestra chiave in cui si forma lo smalto. Una via è emersa con chiarezza: Notch, un sistema di comunicazione cellula‑a‑cellula usato diffusamente nello sviluppo embrionale. In queste mappe dentali, i ligandi di tipo Delta (in particolare DLL1 e DLL4) erano principalmente presenti sugli odontoblasti, mentre i recettori Notch si concentravano sugli ameloblasti in maturazione. Quando i ricercatori bloccarono l’attività di Notch con un farmaco nel loro sistema di co‑coltura, gli ameloblasti ridussero drasticamente la produzione di enamelina, una proteina chiave dello smalto—una forte evidenza che la segnalazione Notch è essenziale perché le cellule produttrici di smalto completino la loro maturazione. 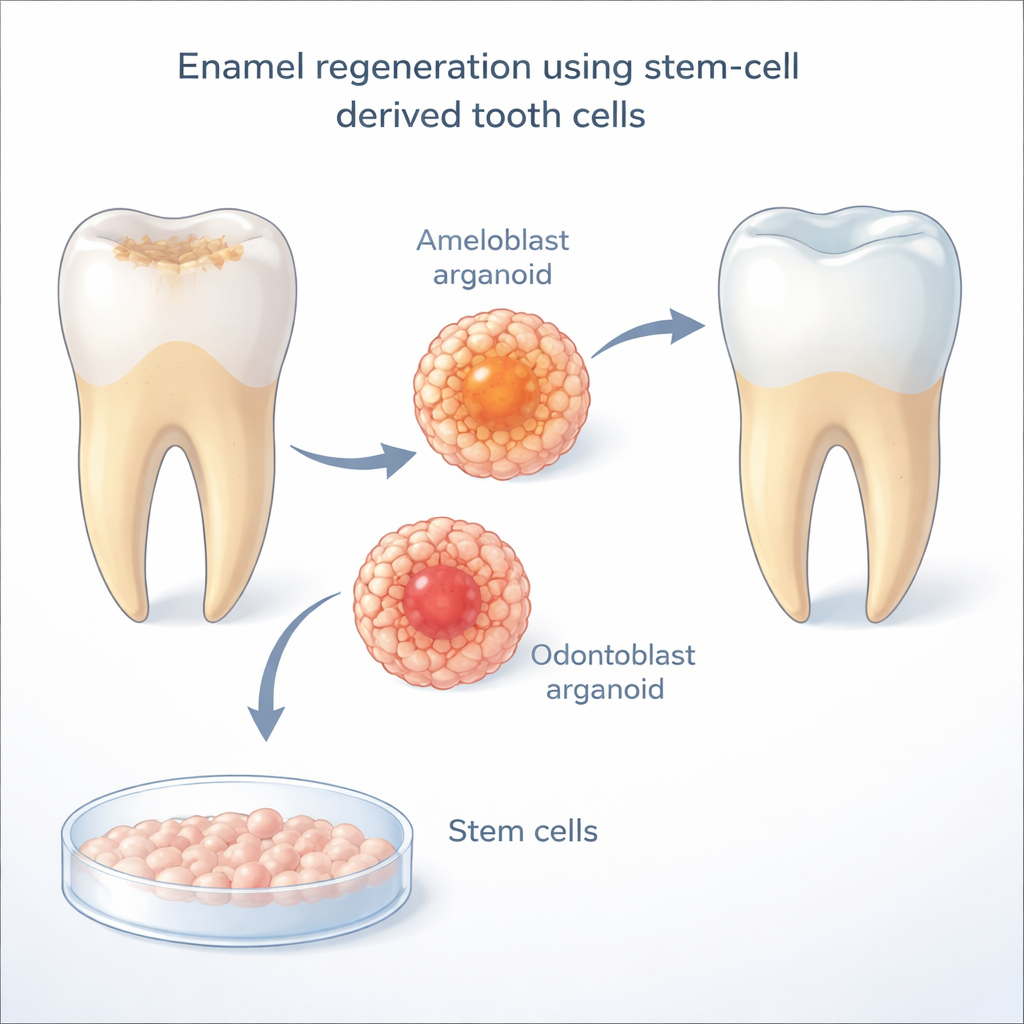
Un interruttore proteico progettato con l’AI per le cellule dello smalto
Per andare oltre, il team voleva attivare Notch in modo preciso e controllabile, senza dipendere da odontoblasti reali. Hanno usato una proteina artificiale chiamata C3‑DLL4, progettata con strumenti computazionali. Questa molecola solubile dispone tre copie del dominio di segnalazione DLL4 in uno impalcatura rigida a tre bracci, permettendole di raggruppare e attivare i recettori Notch sulle cellule vicine proprio come farebbe una cellula adiacente naturale. In linee cellulari reporter, C3‑DLL4 ha fortemente attivato i geni dipendenti da Notch. Quando è stata aggiunta a organoidi di ameloblasti in fase precoce—piccoli aggregati 3D di cellule derivati da staminali—ha indotto un profondo cambiamento nell’attività genica. Gli organoidi sono passati da un profilo immaturo a uno corrispondente agli ameloblasti secernenti e pienamente maturi, accendendo geni caratteristici quali AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 e WDR72. L’abolizione dell’attività di Notch ha avuto l’effetto opposto, bloccando la maturazione e perturbando la produzione delle proteine dello smalto.
Dagli organoidi a un tessuto simile allo smalto
In modo sorprendente, quando questi organoidi di ameloblasti attivati tramite Notch sono stati trapiantati sotto la capsula renale di topi immunodeficienti—un nicchia sicura e ben vascolarizzata spesso usata per testare tessuti umani—hanno iniziato a depositare materiale denso e mineralizzato. Tomografie micro‑CT ad alta risoluzione e tecniche classiche di colorazione per tessuti calcificati hanno confermato la presenza di noduli calcificati dove normalmente tale tessuto non si forma. La microscopia ha mostrato strati organizzati e polarizzati di cellule umane che esprimevano proteine chiave dello smalto e WDR72, un fattore legato alla corretta mineralizzazione dello smalto. Sebbene questo materiale sia meglio descritto come “simile allo smalto” piuttosto che smalto naturale completo, dimostra che ameloblasti umani ingegnerizzati possono, in linea di principio, depositare minerale duro in un organismo vivente. 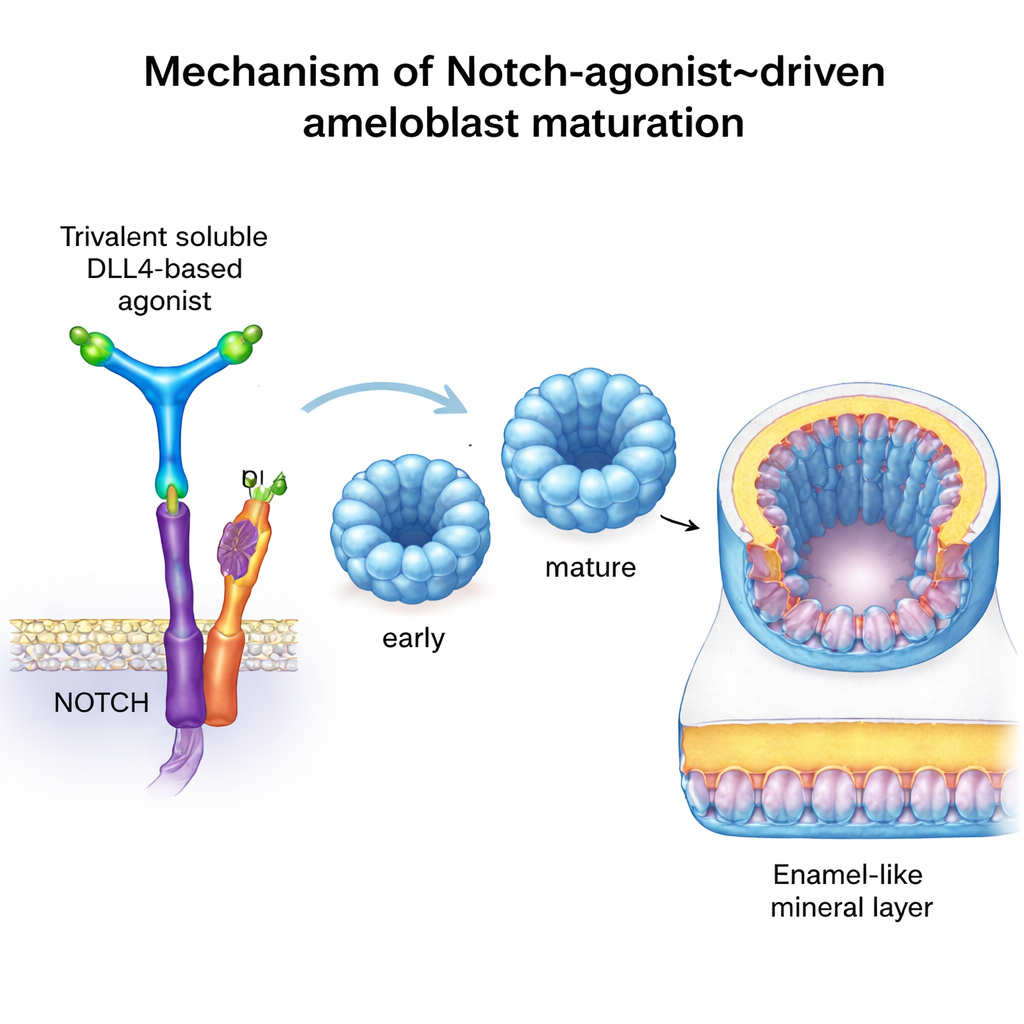
Svelare un mistero genetico alla base dello smalto fragile
Lo studio affronta anche un enigma di lunga data intorno al gene DLX3, le cui mutazioni causano certi difetti ereditari dello smalto e aumentano il rischio di carie. DLX3 è attivo sia negli ameloblasti sia negli odontoblasti, rendendo difficile capire quale tipo cellulare sia maggiormente responsabile quando qualcosa va storto. Usando il loro sistema di organoidi privo di odontoblasti e l’editing genetico CRISPR, i ricercatori hanno rimosso DLX3 specificamente nella linea degli ameloblasti. I primi passi della formazione degli ameloblasti si sono comunque verificati, ma la fase finale di maturazione è crollata: proteine chiave dello smalto come enamelina, AMELX, MMP20, KLK4, TUFT1 e WDR72 sono risultate drasticamente ridotte sia a livello di RNA sia di proteina. Questo dimostra che DLX3 è richiesto direttamente all’interno degli ameloblasti umani per completare il programma di formazione dello smalto, aiutando a spiegare perché varianti vicino a questo gene sono associate a denti fragili e più predisposti alle carie.
Cosa potrebbe significare per la cura dentale futura
Complessivamente, questi risultati delineano una mappa passo‑dopo‑passo dalle cellule staminali agli organoidi produttori di smalto fino a tessuto simile allo smalto in vivo, controllata da un “interruttore” Notch regolabile e dal gene DLX3. Sebbene la rigenerazione clinica del dente sia ancora lontana, questo lavoro fornisce un potente banco di prova per comprendere le malattie dentali genetiche, testare nuovi trattamenti e perfezionare strategie per ricostruire lo smalto perduto con cellule viventi anziché materiali inerti. Per i pazienti, l’obiettivo a lungo termine è che una visita dal dentista un giorno possa prevedere la riparazione di denti consumati o cariati con smalto bioingegnerizzato che si comporti molto più come quello naturale.
Citazione: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Parole chiave: rigenerazione dello smalto, organoidi di ameloblasti, segnalazione Notch, DLX3, cellule staminali dentali