Clear Sky Science · it
L’impianto risveglia il potenziale osteogenico peri-impianto tramite la trasduzione meccanica mediata dall’asse Snx5–EGFR
Perché è importante mantenere l’osso mascellare dopo la perdita di un dente
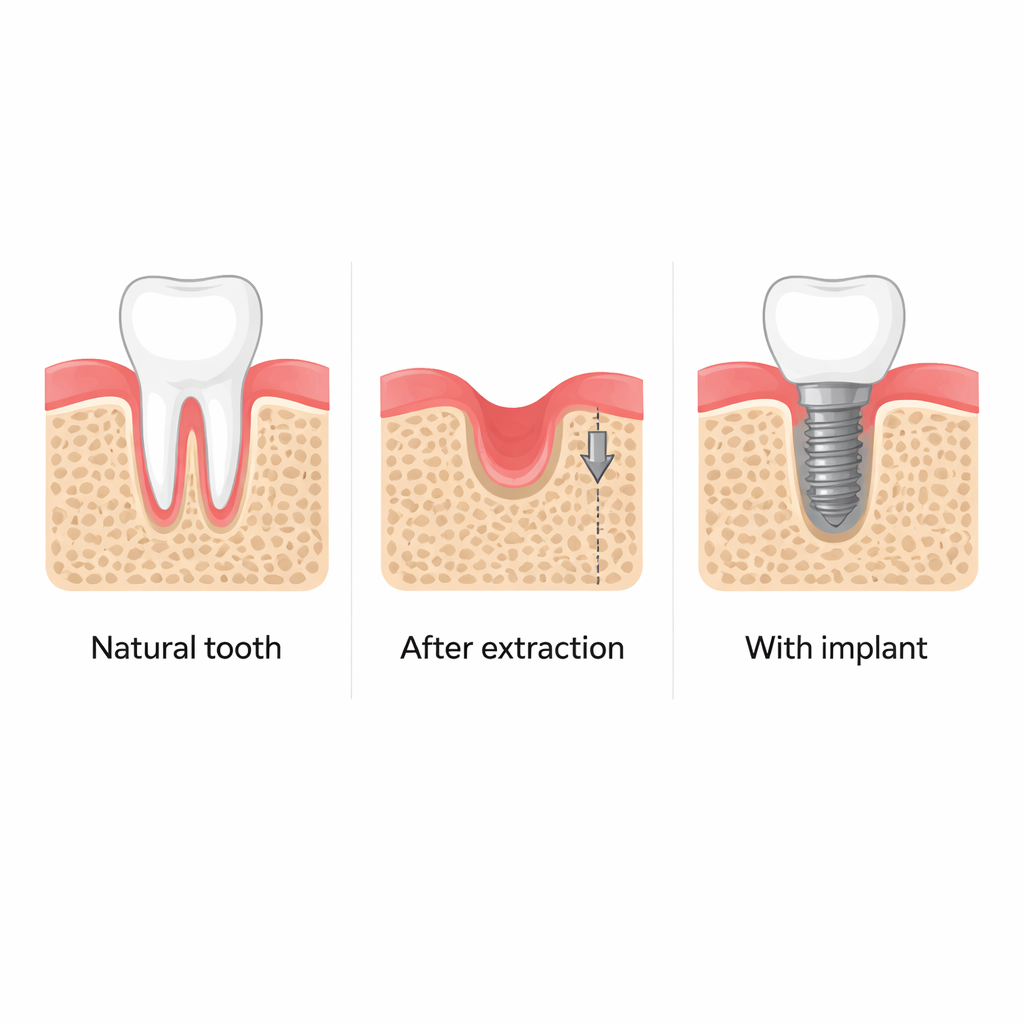
Quando un dente viene estratto, l’osso mascellare circostante tende spesso a riassorbirsi, rendendo più difficile posizionare in seguito impianti dentali stabili e influenzando l’aspetto del volto. I dentisti hanno da tempo notato che inserire semplicemente un impianto in una cavità fresca sembra contribuire a preservare questo osso, anche prima che l’impianto venga utilizzato per masticare. Questo studio pone una domanda semplice ma importante: in che modo l’atto stesso del posizionamento dell’impianto «risveglia» il sistema di riparazione dell’osso, e possiamo sfruttare questo processo per migliorare la rigenerazione dell’osso mascellare?
Gli impianti come discreti protettori dell’osso
Scansioni cliniche di pazienti e esperimenti dettagliati sui topi confermano che posizionare un impianto dentale poco dopo l’estrazione aiuta a mantenere l’altezza e lo spessore dell’osso circostante. Al contrario, le cavità lasciate guarire senza intervento perdono una quantità significativa di osso nel corso di alcuni mesi. Intorno agli impianti, i ricercatori hanno trovato più cellule immature produttrici di osso (osteoprogenitrici), il che indica che il tessuto vicino al perno metallico è biologicamente più attivo. Questa attività aumentata sembra essere guidata non dalle forze masticatorie, ma dagli insoliti stress meccanici creati dal serraggio di un impianto aderente in un osso leggermente sottodimensionato.
Un interruttore nascosto nelle cellule staminali ossee
Il gruppo si è concentrato su un gruppo speciale di cellule staminali del midollo osseo contrassegnate dalla proteina LepR, note per essere fornitori chiave di nuovo osso negli adulti. Confrontando l’attività genica in queste cellule provenienti da osso normale, osso adiacente a impianti e cellule sottoposte a stress in laboratorio, hanno individuato una molecola, il sorting nexin 5 (Snx5), i cui livelli calavano costantemente quando erano presenti segnali meccanici. Nelle regioni attorno agli impianti, le cellule LepR con basso Snx5 avevano maggior probabilità di esprimere marcatori di cellule in fase iniziale di formazione ossea, suggerendo che ridurre Snx5 aiuta a spingere queste cellule staminali «silenti» verso uno stato attivo di produzione ossea.
Quando l’interruttore è rotto, l’osso non percepisce correttamente la forza
Per verificare cosa faccia effettivamente Snx5, i ricercatori hanno usato topi e cellule staminali prive di questa proteina. Senza Snx5, le cellule staminali mostravano una forte tendenza intrinseca a formare osso, anche senza stimolazione aggiuntiva. Ma quando gli scienziati applicavano una trazione meccanica—mimando le deformazioni vicino a un impianto—le cellule normali aumentavano la loro attività osteogenica, mentre le cellule deficienti di Snx5 rispondevano a malapena. In topi vivi, gli impianti negli animali normali innescavano una chiara formazione di nuovo osso attorno al perno in titanio. Al contrario, i topi privi di Snx5 non accumulavano osso aggiuntivo dopo l’impianto, rivelando che Snx5 è cruciale per convertire i segnali meccanici in riparazione ossea aggiuntiva piuttosto che per la formazione ossea di base.
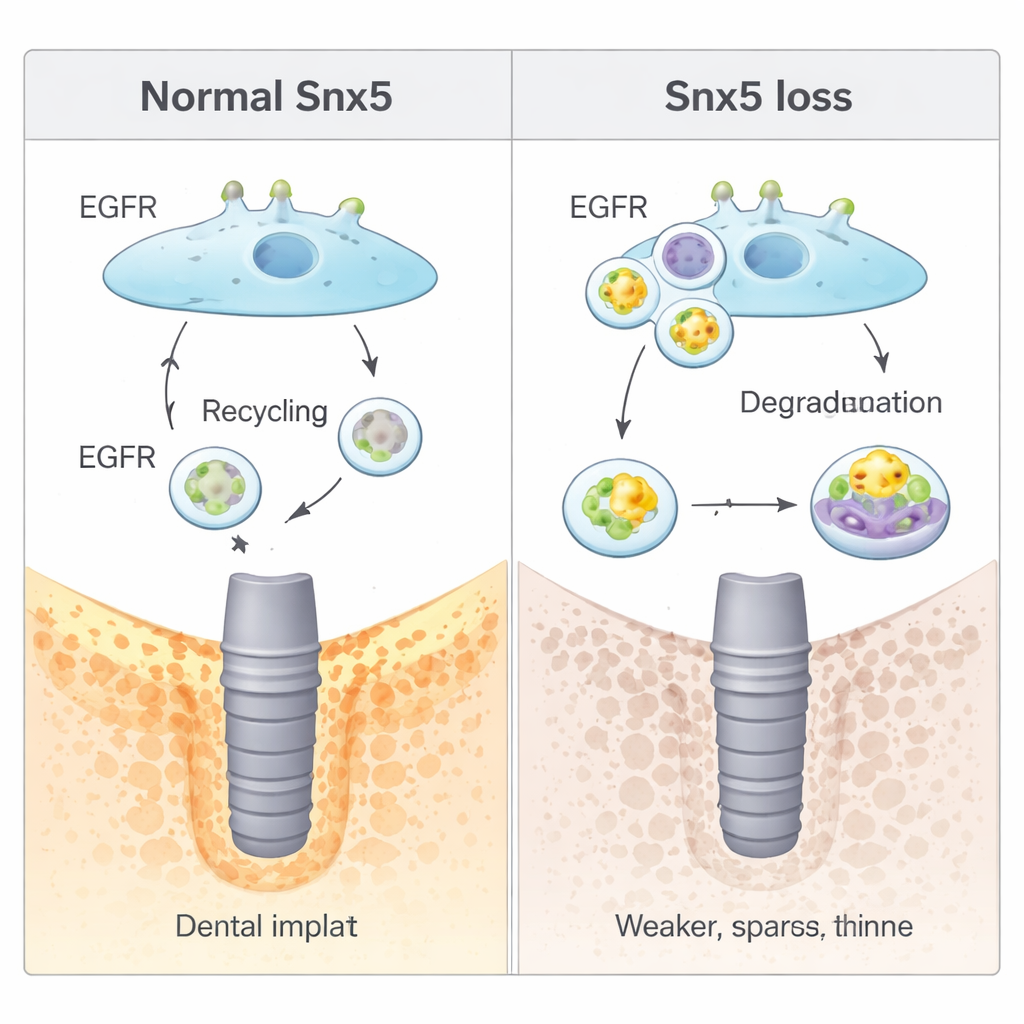
Come una via di riciclo controlla i segnali ossei
Lo studio ha poi chiarito come Snx5 operi a livello molecolare. Molti segnali di crescita nelle cellule transitano tramite recettori sulla superficie cellulare che vengono continuamente internalizzati e poi o riciclati o degradati. Snx5 appartiene a una famiglia di proteine di «smistamento» che guidano questo traffico. Qui, è stato dimostrato che Snx5 indirizza il recettore del fattore di crescita epidermico (EGFR)—un regolatore chiave della crescita cellulare e della differenziazione ossea—di nuovo verso la membrana cellulare dopo la sua internalizzazione. Quando Snx5 mancava, più EGFR veniva deviato verso compartimenti «digestivi» cellulari (lisosomi) e degradato. Questa ridotta segnalazione EGFR aumentava inaspettatamente la formazione ossea di base ma lasciava le cellule meno capaci di adattare il loro comportamento quando cambiavano le forze meccaniche. Farmaci che attivavano artificialmente EGFR attenuavano la formazione ossea supplementare osservata in assenza di Snx5, mentre farmaci che bloccavano la degradazione lisosomiale ripristinavano i segnali EGFR e riducevano di nuovo la formazione ossea.
Cosa significa questo per i pazienti futuri con impianti
Per un lettore non specialistico, questi risultati suggeriscono che l’osso mascellare contiene un sistema integrato in grado di percepire le sottili spinte e trazioni create quando si posiziona un impianto e di tradurle in crescita ossea aggiuntiva. Snx5 agisce come un controllore del traffico che mantiene il recettore di crescita chiave, EGFR, in un ciclo al livello giusto in modo che le cellule staminali ossee possano «udire» e rispondere a questi sussurri meccanici. Quando questo controllore è alterato, l’osso può formarsi più facilmente a riposo ma perde la capacità di risposta fine alle forze. Comprendere questo asse Snx5–EGFR apre la strada a nuovi trattamenti—farmaci o rivestimenti per superfici implantari—che potrebbero modulare la sensibilità meccanica dell’osso, aiutando a preservare l’osso mascellare e migliorare il successo degli impianti in situazioni cliniche difficili.
Citazione: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Parole chiave: impianti dentali, rigenerazione dell’osso mandibolare, meccano-trasduzione, cellule staminali ossee, segnalazione EGFR