Clear Sky Science · it
La via glicolitica KDM6B/Pdk1 che promuove la lattilazione di ZEB2 favorisce la formazione del cemento cellulare
Perché proteggere le radici dentali è importante
La malattia gengivale, o parodontite, è una delle principali cause di perdita dei denti negli adulti. Con il progredire della malattia, essa erode silenziosamente i tessuti che ancorano i denti alla mascella. Uno dei più importanti è il cemento, uno strato sottile e simile all’osso che ricopre la superficie delle radici e permette al dente di “fissarsi” al legamento e all’osso circostanti. Una volta perso il cemento, i denti si allentano e possono infine cadere. Questo studio pone una domanda semplice ma potente: possiamo capire, a livello molecolare, come viene costruito il cemento, in modo da poter un giorno aiutare il corpo a ricostruirlo e mantenere i denti al loro posto per tutta la vita?
Dalle cellule che supportano il dente a un bersaglio terapeutico
Il cemento è prodotto da cellule specializzate chiamate cementoblasti, che si trovano sulla superficie radicolare e depositano nuovo materiale minerale. Queste cellule si comportano in modo molto simile agli osteoblasti (cellule che formano l’osso), ma i segnali che indicano loro quando e come costruire il cemento erano poco noti. I ricercatori si sono concentrati su una molecola chiamata KDM6B, un enzima che modifica etichette chimiche sulle proteine che avvolgono il DNA e può attivare determinati geni. Studiando denti di topo a diverse età e cementoblasti coltivati in laboratorio, hanno osservato che i livelli di KDM6B aumentano durante la fase attiva di formazione del cemento e diminuiscono quando la crescita rallenta. Quando hanno bloccato KDM6B nelle cellule o nei topi, l’attività dei cementoblasti è calata e la parte “cellulare” del cemento — la porzione più spessa e vitale vicino all’apice radicolare — si è assottigliata, suggerendo che KDM6B è un promotore chiave della crescita sana del cemento.
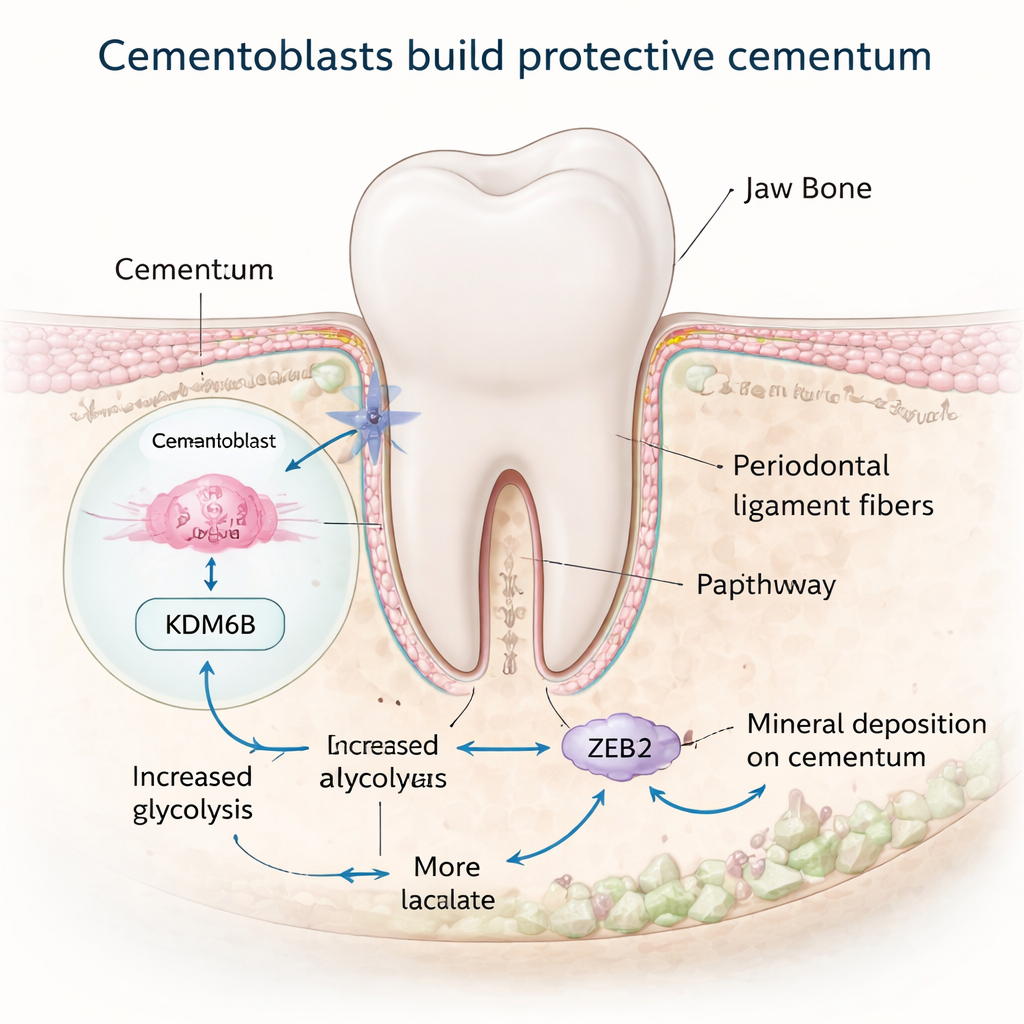
Rimodulare il metabolismo cellulare per costruire minerale
Costruire tessuto mineralizzato richiede molta energia, e molte cellule attivano uno stato metabolico particolarmente efficiente durante questo processo. Il gruppo ha scoperto che KDM6B aiuta i cementoblasti a rimodellare l’uso dello zucchero. Normalmente queste cellule privilegiano una via chiamata glicolisi, che scompone rapidamente il glucosio producendo lattato. Quando KDM6B è stato ridotto, i geni coinvolti nella glicolisi sono stati down-regolati, mentre quelli legati a vie energetiche più lente e dipendenti dall’ossigeno sono risultati misti o aumentati, e le cellule hanno prodotto meno energia complessiva. Un attore centrale in questo spostamento è stato l’enzima PDK1. Tramite strumenti di mappatura genomica, i ricercatori hanno mostrato che KDM6B rimuove fisicamente un marcatore repressivo dalla regione del DNA che controlla il gene Pdk1, permettendo così l’aumento di PDK1. Ripristinare PDK1 in cellule carenti di KDM6B ha riportato molti marcatori di formazione minerale, rivelando un interruttore metabolico KDM6B–PDK1 che alimenta i cementoblasti.
Trasformare il lattato da scarto a segnale utile
Il lattato è spesso considerato un prodotto di scarto dei muscoli sotto sforzo, ma studi recenti ne hanno evidenziato il ruolo come segnale che modifica le proteine. In questo lavoro, la maggiore glicolisi guidata da KDM6B e PDK1 ha aumentato la produzione di lattato nei cementoblasti. I ricercatori hanno quindi monitorato un nuovo tipo di modifica proteica chiamata lattilazione, in cui gruppi derivati dal lattato vengono attaccati a siti specifici delle proteine. Hanno rilevato che i livelli di lattilazione nei cementoblasti aumentano durante i periodi di attiva formazione del cemento e diminuiscono nei topi più anziani e nelle cellule carenti di KDM6B. L’aggiunta di semplice lattato di sodio al sistema ha aumentato la lattilazione, riattivato geni correlati alla mineralizzazione e ripristinato la formazione di noduli minerali sia nelle colture cellulari sia in un modello murino, anche quando KDM6B era bloccato. Questo suggerisce che il lattato stesso può contribuire a recuperare l’attività di costruzione del cemento indebolita.
Un potenziamento molecolare per un regolatore chiave del cemento
Il team si è poi chiesto quali proteine fossero “decorate” dal lattato in modo rilevante per il cemento. Hanno individuato ZEB2, una proteina regolatrice dei geni già nota per promuovere la mineralizzazione dei cementoblasti. Usando tecniche di mappatura delle proteine, hanno identificato siti specifici su ZEB2 che portano marchi di lattilazione e hanno dimostrato che la modifica di un sito critico indebolisce la capacità della cellula di attivare i geni della mineralizzazione. Ulteriori esperimenti hanno mostrato che la via KDM6B–PDK1 aumenta la lattilazione di ZEB2 e che fornire lattato extra può ripristinare l’attività di ZEB2 quando PDK1 è basso. In sostanza, metabolismo e controllo genico sono collegati: la degradazione dello zucchero alimenta la produzione di lattato, che poi modula finemente ZEB2 per mantenere attivi i programmi di formazione del cemento.
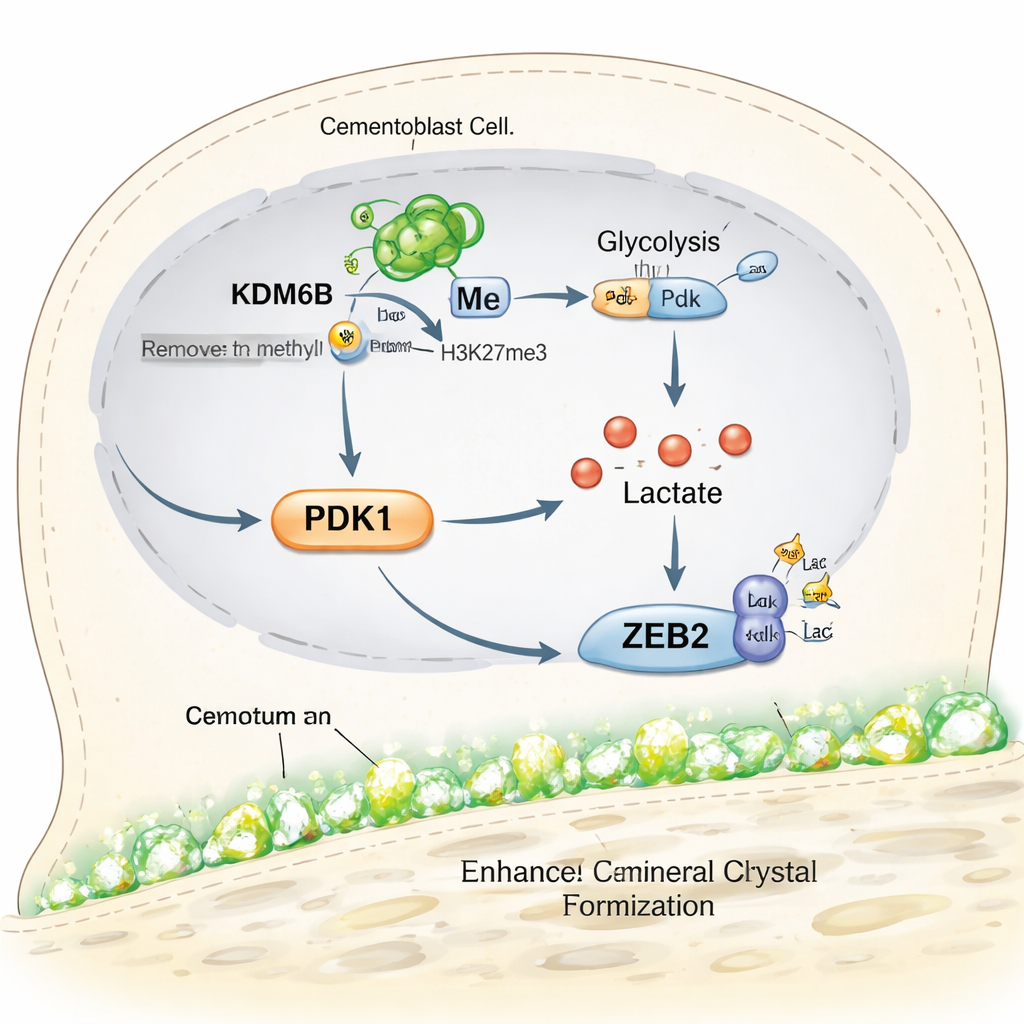
Implicazioni per future terapie che salvano i denti
In termini semplici, lo studio rivela una catena di eventi all’interno delle cellule che formano il cemento: l’enzima KDM6B apre il gene Pdk1, PDK1 spinge le cellule verso un rapido utilizzo degli zuccheri, quel metabolismo genera lattato e il lattato regola chimicamente la proteina ZEB2 per guidare il deposito minerale. Quando uno qualsiasi di questi passaggi è bloccato, la crescita del cemento rallenta, ma la reintegrazione mirata di lattato può in parte restaurarla. Per i pazienti, questo lavoro non si traduce ancora in un trattamento clinico, ma mette in luce nuovi bersagli precisi per farmaci o biomateriali progettati per rigenerare il cemento e stabilizzare i denti nelle fasi avanzate della malattia parodontale. Suggerisce inoltre che interruttori metabolici simili potrebbero essere sfruttati per favorire la guarigione ossea anche in altre parti del corpo.
Citazione: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Parole chiave: rigenerazione del cemento, parodontite, metabolismo dei cementoblasti, demetilasi istonica KDM6B, lattilazione proteica