Clear Sky Science · it
Approfondimenti strutturali sulle mutazioni associate a malattie nella macchina di processamento dei microRNA
Come minuscole forbici di RNA plasmano salute e malattia
All’interno di ogni cellula, un sistema di editing nascosto rifinisce i messaggi genetici prima che vengano letti. Questo sistema si basa su minuscoli frammenti di RNA chiamati microRNA, che agiscono come manopole di regolazione fine per migliaia di geni contemporaneamente. Quando le “macchine” molecolari che producono i microRNA funzionano correttamente, le cellule crescono, si dividono e si specializzano in modo controllato. Ma quando queste macchine sono danneggiate da mutazioni, l’equilibrio dell’attività genica può inclinarsi verso cancro, malattie del sangue o problemi nello sviluppo cerebrale. Questo articolo spiega come la comprensione delle forme tridimensionali di queste macchine aiuti gli scienziati a individuare cosa va storto e come ciò potrebbe essere corretto.
Il kit della cellula per attenuare i geni
I microRNA sono brevi pezzi di RNA, lunghi circa 22 monomeri, che non codificano proteine. Invece, si legano a RNA messaggeri più lunghi e ne segnano la distruzione o ne bloccano la traduzione, riducendo quindi l’espressione genica piuttosto che spegnerla del tutto. Per produrre questi microRNA, le cellule fanno passare precursor di RNA più lunghi attraverso una catena di montaggio attentamente scandita. Prima, l’enzima DROSHA taglia i trascritti primari ingombranti nel nucleo in pezzi più corti a forma di forcina. Questi pezzi poi migrano nel citoplasma, dove un altro enzima, DICER, misura e li taglia in duplex di dimensioni da microRNA. Infine, un filamento di ciascun duplex viene caricato in una proteina chiamata Argonaute 2 (AGO2), che usa il microRNA come guida per trovare messaggi corrispondenti e silenziarli. 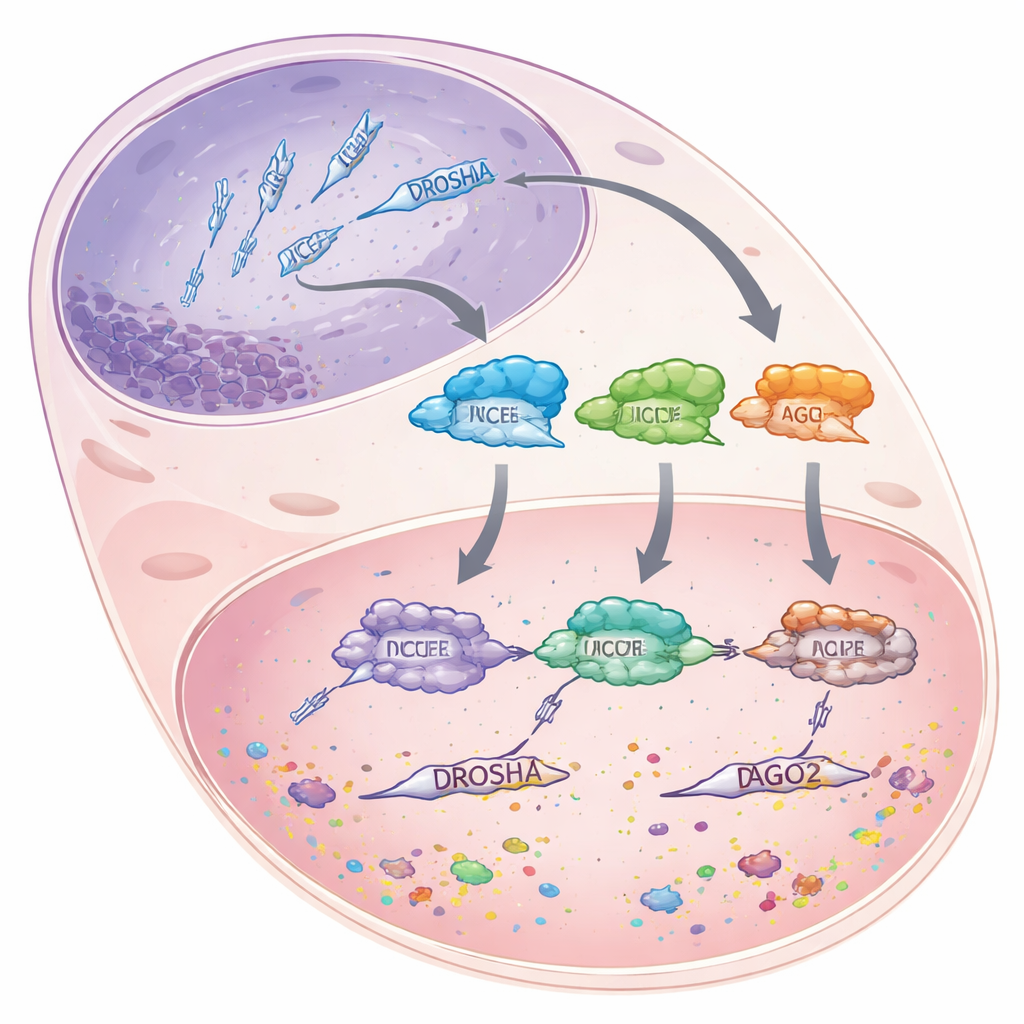
Forme delicate con compiti di precisione
DROSHA, DICER e AGO2 non sono semplici forbici; ciascuno è costruito da numerose parti interagenti che devono muoversi in modo coreografato. DROSHA lavora insieme a una proteina partner, DGCR8, per aggrappare le estremità di un forcina primaria e valutare esattamente dove tagliare. DICER usa una sorta di righello incorporato formato dai suoi domini per impostare una distanza fissa tra il punto in cui tiene l’estremità della forcina e dove il suo centro catalitico effettua il taglio. AGO2 avvolge un singolo filamento di microRNA in modo che la sua regione “seed” sia perfettamente esposta per riconoscere i messaggi bersaglio, mentre ioni metallici e aminoacidi chiave nel suo nucleo si allineano per sezionare quei bersagli quando l’appaiamento è sufficientemente forte. In tutti e tre le proteine, scanalature cariche positivamente e giunzioni flessibili guidano i filamenti di RNA al loro posto mentre tasche che legano metalli e residui catalitici eseguono i tagli chimici.
Quando le forbici sono piegate o smussate
Studi genetici in pazienti con cancro, malattie del sangue e sindromi neuroevolutive hanno scoperto ammassi di mutazioni in queste macchine dei microRNA. Molti dei cambiamenti più dannosi si trovano direttamente nei centri catalitici o nelle superfici che afferrano strettamente l’RNA. In DROSHA, per esempio, sostituzioni come E1147K e D1219G si collocano al cuore del sito di taglio e compromettono la capacità di trattenere ioni metallici essenziali, lasciando l’enzima incapace di processare i microRNA primari. Altre mutazioni di DROSHA, come troncamenti che rimuovono la regione di taglio o variazioni che destabilizzano le eliche di supporto, indeboliscono l’intero complesso e causano cali globali dei livelli di microRNA in tumori di Wilms, disordini del midollo osseo e malattie del sistema nervoso. In DICER, mutazioni ricorrenti si raggruppano in uno dei suoi due domini di taglio, alterando la produzione in modo che un braccio del duplex di microRNA venga perso, il che sposta l’equilibrio tra segnali che promuovono o sopprimono la crescita. 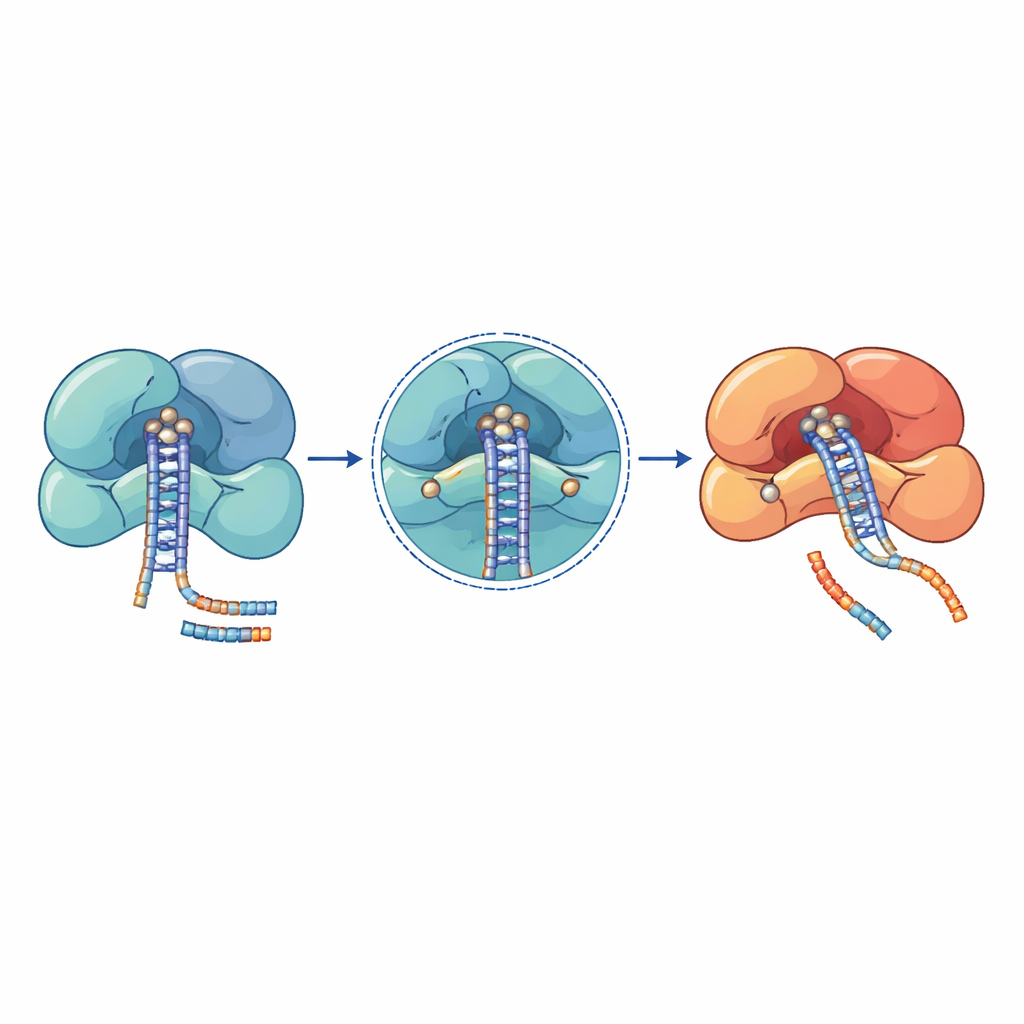
Guide disallineate nel cervello e oltre
Le mutazioni di AGO2 raccontano una storia diversa ma correlata. Colpi diretti al suo nucleo catalitico sono rari, probabilmente perché sarebbero letali precocemente nello sviluppo. Invece, le varianti legate a malattia tendono ad apparire in regioni linker flessibili e nelle giunzioni di dominio che tengono insieme la forma di AGO2. Nella sindrome di Lessel–Kreienkamp, una condizione neuroevolutiva, le mutazioni in questi linker e nelle superfici circostanti torcono sottilmente il modo in cui le parti PAZ, MID e PIWI di AGO2 si impacchettano e si muovono. Questo può disallineare la microRNA guida o indebolirne la presa sugli RNA bersaglio, sfocando la precisione del silenziamento genico durante lo sviluppo cerebrale. Cambiamenti strutturali simili in qualsiasi punto della via dei microRNA — sia in DROSHA, DICER o AGO2 — possono riverberare all’esterno, alterando intere reti geniche coinvolte nella crescita cellulare, nella formazione del sangue o nel cablaggio neuronale.
Trasformare indizi strutturali in trattamenti futuri
Sovrapponendo le mutazioni patologiche alle mappe 3D ad alta risoluzione di queste proteine, i ricercatori possono classificare esattamente come ogni cambiamento causa problemi — sia che renda meno affilato il bordo di taglio, allenti contatti critici con proteine partner o pieghi eliche chiave fuori allineamento. Questi approfondimenti strutturali aprono la porta a interventi mirati: piccole molecole che stabilizzano interfacce indebolite, RNA progettati che riportano enzimi parzialmente funzionali sui substrati corretti, o composti allosterici che spingono le proteine mutate verso conformazioni più attive. Per un lettore non specialista, il messaggio è che piccole modifiche strutturali nelle forbici di RNA della cellula possono avere effetti sproporzionati sulla salute, ma forniscono anche punti di presa molto precisi per progettare terapie di nuova generazione consapevoli della mutazione.
Citazione: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Parole chiave: microRNA, interferenza a RNA, DROSHA DICER AGO2, genetica del cancro, disturbi dello sviluppo neurologico