Clear Sky Science · it
Meccanismi regolatori per la stabilità della proteina Snail: sistema ubiquitina–proteasoma e autofagia mediata da chaperoni
Perché la diffusione del cancro dipende da una proteina fragile
Il cancro diventa veramente pericoloso quando le cellule si staccano dal tumore primario e raggiungono organi lontani. Questa diffusione, o metastasi, dipende in parte da una potente proteina “interruttore maestro” chiamata Snail, che aiuta le cellule ad allentare i loro legami e a diventare più mobili. Questo articolo spiega come le nostre cellule normalmente tengano Snail sotto stretto controllo smaltendola rapidamente tramite due principali sistemi di smaltimento. Comprendere questo equilibrio offre nuove idee per rallentare o prevenire le metastasi.
Dalle cellule strettamente compatte agli invasori vaganti
Nei tessuti sani, le cellule epiteliali formano strati ordinati, simili a mattoni, che restano al loro posto e aderiscono saldamente alle vicine. Per una cellula tumorale fuggire spesso è necessaria una trasformazione chiamata transizione epitelio–mesenchimale, o EMT, in cui perde i contatti stretti e acquisisce la capacità di muoversi e invadere. Snail è un driver chiave di questa trasformazione: quando è presente nel nucleo cellulare, spegne i geni che mantengono l’adesione cellula–cellula e attiva i geni che favoriscono movimento e invasione. Elevati livelli di Snail sono associati a tumori aggressivi e a scarsa prognosi; perciò le cellule hanno evoluto meccanismi per mantenere Snail raro e di breve durata in condizioni normali.
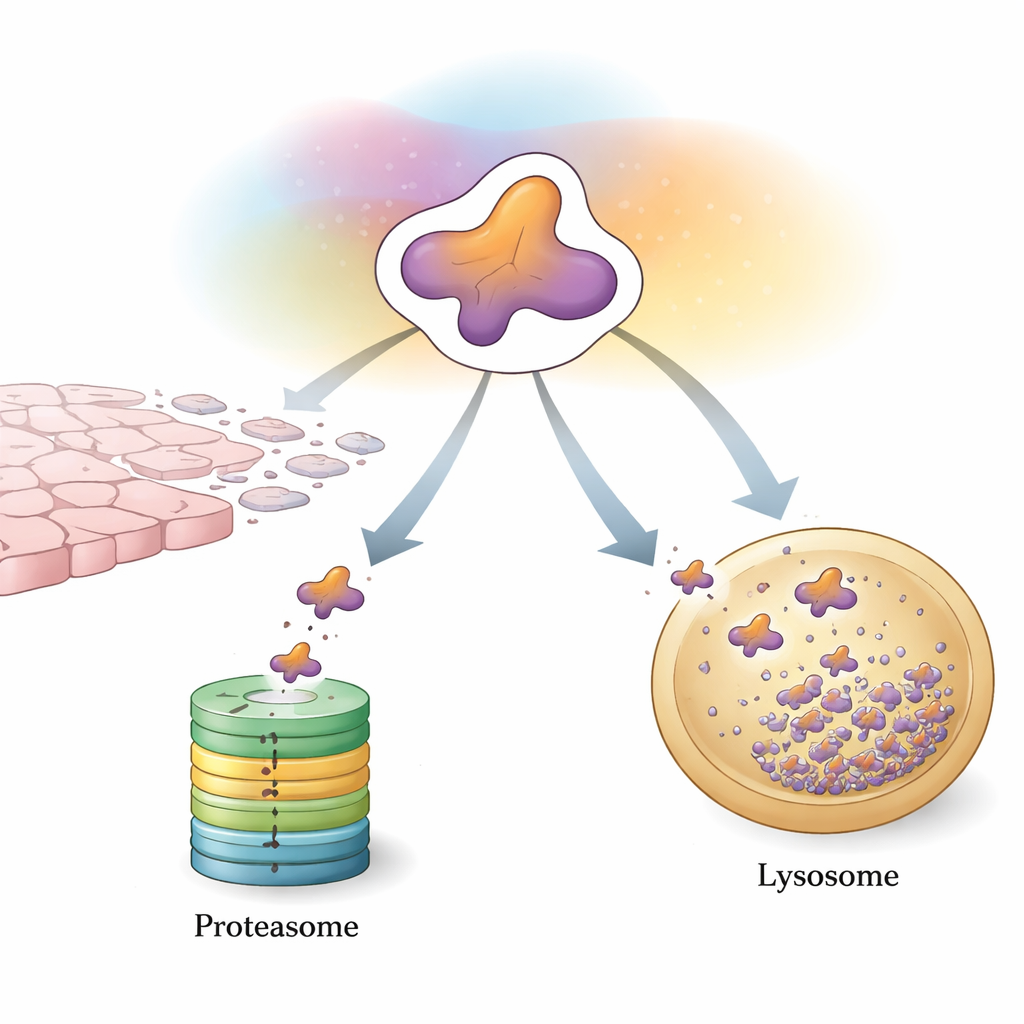
La prima linea di controllo della cellula: etichettare e frantumare
Un modo principale con cui le cellule controllano Snail è il sistema ubiquitina–proteasoma, una macchina che etichetta e sminuzza le proteine indesiderate. Enzimi specializzati attaccano piccoli “segnali” costituiti dalla proteina ubiquitina su Snail. Quando questi segnali si accumulano in un certo schema, Snail viene indirizzata verso il proteasoma, un complesso a forma di barile che la sminuzza in frammenti. Un ampio cast di proteine ausiliarie regola finemente questo processo. Alcuni enzimi aggiungono catene promuoventi la degradazione che inviano rapidamente Snail al trituratore, contribuendo a contenere crescita tumorale e diffusione. Altri invece aggiungono catene che stabilizzano Snail o ne aumentano indirettamente la produzione genica, spostando l’equilibrio verso EMT e metastasi. Modifiche chimiche come fosforilazione e acetilazione agiscono come interruttori aggiuntivi, controllando quali helper possono legarsi a Snail e se verrà distrutta o risparmiata.
Rimuovere i freni: enzimi che salvano Snail
La storia non finisce con l’etichettatura per la distruzione. Un altro gruppo di enzimi, chiamati deubiquitinasi, può rimuovere le bandierine di ubiquitina, salvando Snail dal proteasoma. Molte di queste deubiquitinasi sono attivate o potenziate nei tumori, permettendo a Snail di sfuggire alla degradazione e persistere nel nucleo. La loro azione dipende fortemente dal contesto cellulare: in alcune situazioni stabilizzano direttamente Snail, in altre influenzano la sua localizzazione o il modo in cui interagisce con proteine partner. Segnali provenienti da vie associate al cancro, come fattori di crescita e risposte allo stress, alimentano questa rete decidendo se Snail sarà rapidamente rimossa o libera di guidare il programma EMT.
Una seconda rete di sicurezza: consegna selettiva al centro di riciclo cellulare
Oltre al proteasoma, le cellule si affidano all’autofagia, un insieme di vie che trasportano proteine verso compartimenti acidi chiamati lisosomi per la degradazione. Questa rassegna mette in evidenza una forma altamente selettiva nota come autofagia mediata da chaperoni (CMA) come seconda via principale per il controllo di Snail. La CMA riconosce una breve sequenza all’interno di Snail e, con l’aiuto di proteine di scorta, consegna Snail citoplasmatica ai lisosomi per la distruzione. Nelle cellule di carcinoma mammario meno aggressive, questo sistema mantiene Snail per lo più fuori dal nucleo e soggetta alla rimozione lisosomiale. Nei tumori mammari più aggressivi e triplo negativi, Snail tende ad accumularsi nel nucleo e a eludere la CMA, rafforzando la sua capacità di innescare EMT e metastasi.
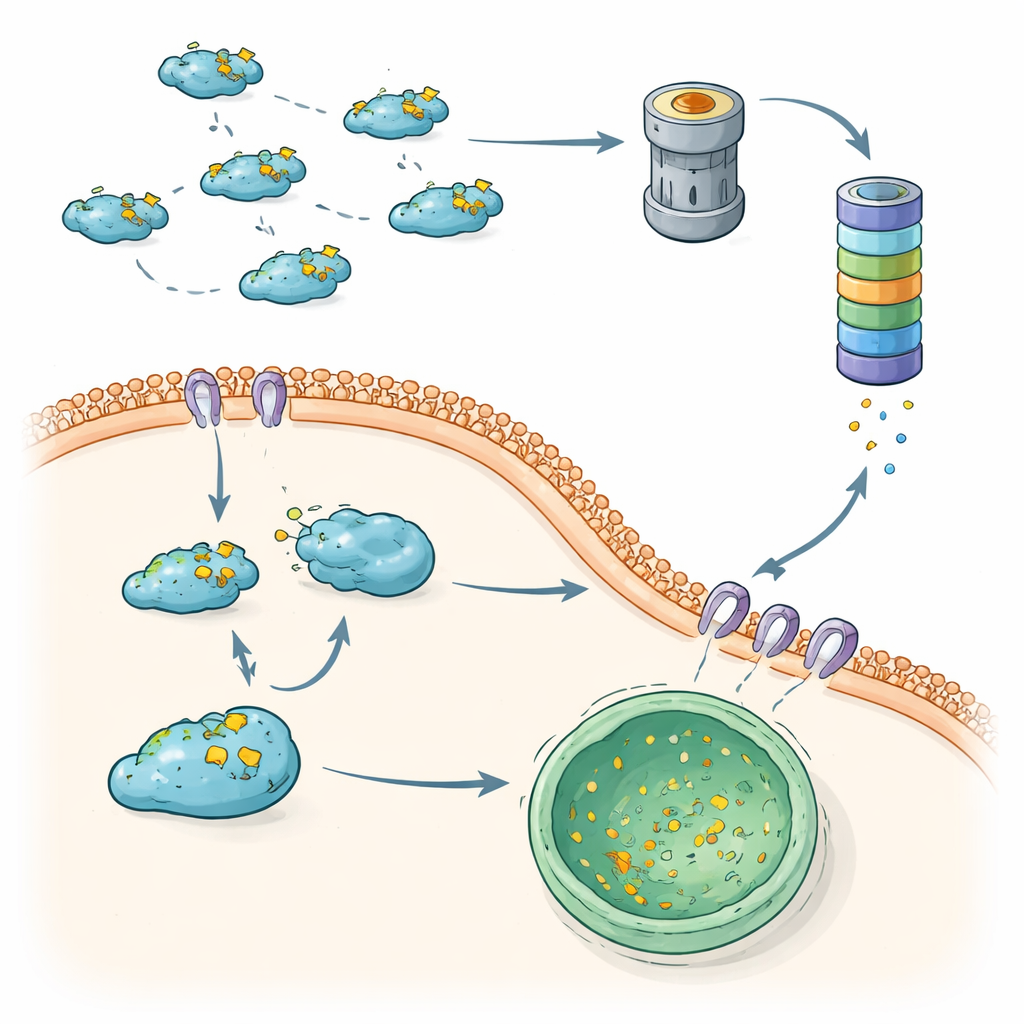
Quando il controllo qualità fallisce, la metastasi avanza
Considerati nel loro insieme, questi risultati rivelano che le cellule utilizzano due assi complementari di “controllo qualità” per contenere Snail: la via ubiquitina–proteasoma e la degradazione lisosomiale basata sulla CMA. Quando entrambi funzionano correttamente, Snail viene rapidamente riciclata, limitando l’EMT e aiutando a prevenire la diffusione delle cellule tumorali. Quando uno dei due assi è indebolito — tramite variazioni negli enzimi di etichettatura, nelle deubiquitinasi o nei componenti della CMA — Snail diventa più stabile, si accumula nel nucleo e promuove con forza comportamenti invasivi. Mappando queste vie intrecciate di degradazione, l’articolo delinea nuove possibilità terapeutiche: farmaci che ripristinino o potenzino la degradazione di Snail, o che la indirizzino nuovamente verso la CMA o la distruzione proteasomiale, potrebbero contribuire a rimettere i freni sulle metastasi senza bloccare completamente questi essenziali sistemi di riciclo proteico.
Citazione: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Parole chiave: metastasi del cancro, transizione epitelio–mesenchimale, proteina Snail, degradazione proteica, autofagia