Clear Sky Science · it
La carenza della componente dell’esocist Exoc5 aggrava la progressione della fibrosi renale
Perché la cicatrizzazione renale è importante
La malattia renale cronica colpisce centinaia di milioni di persone nel mondo, e una ragione principale per cui progredisce è la fibrosi: tessuto cicatriziale che sostituisce progressivamente il tessuto renale funzionante. Questo studio esplora una macchina cellulare meno nota, l’esocist e una delle sue subunità chiamata Exoc5, per porre una domanda pratica: questa proteina aiuta i reni a guarire correttamente dopo un danno, o li spinge verso la formazione di cicatrici e il fallimento?
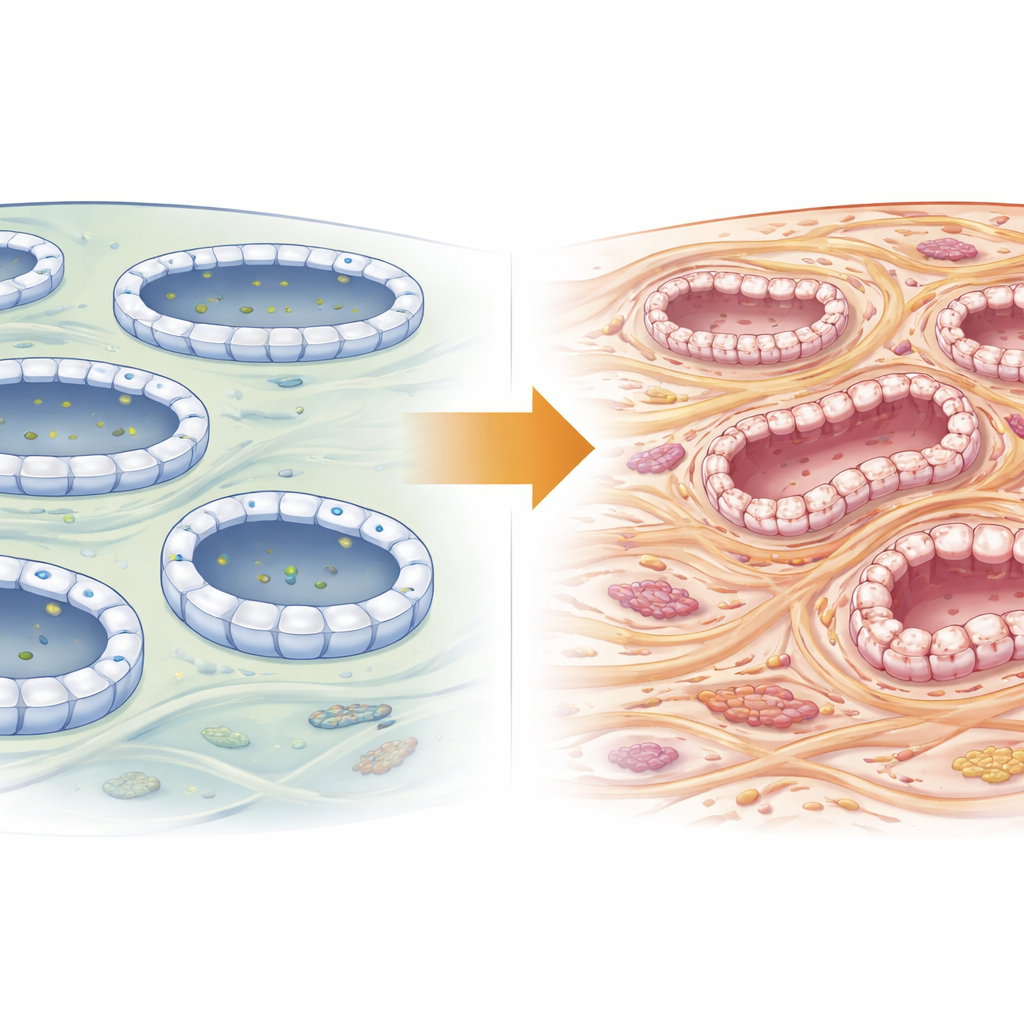
Un hub di smistamento cellulare nelle cellule tubulari renali
Ogni cellula del tubulo renale è un vivace centro logistico, che sposta costantemente piccole vescicole cariche di materiale verso punti precisi della sua superficie. Questo traffico è organizzato dall’esocist, un complesso di aggancio composto da otto parti. Exoc5 si trova al centro di questa macchina, collegando il carico che arriva dall’interno della cellula al sito di docking sulla membrana esterna. Lavori precedenti hanno mostrato che la perturbazione di Exoc5 danneggia vari organi e che esso aiuta le cellule del tubulo renale a mantenere la loro struttura stretta e ordinata. Poiché la perdita di tale struttura è una caratteristica della fibrosi, gli autori hanno ipotizzato che Exoc5 possa influenzare se i reni danneggiati si riprendono o sviluppano cicatrici.
Mettere alla prova il ruolo di Exoc5 nei reni dei topi
I ricercatori hanno generato topi nei quali Exoc5 è stato eliminato solo nelle cellule del tubulo prossimale—i segmenti che svolgono la maggior parte della filtrazione e del riassorbimento renale. Sorprendentemente, questi topi crescevano normalmente e presentavano struttura, localizzazione dei trasportatori e funzione renale normali in condizioni ordinarie. Per simulare un danno localizzato intenso che spesso porta a cicatrizzazione, il gruppo ha quindi legato un uretere, una procedura standard che causa accumulo di pressione, infiammazione e fibrosi nel rene interessato nell’arco di una settimana. In entrambi i gruppi, normali e privi di Exoc5, questa ostruzione ridusse i livelli di Exoc5, ma gli animali knockout svilupparono un restringimento tubulare molto più severo, accumulo di collagene e invasione da parte di cellule legate all’infiammazione.
Dai tubi ordinati alle cellule vaganti
Le cellule tubulari sane sono strettamente connesse, con superfici superiore e inferiore ben definite. Durante la fibrosi spesso subiscono una «transizione epitelio-mesenchimale» (EMT), uno spostamento da uno stato ancorato e a strato a uno più mobile e fibrillare. Gli autori hanno osservato che dopo l’ostruzione i reni privi di Exoc5 mostravano una più marcata attivazione dei principali promotori dell’EMT e livelli più elevati di proteine tipiche di cellule migranti e produttrici di matrice, insieme a una maggiore perdita di proteine di giunzione che normalmente mantengono la polarità delle cellule tubulari. Hanno inoltre riscontrato la ricomparsa di Pax2, un regolatore dello sviluppo normalmente spento una volta che i tubuli renali maturano. Pax2 riemerse in modo più pronunciato nei tubuli privi di Exoc5, in particolare nelle cellule stressate che non stavano dividendosi con successo, suggerendo che la perdita di Exoc5 spinge le cellule verso uno stato parzialmente riparato e dedifferenziato, incline alla formazione di cicatrici.
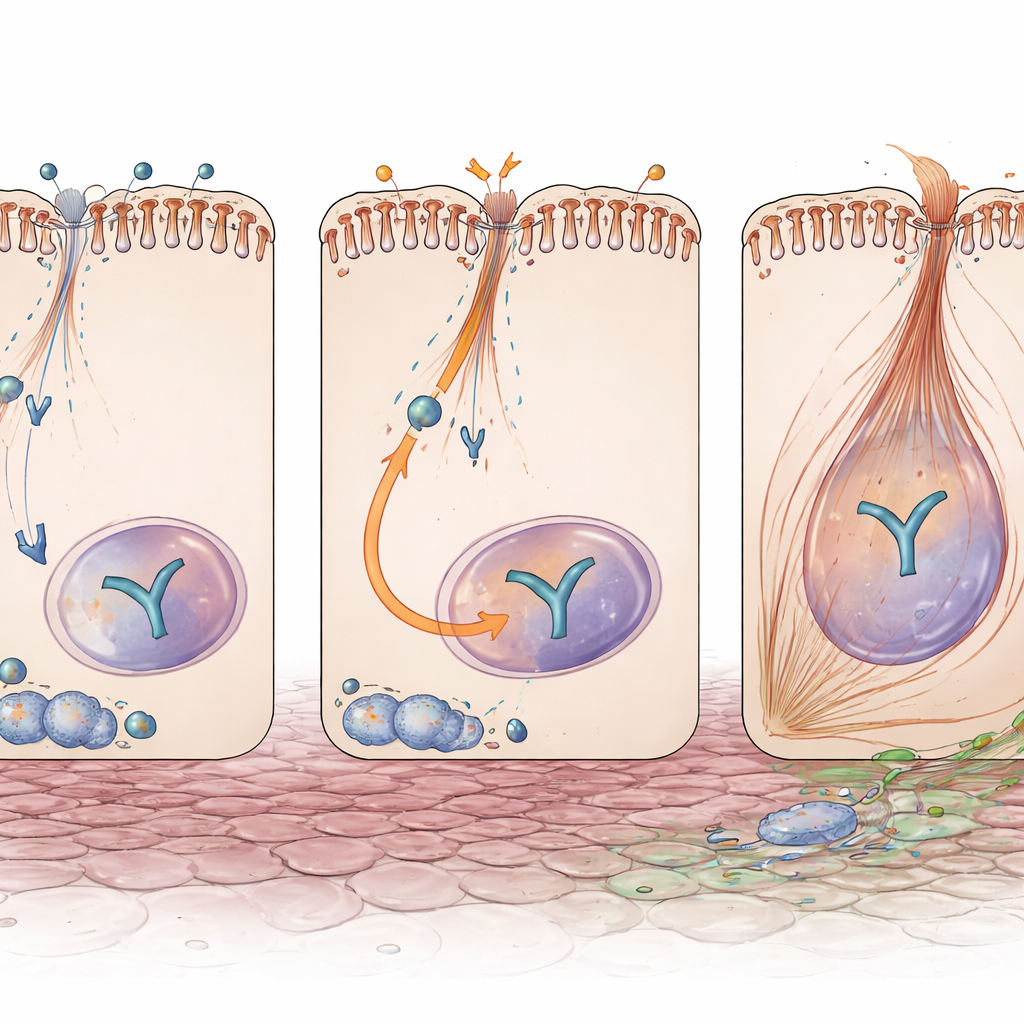
Un interruttore che collega danno e segnali di cicatrizzazione
Un altro attore centrale nella fibrosi è YAP, una proteina sensibile ai segnali che si sposta nel nucleo per attivare geni coinvolti nella crescita e nella produzione di matrice. Anche in assenza di danno, i tubuli privi di Exoc5 avevano livelli più alti di proteina YAP. Dopo l’ostruzione, YAP risultò più fortemente attivata e concentrata nei nuclei cellulari in questi reni, e i suoi prodotti a valle—molecole note per guidare il rimodellamento fibrotico—erano elevati. È importante che ciò non derivasse da una maggiore attività trascrizionale del gene YAP, implicando che Exoc5 normalmente frena YAP a livello di proteina o di traffico intracellulare. In cellule tubulari renali umane coltivate, ridurre EXOC5 mediante interferenza a RNA aumentò YAP e Pax2, e rese le cellule più reattive al segnale fibrotico TGF-β, con più marcati cambiamenti di tipo EMT e un numero maggiore di cellule che acquisivano fibre contrattili tipiche dei miofibroblasti.
Cosa significa per i trattamenti futuri
Nel complesso, i risultati descrivono Exoc5 come una guardia silenziosa: sotto stress aiuta le cellule tubulari a mantenere la loro identità organizzata e tiene sotto controllo segnali pro-cicatriziali come YAP e Pax2. Quando i livelli di Exoc5 diminuiscono—sia per perdita genetica sia per danno—le cellule tubulari perdono più facilmente la polarità, ricadono in uno stato simile allo sviluppo e alimentano il processo fibrotico. Poiché l’eliminazione di Exoc5 nei tubuli prossimali non danneggiò i reni sani ma peggiorò chiaramente la cicatrizzazione dopo il danno, il lavoro indica Exoc5 e i suoi partner di segnalazione come bersagli promettenti per terapie volte a rallentare o invertire la fibrosi renale prima che progredisca verso l’insufficienza renale.
Citazione: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Parole chiave: fibrosi renale, Exoc5, transizione epitelio-mesenchimale, segnalazione YAP, malattia renale cronica