Clear Sky Science · it
La supplementazione di L-aspartato corregge MASLD e MASH nei topi inibendo la frammentazione mitocondriale mediata dall’interazione piastrina–epatocita tramite l’asse ATP–P2X7–NEK7–DRP1
Perché questo studio sul fegato è importante
Molte persone accumulano grasso in eccesso nel fegato senza saperlo. Questo problema silenzioso, oggi chiamato steatosi epatica associata a disfunzione metabolica (MASLD), può progredire verso infiammazione grave, fibrosi e persino carcinoma epatocellulare. Il lavoro qui riassunto esplora se un semplice amminoacido naturale, l’L-aspartato, possa proteggere il fegato nei topi e mette in luce un colpevole inatteso nel danno epatico: piastrine iperattive che danneggiano le “centrali energetiche” delle cellule epatiche, i mitocondri.
Un problema epatico comune nella vita moderna
La MASLD è fortemente correlata all’obesità e al diabete di tipo 2 e potrebbe presto interessare più di un terzo della popolazione mondiale. Nella MASLD, le cellule epatiche si riempiono di grasso, vanno in stress e cominciano a morire, innescando infiammazione e formazione di tessuto cicatriziale. I mitocondri sani normalmente bruciano grassi e zuccheri per produrre energia, ma in questa malattia si danneggiano e si frammentano, per cui il fegato ossida meno grasso e ne accumula di più. Nonostante l’estensione del problema, finora è stato approvato un solo farmaco e aiuta solo una frazione dei pazienti, quindi i ricercatori cercano trattamenti sicuri ed economici che ripristinino la macchina energetica epatica.
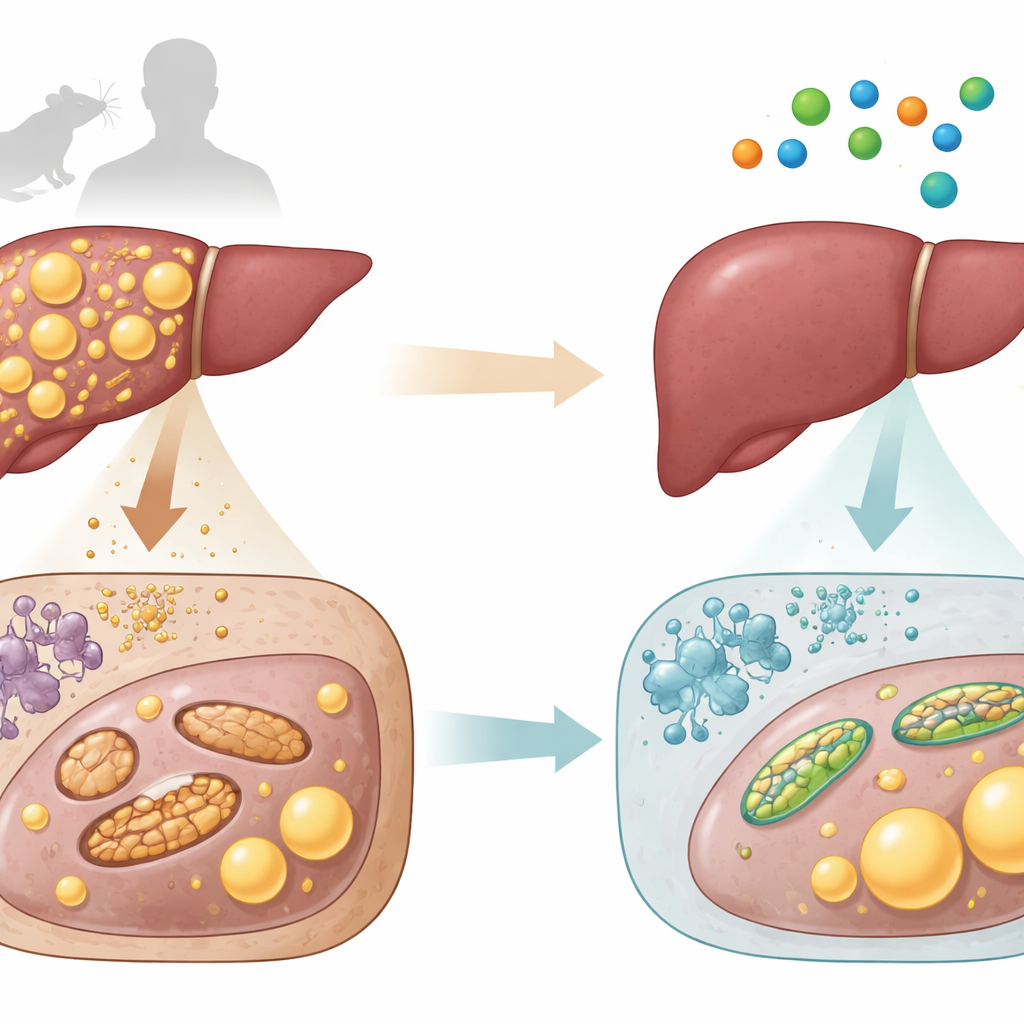
Un amminoacido semplice come possibile aiuto
L‑aspartato è un piccolo componente delle proteine che partecipa anche ai cicli energetici dell’organismo ed è già impiegato in ambito clinico come composto di supporto epatico. I ricercatori hanno prima misurato l’L‑aspartato in campioni di sangue e di fegato di topi e di persone. Hanno rilevato che animali e pazienti umani con fegati più grassi e più danneggiati presentavano livelli costantemente più bassi di L‑aspartato nel tessuto epatico. In entrambe le specie, meno L‑aspartato era associato a maggiore contenuto di grasso e a segnali più intensi di danno epatico. Questo schema suggeriva che la diminuzione dell’L‑aspartato potesse andare di pari passo con il peggioramento della salute epatica.
Invertire la steatosi e l’infiammazione nei topi
Il gruppo ha quindi chiesto se reintegrare L‑aspartato potesse effettivamente riparare la malattia. Hanno alimentato i topi con una dieta ricca di grassi e colesterolo o con una dieta speciale che provoca infiammazione epatica severa e fibrosi, riproducendo la MASLD umana e la sua forma avanzata, MASH. Quando questi topi hanno ricevuto iniezioni di L‑aspartato a dosi comparabili a quelle usate in clinica, i loro fegati sono diventati più chiari e meno untuosi, gli enzimi epatici nel sangue sono diminuiti e gli esami microscopici hanno mostrato meno goccioline di grasso, meno infiammazione e ridotta fibrosi. Questi benefici sono apparsi sia nella steatosi iniziale sia nella malattia infiammatoria avanzata e sono risultati confrontabili a quelli di farmaci di riferimento consolidati nei medesimi modelli.
Proteggere le “centrali” cellulari
Analizzando il fegato, gli scienziati hanno osservato che i topi malati avevano meno mitocondri, molti dei quali ingranditi e danneggiati o frammentati in piccoli pezzi. Il trattamento con L‑aspartato ha ripristinato una rete mitocondriale più sana e allungata. Ha aumentato l’attività di complessi enzimatici chiave per la produzione di energia, elevato l’utilizzo di ossigeno mitocondriale e la produzione di ATP, e incrementato i marker di “pulizia” e rinnovamento mitocondriale. Misure sull’intero animale hanno mostrato un consumo di ossigeno e una spesa energetica maggiori, indicando che i topi bruciavano più carburante nel complesso e non semplicemente mangiando meno.
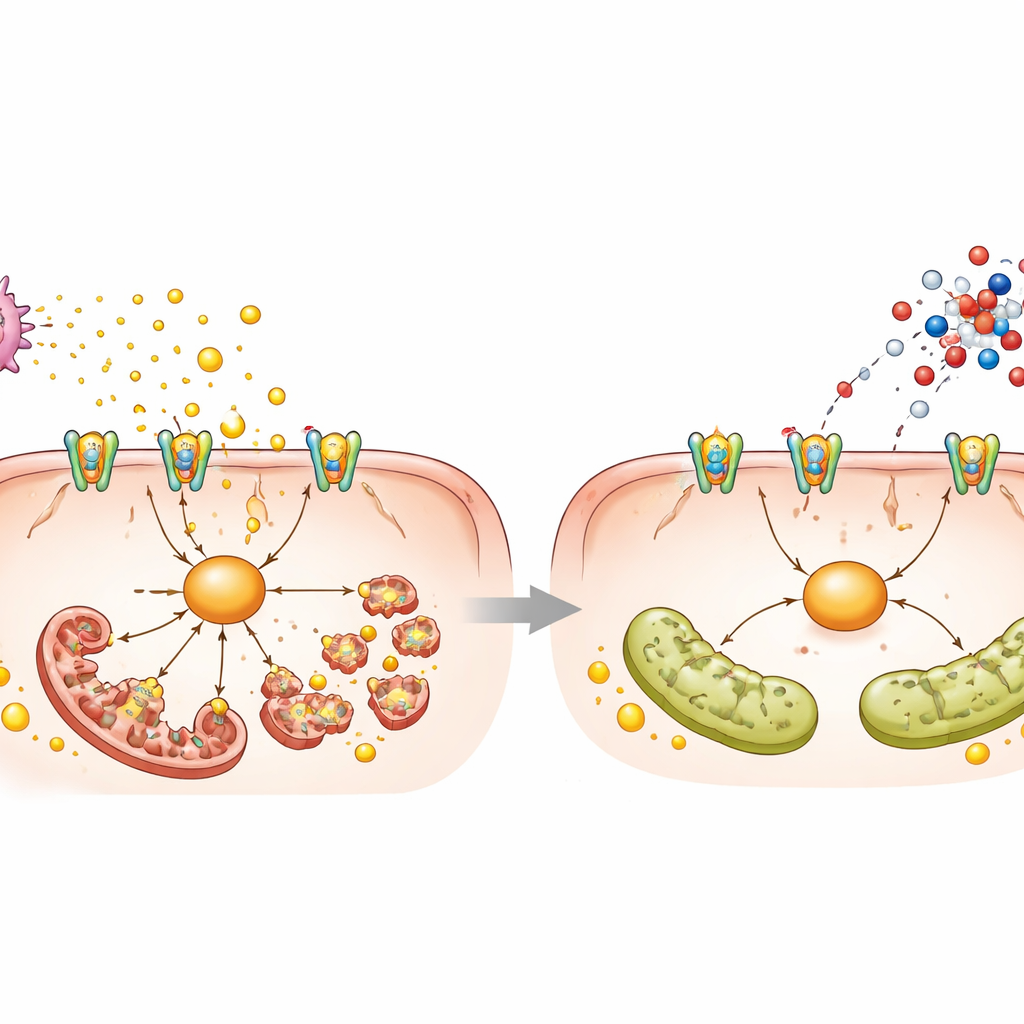
Piastrine, un segnale tossico e una catena molecolare
Per comprendere come l’L‑aspartato producesse questi effetti, i ricercatori hanno combinato l’analisi dell’attività genica e del profilo dei metaboliti dopo una singola dose. È emerso un segnale inatteso: vie correlate all’attivazione piastrinica e a una molecola messaggera chiamata cGMP. Nella steatosi, le piastrine nel sangue e nel fegato erano più numerose e attivate, e rilasciavano ATP in eccesso, una molecola energetica normale che diventa dannosa quando viene rilasciata all’esterno delle cellule. Questo ATP attivava un recettore chiamato P2X7 sulle cellule epatiche, che a sua volta attivava una proteina chiamata NEK7 e la proteina di fissione DRP1, inducendo la frammentazione dei mitocondri e promuovendo l’accumulo di grasso e la morte cellulare. L‑aspartato aumentava i livelli di cGMP all’interno delle piastrine, attenuava la loro attivazione e aggregazione, riduceva il rilascio di ATP e calmava questa catena P2X7–NEK7–DRP1 all’interno delle cellule epatiche. Bloccare direttamente le piastrine con aspirina, inibire P2X7 o silenziare NEK7 ha riprodotto molti degli effetti protettivi dell’L‑aspartato, sostenendo l’idea che il dialogo piastrina–fegato sia centrale nel danno.
Cosa potrebbe significare per i pazienti
Nel complesso, questi risultati suggeriscono che nella steatosi epatica le piastrine iperattive inondano il fegato di ATP, innescando una cascata molecolare che frantuma i mitocondri e aggrava l’accumulo di grasso e il danno. Nei topi, la supplementazione con L‑aspartato interrompe questo circolo: mantiene le piastrine più calme, limita il rilascio di ATP, preserva la forma e la funzione mitocondriale e inverte sia la steatosi semplice sia la malattia infiammatoria e fibrotica. Poiché l’L‑aspartato è economico e già impiegato come agente di supporto epatico, il lavoro lo identifica come un candidato promettente da testare nella MASLD e nella MASH umane, e al tempo stesso indica il danno mitocondriale guidato dalle piastrine come nuovo bersaglio per future terapie.
Citazione: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
Parole chiave: steatosi epatica, piastrine, mitocondri, L-aspartato, malattia metabolica del fegato