Clear Sky Science · it
Un circuito di retroazione positiva ESRP1/circPHGDH/miR-149/RAP1B promuove i comportamenti maligni e la glicolisi nelle cellule del cancro della prostata
Perché questa ricerca è importante per la salute degli uomini
Il cancro della prostata è uno dei tumori più comuni negli uomini, e molti tumori diventano alla fine aggressivi e resistenti alle terapie. Questo studio scopre un circuito di controllo nascosto all’interno delle cellule del cancro della prostata che le aiuta a crescere più rapidamente, a diffondersi più facilmente e a riorganizzare il modo in cui usano gli zuccheri per produrre energia. Mappando questo anello molecolare, i ricercatori evidenziano nuove vulnerabilità che potrebbero essere sfruttate per rallentare la malattia o rendere più efficaci le terapie esistenti.
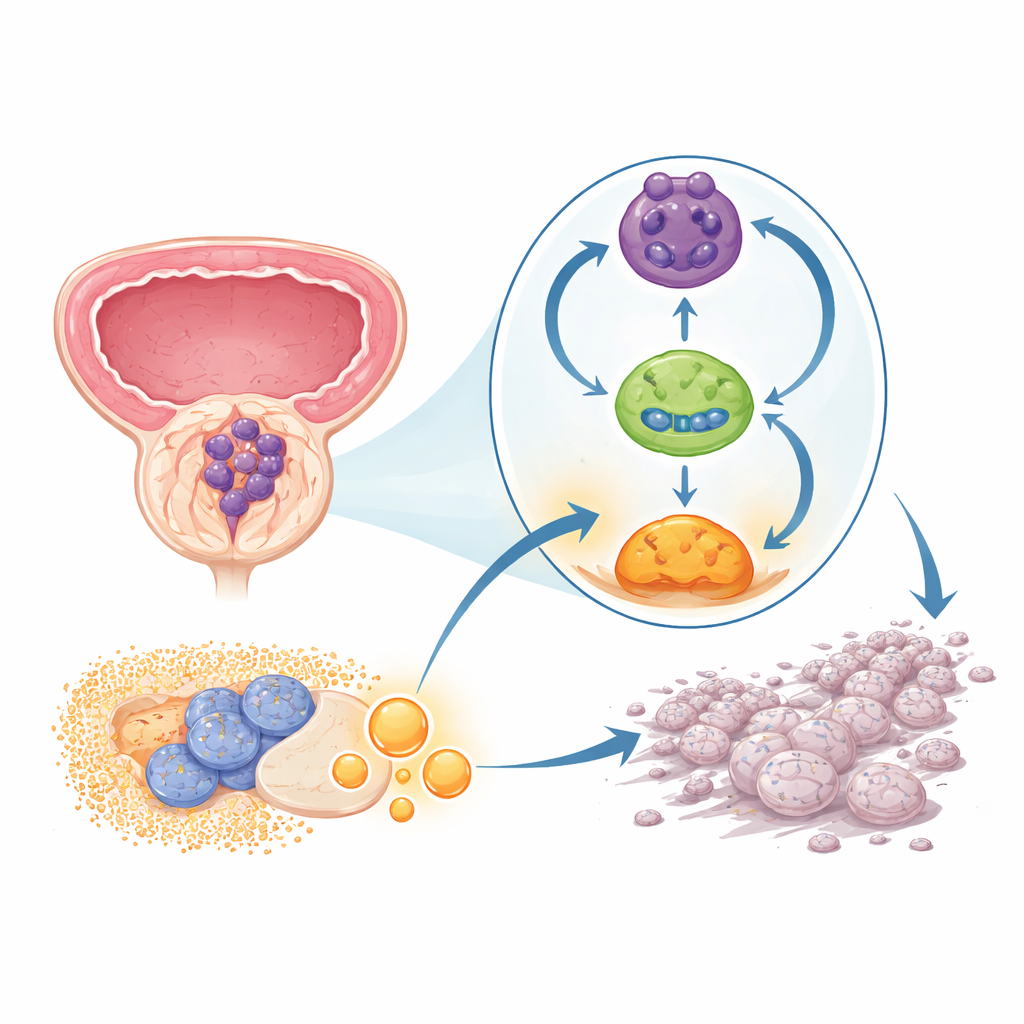
Un circuito nascosto che mantiene il cancro attivo
Il gruppo di ricerca si è concentrato su una classe di materiale genetico recentemente apprezzata: gli RNA circolari. Diversamente dai normali filamenti lineari, queste molecole formano anelli chiusi e sono particolarmente stabili. Nei campioni di tumore prostatico e nelle linee cellulari, i ricercatori hanno trovato che un particolare RNA circolare, chiamato circPHGDH, era costantemente più abbondante rispetto al tessuto non canceroso circostante. I pazienti i cui tumori presentavano livelli maggiori di questo RNA tendevano ad avere tumori più grandi, una crescita locale più avanzata e metastasi a distanza, suggerendo che circPHGDH contribuisca a una forma di malattia più pericolosa.
Come le cellule tumorali cambiano comportamento
Per capire cosa fa realmente circPHGDH, gli scienziati ne hanno modificato i livelli in cellule del cancro della prostata coltivate in laboratorio. Quando hanno ridotto circPHGDH, le cellule hanno formato meno colonie, si sono mosse e invadevano membrane con minore efficienza e hanno mostrato segni di mantenimento di uno stato più «epiteliale», meno incline alla diffusione. Allo stesso tempo, le cellule si sono allontanate dallo stile metabolico vorace di zuccheri tipico di molti tumori: la loro dipendenza dalla glicolisi è diminuita e hanno usato maggiormente la respirazione ossidativa. Quando circPHGDH è stato invece aumentato, tutti questi tratti promuoventi il cancro si sono mossi nella direzione opposta.
Piccoli RNA e una catena di segnale per la crescita
Lo studio ha quindi tracciato come circPHGDH eserciti questi effetti. Nel citoplasma della cellula, circPHGDH agisce come una spugna per un piccolo RNA regolatore chiamato miR-149, assorbendolo e impedendogli di reprimere i suoi bersagli abituali. Un bersaglio chiave è RAP1B, una proteina di segnalazione che alimenta una via di crescita e sopravvivenza nota per la sua importanza nel cancro della prostata. Quando miR-149 viene sequestrato da circPHGDH, i livelli di RAP1B aumentano e attivano segnali a valle che favoriscono la divisione cellulare, il movimento e un metabolismo fortemente basato sulla glicolisi. Ripristinare miR-149 o ridurre direttamente RAP1B ha invertito molti degli effetti dannosi, sia nelle colture cellulari sia in topi portatori di tumori prostatici umani.
Scarti metabolici che alimentano il circuito
Un altro livello della storia riguarda come circPHGDH viene prodotto. La sua formazione dipende da una proteina di splicing chiamata ESRP1, che contribuisce a decidere come i messaggi di RNA grezzi vengono tagliati e ricongiunti. I ricercatori hanno dimostrato che ESRP1 si lega a siti specifici intorno alla regione di circPHGDH e favorisce la sua forma circolare rispetto alla versione lineare standard. In modo cruciale, hanno scoperto che il lattato — prodotto finale della glicolisi — modifica chimicamente ESRP1 in un singolo sito, rendendo la proteina più stabile. Poiché circPHGDH stesso spinge le cellule verso una maggiore glicolisi e quindi verso una maggiore produzione di lattato, si crea un circuito auto‑rinforzante: ESRP1 aumenta circPHGDH, circPHGDH innalza RAP1B e la glicolisi, la glicolisi genera lattato e il lattato, a sua volta, stabilizza ESRP1.
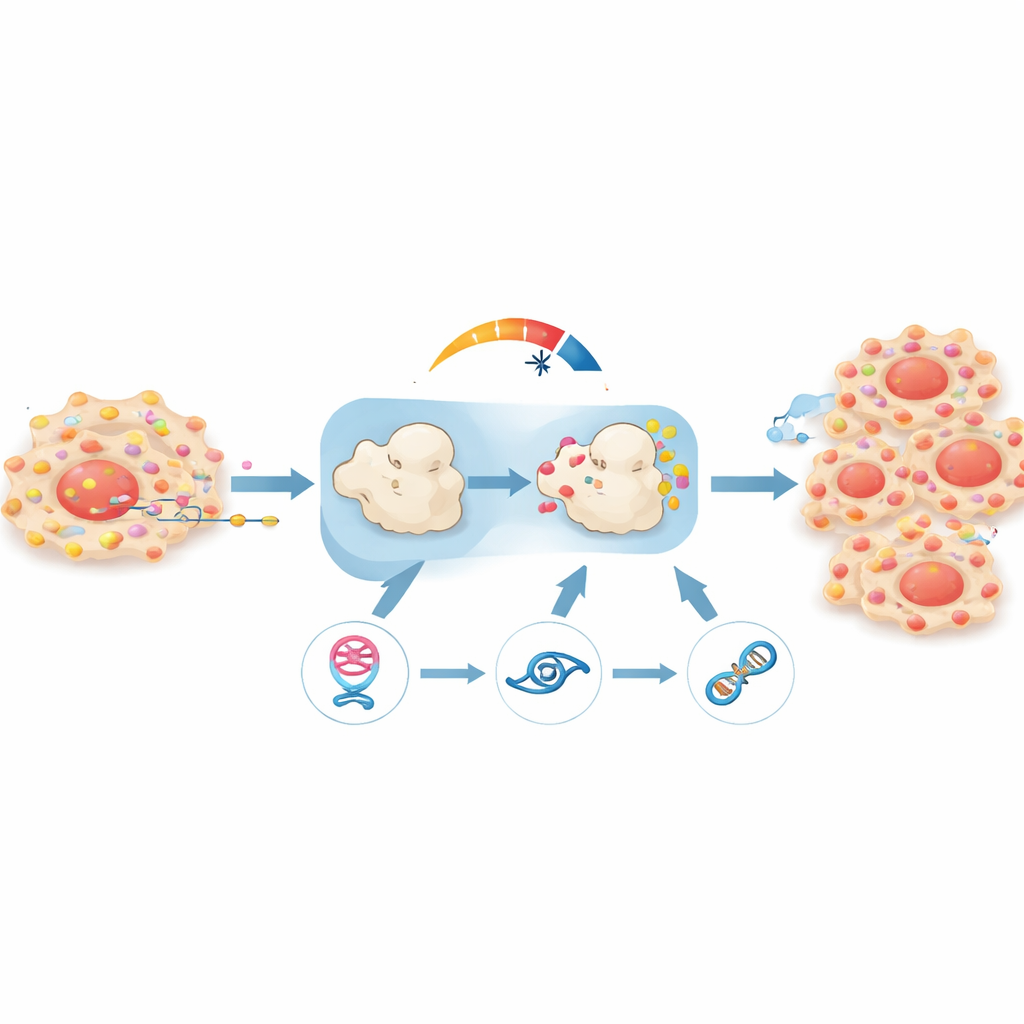
Prove da modelli animali
Per verificare se questo circuito conta davvero in un organismo vivente, il team ha impiantato cellule del cancro della prostata umano in topi. I tumori in cui circPHGDH era stato silenziato crescevano più lentamente, pesavano meno e mostravano meno segni di diffusione, come misurato dall’imaging dell’intero corpo e dall’analisi dei tessuti. I marcatori di proliferazione cellulare erano più bassi e la struttura del tumore appariva meno aggressiva al microscopio. Quando i ricercatori bloccarono miR-149 o riportarono RAP1B ai livelli precedenti in questi stessi tumori, gran parte della crescita e della diffusione è ricomparsa, confermando che la catena circPHGDH–miR-149–RAP1B è un motore centrale del comportamento della malattia.
Cosa significa per i trattamenti futuri
Complessivamente, i risultati rivelano un circuito di retroazione positiva in cui una proteina di splicing, un RNA circolare, un piccolo RNA regolatore e una proteina di segnalazione cooperano per spingere le cellule del cancro della prostata verso crescita rapida, invasione e metabolismo dipendente dagli zuccheri. Per i non specialisti, il messaggio chiave è che le cellule tumorali possono collegare i loro controlli genetici e metabolici in circuiti auto‑rinforzanti che mantengono la progressione della malattia. Interrompere questo circuito — bloccando circPHGDH, ripristinando miR-149, inibendo RAP1B o interferendo con la modificazione di ESRP1 dipendente dal lattato — offre diverse strade promettenti per farmaci futuri volti a rallentare o fermare il cancro della prostata aggressivo.
Citazione: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
Parole chiave: cancro della prostata, RNA circolare, metabolismo tumorale, microRNA, vie di segnalazione