Clear Sky Science · it
PAK4 nelle malattie metaboliche: regolazione dai segnali nutrizionali e implicazioni terapeutiche
Perché un interruttore cellulare conta per la salute quotidiana
L'obesità, il diabete di tipo 2 e la malattia del fegato grasso vengono spesso ridotti alle calorie, ma nelle profondità delle nostre cellule sono gli interruttori molecolari a decidere se bruciamo o immagazziniamo carburante. Questa rassegna si concentra su uno di questi interruttori, una proteina chiamata PAK4, e spiega come risponda ai segnali nutrizionali e ormonali variabili, rimodellando il metabolismo in tessuto adiposo, fegato e muscolo. Comprendere questo sistema di controllo nascosto potrebbe aprire la strada a nuovi trattamenti che affrontano più malattie metaboliche contemporaneamente anziché un sintomo alla volta. 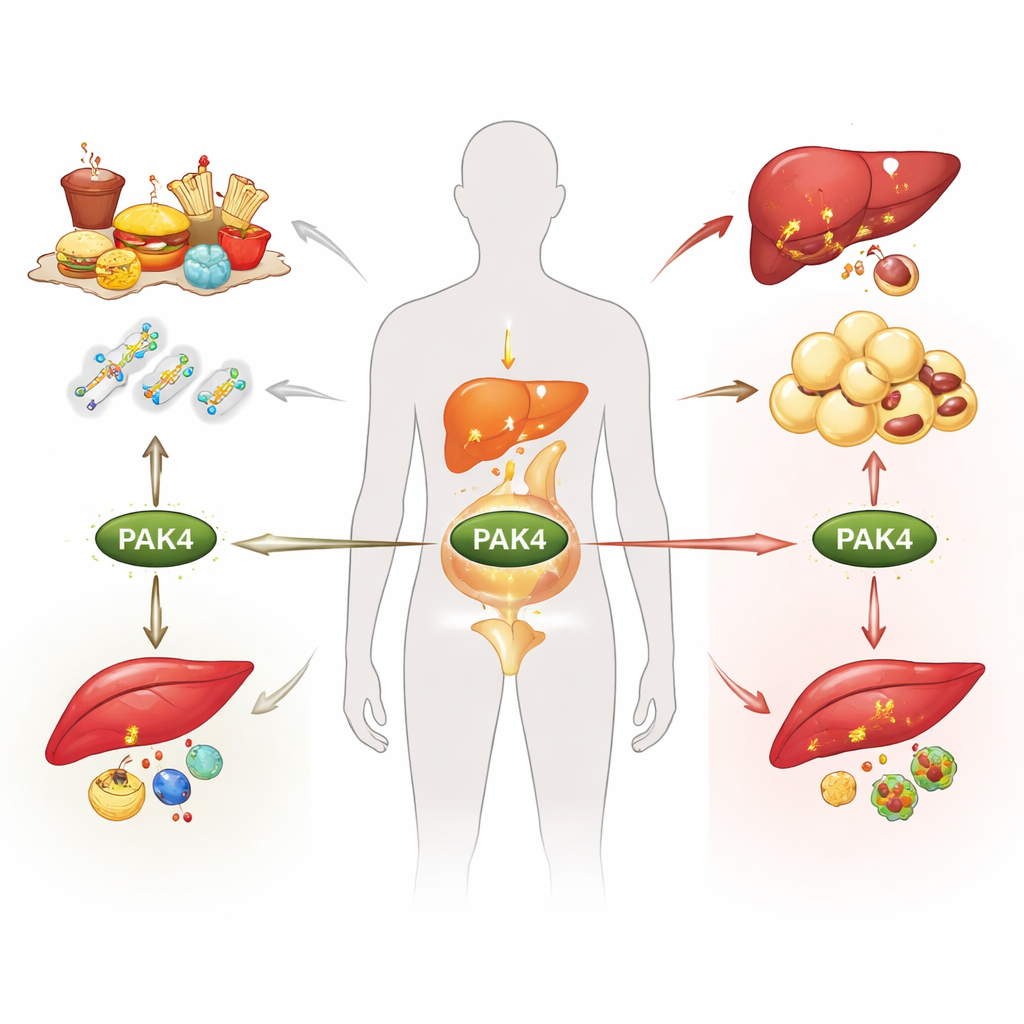
Un interruttore maestro nascosto nelle nostre cellule
PAK4 appartiene a una famiglia di enzimi che trasmettono segnali da piccoli “messaggeri” molecolari all’interno delle cellule. In condizioni di salute, PAK4 è presente a livelli bassi negli organi metabolici principali. Quando l’equilibrio energetico si altera, come nell’obesità o nel diabete di tipo 2, i suoi livelli aumentano nel tessuto adiposo, nel fegato e nel muscolo scheletrico. L’attività di PAK4 è controllata in diversi modi: da messaggeri a monte che ne modulano la conformazione e da tag chimici aggiunti o rimossi dopo la sintesi della proteina. Questi includono fosfati che possono attivare PAK4 o segnarlo per la degradazione, oltre a tag che ne influenzano stabilità o attività. Digiuno, alimentazione, ormoni e stress influenzano tutti questi tag, perciò PAK4 in pratica “sente” lo stato nutrizionale del corpo e trasmette quell’informazione a vie metaboliche chiave.
Come PAK4 spinge le cellule adipose verso l’accumulo
Nelle cellule adipose, PAK4 agisce come un freno sul consumo di grasso. Normalmente, quando digiuniamo o aumentano gli ormoni dello stress, un altro enzima chiamato PKA avvia la degradazione controllata dei depositi di grasso nelle piccole goccioline lipidiche. La rassegna descrive come PAK4 contrasti questo processo aggiungendo fosfati inibitori direttamente sulla lipasi sensibile agli ormoni e su una proteina legante acidi grassi che aiuta a trasportare i lipidi. Questi cambiamenti indeboliscono il macchinario che rilascia il grasso dallo stoccaggio. PAK4 sostiene anche la formazione di nuove cellule adipose nelle fasi precoci della vita aiutando proteine del ciclo cellulare a indirizzare le cellule precursori verso il destino di accumulo. Quando PAK4 viene eliminato o bloccato in modelli animali, gli adipociti bruciano più carburante, mostrano caratteristiche di “brunificazione” che aumentano il dispendio energetico, e gli animali risultano protetti dall’aumento di peso indotto dalla dieta. 
Il ruolo di PAK4 nel fegato grasso e nella gestione dello zucchero nel muscolo
Nel fegato, PAK4 favorisce ancora una volta l’accumulo rispetto alla degradazione. Durante il digiuno o con una dieta chetogenica, i livelli di PAK4 diminuiscono, permettendo alle cellule epatiche di aumentare la lipolisi e la produzione di corpi chetonici, che forniscono energia ad altri tessuti e possono persino rallentare la crescita tumorale. Quando PAK4 è abbondante, aggiunge residui fosfato a un corepressore nucleare che poi reprime PPARα, un regolatore principale dell’ossidazione dei grassi e della produzione di chetoni. Il risultato è più grasso intrappolato nel fegato e meno chetoni protettivi nel circolo sanguigno. Nel muscolo scheletrico, PAK4 interferisce con AMPK, un sensore energetico centrale che promuove sia l’assorbimento di glucosio sia l’attività mitocondriale. Modificando AMPK in modo da bloccarne l’attivazione, PAK4 riduce la quantità di trasportatore del glucosio sulla superficie delle cellule muscolari e contribuisce alla resistenza all’insulina. La perdita di PAK4 specifica nel muscolo nei topi inverte questi effetti, migliorando il controllo della glicemia anche in condizioni di obesità.
Stress, protezione e legami con altri interruttori cellulari
La rassegna mette in luce anche l’impatto di PAK4 oltre il metabolismo di tutti i giorni. Durante episodi di ridotto flusso ematico e successiva riperfusione in organi come il fegato, PAK4 indebolisce le difese antiossidanti taggando e destabilizzando Nrf2, un fattore chiave nella protezione dallo stress ossidativo. Allo stesso tempo, un altro membro della famiglia, PAK1, ricopre spesso ruoli più favorevoli nel muscolo cardiaco, nel muscolo scheletrico e nelle cellule pancreatiche che secernono insulina, contribuendo a mantenere un normale metabolismo del glucosio. Questo contrasto tra la segnalazione dannosa di PAK4 nelle malattie metaboliche e le azioni generalmente benefiche di PAK1 sottolinea l’esigenza di farmaci altamente selettivi che blocchino PAK4 senza interferire con proteine affini essenziali per la salute cardiaca e endocrina.
Trasformare una scoperta in terapia
Poiché PAK4 è iperattivo nel cancro e nei disturbi metabolici, i progettisti di farmaci hanno cercato piccole molecole in grado di bloccarne l’attività, nonché nuovi farmaci “degrader” che segnano lo stesso PAK4 per la rimozione. I primi composti bloccanti PAK4 hanno mostrato potenziale antitumorale ma hanno incontrato difficoltà di specificità e di comportamento farmacocinetico. Molecole più recenti, che mirano con maggiore precisione a PAK4, hanno prodotto risultati notevoli in topi obesi: peso corporeo ridotto senza diminuzione dell’assunzione di cibo, fegati più sani, muscoli più attivi e migliore controllo glicemico. I degradatori fanno un passo ulteriore eliminando fisicamente PAK4, e studi animali iniziali suggeriscono che potrebbero proteggere dalla perdita muscolare e da alcuni tumori. Complessivamente, queste evidenze supportano l’idea che attenuare PAK4 potrebbe alleviare contemporaneamente obesità, diabete e fegato grasso, trasformando un tempo un interruttore cellulare poco noto in un promettente obiettivo per future terapie metaboliche.
Citazione: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Parole chiave: PAK4, malattia metabolica, obesità, fegato grasso, resistenza all'insulina