Clear Sky Science · it
La proteina sensibile al redox HMGB1: ruoli intracellulari ed extracellulari
Perché una proteina mutaforma conta per la salute
Dentro quasi ogni cellula del corpo si trova una piccola proteina chiamata HMGB1 che si comporta un po’ come un coltellino svizzero. In condizioni tranquille aiuta silenziosamente a organizzare il DNA. Ma quando le cellule sono stressate o danneggiate, HMGB1 può uscire dal nucleo, attraversare il tessuto circostante e funzionare come segnale di allarme per il sistema immunitario. Questo articolo di revisione spiega come piccole modifiche chimiche guidate dall’ossidazione trasformino HMGB1 in personalità biologiche molto diverse — che possono proteggere i tessuti, indurre infiammazione o contribuire a malattie croniche. Capire questo «anello dell’umore» molecolare potrebbe aprire nuove strade per calmare l’infiammazione eccessiva senza spegnere completamente il sistema immunitario.
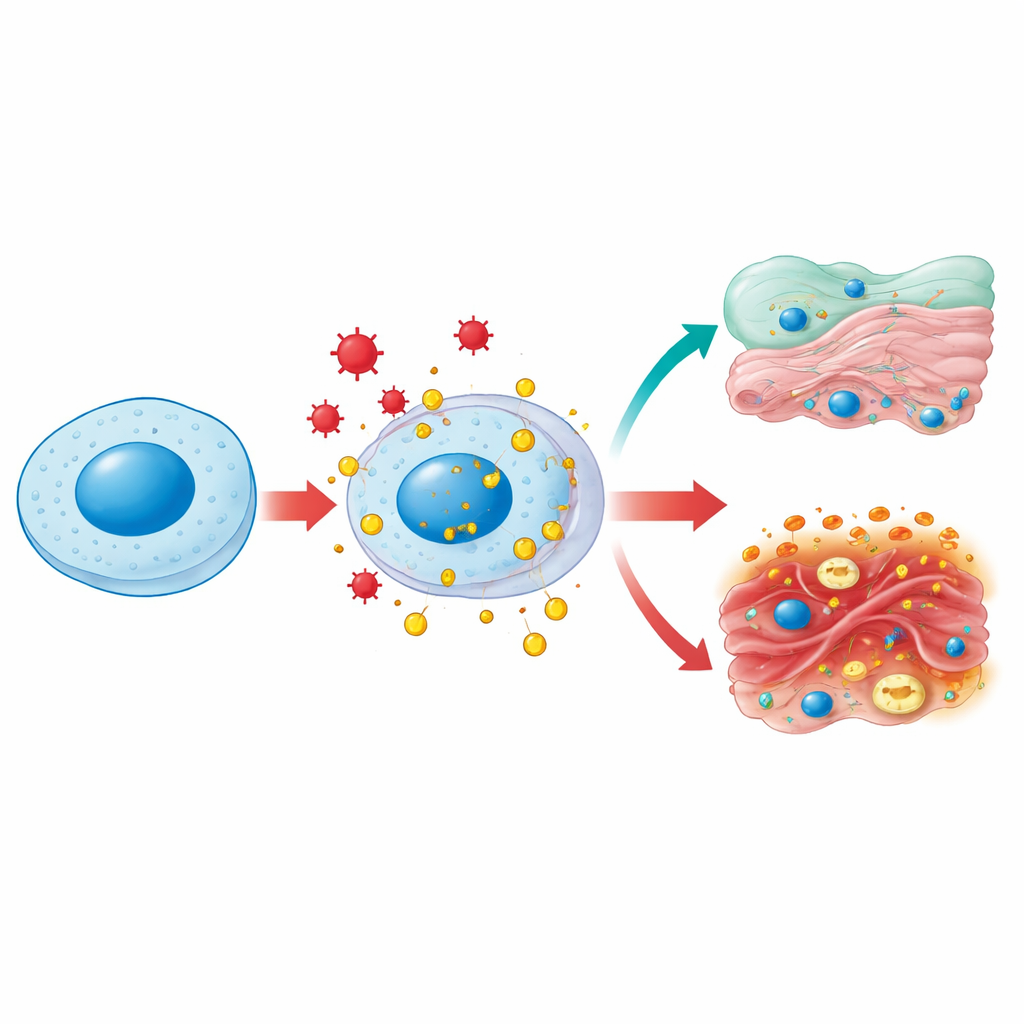
Una proteina, molti quartieri
HMGB1 vive normalmente nel nucleo cellulare, dove piega e allenta il DNA per consentire la copia e la riparazione dei geni. Sotto stress — come infezione, alti livelli di zucchero nel sangue o danno tossico — può essere modificata chimicamente ed essere escortata fuori verso il citoplasma e poi all’esterno. Nel citoplasma, HMGB1 contribuisce a mantenere sane le mitocondrie, le centrali energetiche della cellula, favorendo un processo di pulizia chiamato autofagia e prevenendo una frammentazione eccessiva di questi organelli. Quando rilasciata all’esterno della cellula, HMGB1 diventa un classico «segnale di pericolo»: le cellule immunitarie lo riconoscono come indicazione di danno tessutale e accorrono sul posto. La stessa molecola quindi svolge ruoli di manutenzione all’interno delle cellule e ruoli di allarme all’esterno, a seconda di dove si trova e di come è stata chimicamente regolata.
Come l’ossidazione riscrive il suo comportamento
Il fulcro di questa revisione è come l’ossidazione — reazioni promosse da specie reattive dell’ossigeno (ROS) — rimodelli HMGB1. La proteina contiene tre residui contenenti zolfo che funzionano come piccoli interruttori. Nello stato completamente ridotto, HMGB1 tende a favorire la sopravvivenza cellulare e il reclutamento delle cellule riparatrici. Un’ossidazione lieve può legare due di questi siti tra loro all’interno della stessa proteina, creando una forma «disolfuro» particolarmente abile nell’agganciarsi ai recettori immunitari come i recettori Toll-like e RAGE sulle superfici cellulari. Questa versione stimola fortemente la produzione di messaggeri infiammatori. Uno stress ossidativo più intenso può spingere la molecola verso una forma sovra-ossidata che non è più in grado di legare efficacemente DNA o recettori; questa versione «bruciata» diventa immunologicamente silente ed è associata alla fase di risoluzione dell’infiammazione e a programmi di morte cellulare che non provocano una reazione immunitaria.
Da segnali di morte cellulare a fattori di malattia
HMGB1 è profondamente intrecciata con i molteplici modi in cui le cellule muoiono. Durante forme violente di morte come necrosi, necroptosi, ferroptosi e piroptosi, HMGB1 fuoriesce o viene trasportata attivamente fuori dalle cellule, portando con sé una firma redox che riflette le condizioni ossidative circostanti. All’inizio della necrosi tende a trovarsi in forma ridotta, mentre lo stress prolungato la spinge verso stati più ossidati. Una volta all’esterno, HMGB1 ridotta può favorire l’autofagia protettiva in alcune cellule tumorali, aiutandole a sopravvivere alla chemioterapia, mentre le forme ricche di disolfuri e dimerizzate amplificano le cascate infiammatorie e l’attivazione del complemento che possono peggiorare il danno tissutale. HMGB1 può anche retroagire per promuovere determinati percorsi di morte — per esempio collaborando con lipidi batterici per innescare la necroptosi o favorendo la morte cellulare dipendente dal ferro nelle cellule di supporto cerebrale dopo un ictus. In questo modo, HMGB1 sia segnala sia modula l’equilibrio vita–morte nei tessuti.
Legami con infiammazione, autoimmunità e cancro
Poiché il suo comportamento è così sensibile all’ossidazione, le diverse varianti di HMGB1 compaiono in schemi distinti nelle malattie. HMGB1 ricca di disolfuri è fortemente associata all’infiammazione cronica: è presente nelle articolazioni infiammate dell’artrite reumatoide, nel fegato fibrotico, nel danno polmonare, nel danno da ischemia–riperfusione dopo chirurgia e nella sepsi, dove i suoi livelli ematici correlano con la gravità e il rischio di morte. HMGB1 ridotta, al contrario, spesso si associa alla migrazione cellulare e al rimodellamento tissutale, come lo spostamento di fibroblasti cardiaci o di monociti guidati dalla chemochina CXCL12. HMGB1 sovra-ossidata e immunologicamente silente è arricchita in contesti come l’apoptosi in stadio avanzato, dove l’organismo desidera eliminare le cellule morenti senza provocare una reazione. Nei tumori, la forma disolfuro supporta un ambiente immunitario soppressivo e permissivo alla crescita, mentre bloccare HMGB1 può ridurre i tumori e rendere più efficaci le immunoterapie con checkpoint.
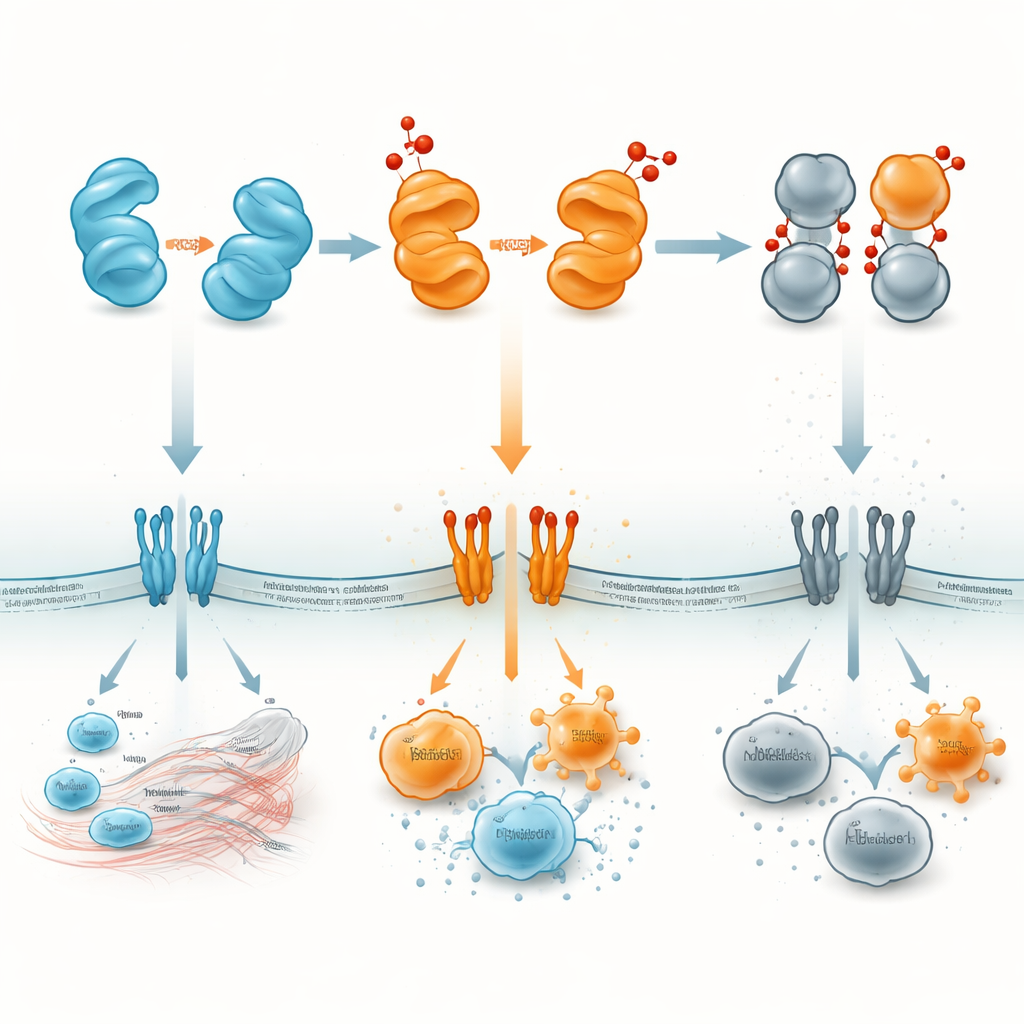
Trasformare un allarme molecolare in un bersaglio terapeutico
Per un osservatore non esperto, HMGB1 può essere pensata come un piccolo allarme proteico il cui volume e messaggio cambiano con il suo stato chimico. HMGB1 ridotta tende a chiamare le squadre di riparazione; le forme disolfuro e dimeriche possono suonare un allarme forte che alimenta un’infiammazione dannosa; e la forma completamente ossidata cade praticamente in silenzio, contribuendo a far terminare l’infiammazione. Mappando dove e quando compare ciascuna versione — nei nuclei, nel citoplasma, nel sangue o in organi specifici — i ricercatori sperano di progettare farmaci che blocchino le forme dannose o stabilizzino quelle utili. Tali strategie potrebbero permettere ai medici di trattare sepsi, autoimmunità, ictus, danno polmonare o cancro mirando non solo a HMGB1 in sé, ma anche all’«interruttore dimmer» ossidativo che controlla come questa proteina comunica con il sistema immunitario.
Citazione: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Parole chiave: HMGB1, infiammazione, stress ossidativo, morte cellulare, malattia autoimmune