Clear Sky Science · it
UBE2M come ponte tra neddilazione e regolazione del ciclo cellulare nell'adenocarcinoma colorettale
Perché questa ricerca è importante per il cancro intestinale
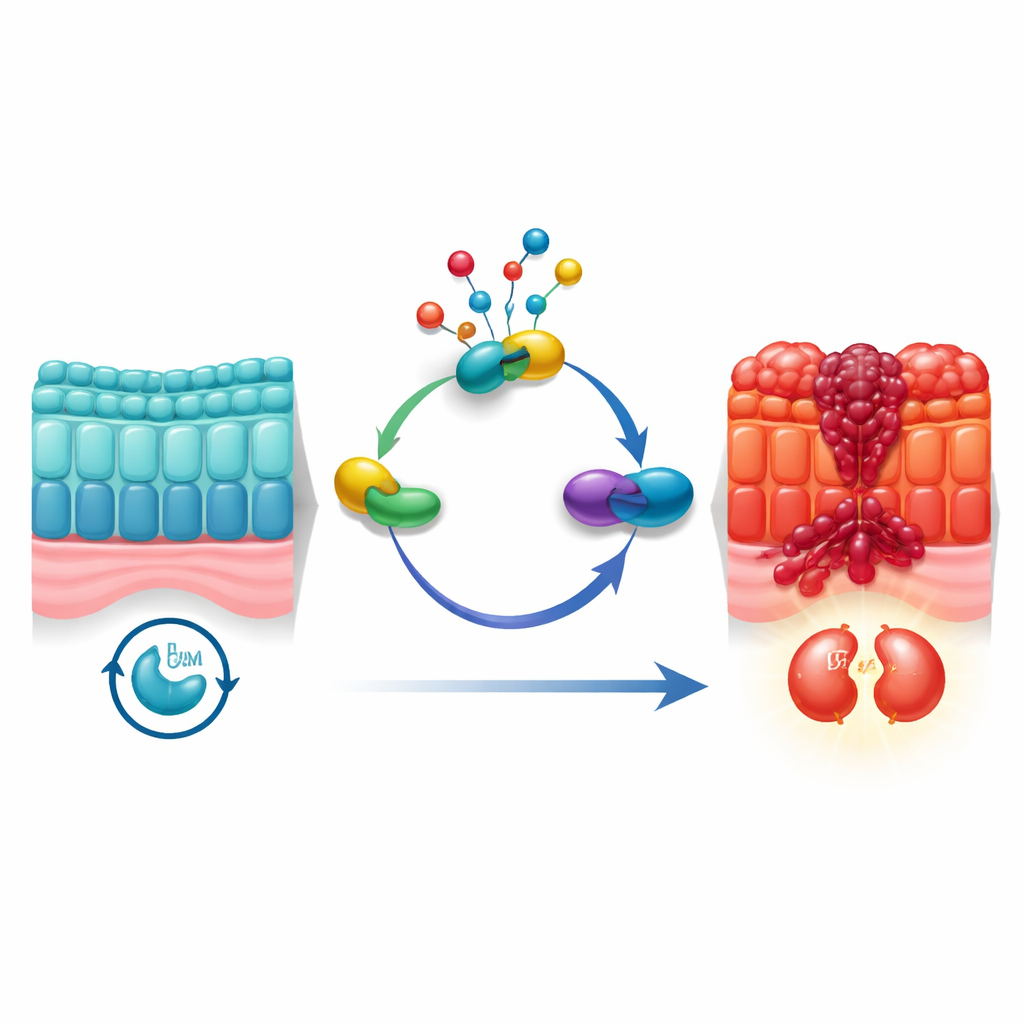
Il cancro colorettale è uno dei tumori più diffusi e letali nel mondo, in gran parte perché le cellule tumorali imparano a dividersi senza controllo. Questo studio mette in luce un interruttore di regolazione finora nascosto che aiuta le cellule del cancro colorettale a superare rapidamente un controllo critico della divisione cellulare. Rivelando come funziona questo interruttore a livello molecolare — e mostrando che un farmaco antifungino esistente può interferire con esso — il lavoro indica un possibile nuovo modo per rallentare o fermare la crescita tumorale.
Un livello nascosto di controllo all'interno delle cellule tumorali
Le cellule non si dividono a caso; percorrono un ciclo ordinato con checkpoint che verificano se è sicuro replicare il DNA e separarsi in due. Le cellule tumorali spesso alterano questi checkpoint. Gli autori si sono concentrati su un processo di etichettatura chimica chiamato neddilazione, che modifica sottilmente le proteine dopo la loro sintesi. Studi precedenti suggerivano che la neddilazione sia più attiva in molti tumori, ma come si colleghi al ciclo di divisione delle cellule colorettali non era chiaro. Utilizzando grandi dataset a singola cellula provenienti da tumori umani, insieme a dati di espressione genica in massa di oltre 1.800 pazienti, il team ha scoperto che l'attività di neddilazione è particolarmente elevata nelle cellule intestinali maligne che si trovano nella fase G2/M — il cancello finale prima che una cellula si divida.
Sotto i riflettori: una proteina «ponte» molecolare
Per capire quali molecole collegano la neddilazione alla divisione cellulare, i ricercatori hanno usato analisi computazionali in stile rete per setacciare migliaia di geni. Una proteina è emersa in modo evidente: UBE2M, un enzima che aiuta ad attaccare la piccola etichetta NEDD8 ad altre proteine. UBE2M non solo risultava fortemente collegata alle vie della neddilazione e del ciclo cellulare nei dati; era anche presente a livelli molto più alti nei tumori colorettali rispetto al tessuto sano circostante. I pazienti i cui tumori esprimevano più UBE2M tendevano ad avere una sopravvivenza peggiore, indicando che potrebbe essere un motore della malattia e non un semplice spettatore. Quando il gruppo ha ridotto UBE2M in linee cellulari tumorali e in modelli murini, la crescita tumorale rallentava, le divisioni cellulari diminuivano e aumentava la morte programmata. Al contrario, forzare l'espressione di UBE2M accelerava la crescita e la progressione del ciclo cellulare.
Una staffetta che protegge una proteina chiave della proliferazione
Approfondendo, gli scienziati hanno indagato come UBE2M faciliti la divisione cellulare. Hanno scoperto che UBE2M non agisce da solo ma avvia una staffetta coinvolgendo altre due proteine, USP39 e PABPC1. Normalmente, PABPC1 viene segnato per la distruzione da una catena di etichette ubiquitina, che lo indirizzano al macchinario di riciclo proteico della cellula. Il team ha dimostrato che UBE2M modifica chimicamente USP39 con l'etichetta NEDD8. Questa modifica potenzia la capacità di USP39 di rimuovere catene di ubiquitina da PABPC1, salvandolo dalla degradazione e rendendolo più stabile. Con più PABPC1 disponibile, la cellula è più efficiente nella traduzione di specifici mRNA in proteine, incluso l'mRNA per CCNB1, una ciclina che funge da acceleratore per il checkpoint G2/M. In sostanza, UBE2M contribuisce a stabilizzare PABPC1, che a sua volta aumenta la produzione di CCNB1, spingendo le cellule verso la divisione.
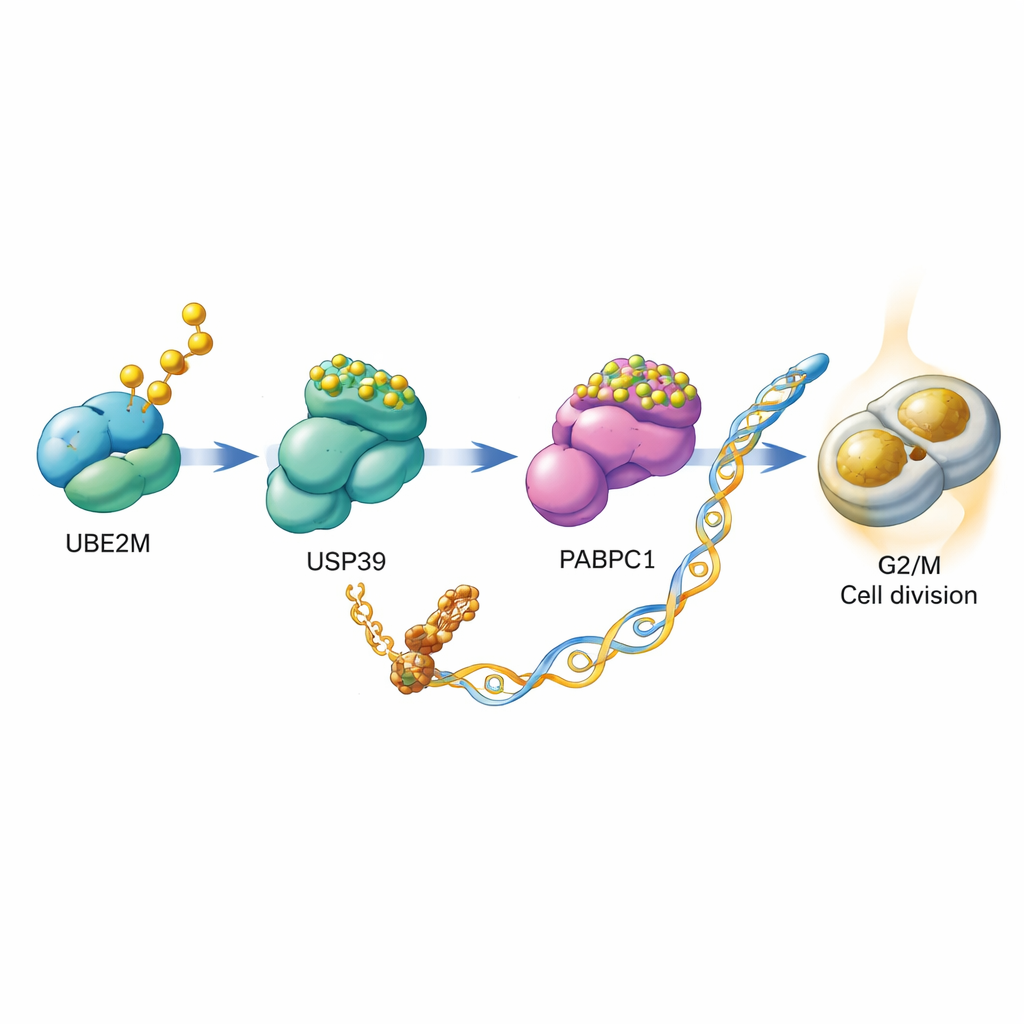
Dal meccanismo molecolare all'opportunità farmacologica
La scoperta di questa catena UBE2M–USP39–PABPC1–CCNB1 ha suggerito una nuova debolezza nelle cellule del cancro colorettale. Gli autori si sono rivolti alla micafungina, un farmaco già usato per trattare le infezioni fungine e recentemente identificato come inibitore dell'attività di neddilazione mediata da UBE2M. In cellule tumorali intestinali coltivate in laboratorio, la micafungina ha ridotto la neddilazione di USP39, aumentato la degradazione di PABPC1 e abbassato i livelli della proteina CCNB1. Di conseguenza, la divisione cellulare rallentava, più cellule restavano bloccate al checkpoint G2/M e aumentava l'apoptosi. In topi impiantati con cellule di cancro colorettale, il trattamento giornaliero con micafungina ha significativamente ridotto le dimensioni dei tumori rispetto agli animali non trattati, senza la necessità di rimuovere direttamente UBE2M.
Che cosa significa per i pazienti a lungo termine
Questo lavoro dipinge un quadro chiaro di come un singolo enzima, UBE2M, possa collegare un sottile sistema di etichettatura proteica alla decisione di una cellula tumorale intestinale di dividersi. Stabilizzando un fattore di traduzione (PABPC1) tramite USP39, UBE2M aumenta indirettamente i livelli di un potente regolatore del ciclo cellulare, CCNB1, permettendo ai tumori di crescere più rapidamente. Sebbene siano necessarie ulteriori ricerche e test clinici, i risultati suggeriscono che bloccare questa catena — potenzialmente con farmaci riproposti come la micafungina — potrebbe offrire una nuova strategia mirata per rallentare la progressione del cancro colorettale e migliorare gli esiti per i pazienti.
Citazione: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Parole chiave: cancro colorettale, ciclo cellulare, neddilazione, UBE2M, terapia mirata