Clear Sky Science · it
CDK13 guida il carcinoma renale a cellule chiare tramite la modificazione m6A dell’RNA di ACLY mediata da METTL16
Perché i tumori renali ricchi di grasso sono importanti
Il carcinoma renale a cellule chiare appare spesso pallido e oleoso al microscopio perché le sue cellule sono piene di lipidi. Quell’aspetto insolito non è solo estetico; riflette una riorganizzazione profonda di come queste cellule tumorali gestiscono il carburante. Questo studio pone una domanda semplice ma cruciale: quale interruttore molecolare spinge le cellule tumorali renali ad accumulare grasso, e si può spegnere quell’interruttore per rallentare la malattia?
Un direttore nascosto della crescita tumorale
I ricercatori si sono concentrati su una proteina chiamata CDK13, parte di una famiglia di enzimi che normalmente aiutano le cellule a dividersi. Analizzando ampi set di dati di pazienti e campioni tumorali, hanno trovato che i livelli di CDK13 sono costantemente più alti nei carcinomi renali a cellule chiare rispetto al tessuto renale normale. I pazienti i cui tumori esprimevano maggiormente CDK13 tendevano ad avere tumori più grandi, in stadio avanzato e con prognosi peggiore. Quando il gruppo ha ridotto CDK13 nelle linee cellulari di carcinoma renale, le cellule crescevano più lentamente e avevano difficoltà a progredire nel ciclo cellulare, suggerendo che CDK13 agisca come un direttore nascosto che coordina crescita e sopravvivenza.
Dal glucosio al grasso: la riorganizzazione della fabbrica energetica cellulare
Poiché i tumori renali a cellule chiare sono pieni di lipidi, il team ha esaminato se CDK13 controlli anche la sintesi lipidica. Usando un mix di profilazione dell’espressione genica e colorazioni microscopiche dei grassi, hanno dimostrato che l’aumento di CDK13 incrementa l’accumulo di goccioline lipidiche all’interno delle cellule tumorali, mentre la riduzione di CDK13 produce l’effetto opposto. CDK13 influenzava in modo marcato un enzima chiamato ACLY, che converte un comune intermedio metabolico in acetil‑CoA, il materiale di partenza per la sintesi di acidi grassi e colesterolo. Nelle biopsie dei pazienti, livelli elevati di CDK13 andavano di pari passo con livelli elevati di ACLY e entrambe le proteine si concentravano nelle stesse aree del tessuto tumorale. Quando ACLY veniva sovraespresso artificialmente, molte delle anomalie di crescita e di accumulo lipidico causate dalla perdita di CDK13 venivano ripristinate, collocando ACLY come un effettore chiave a valle di questa via. 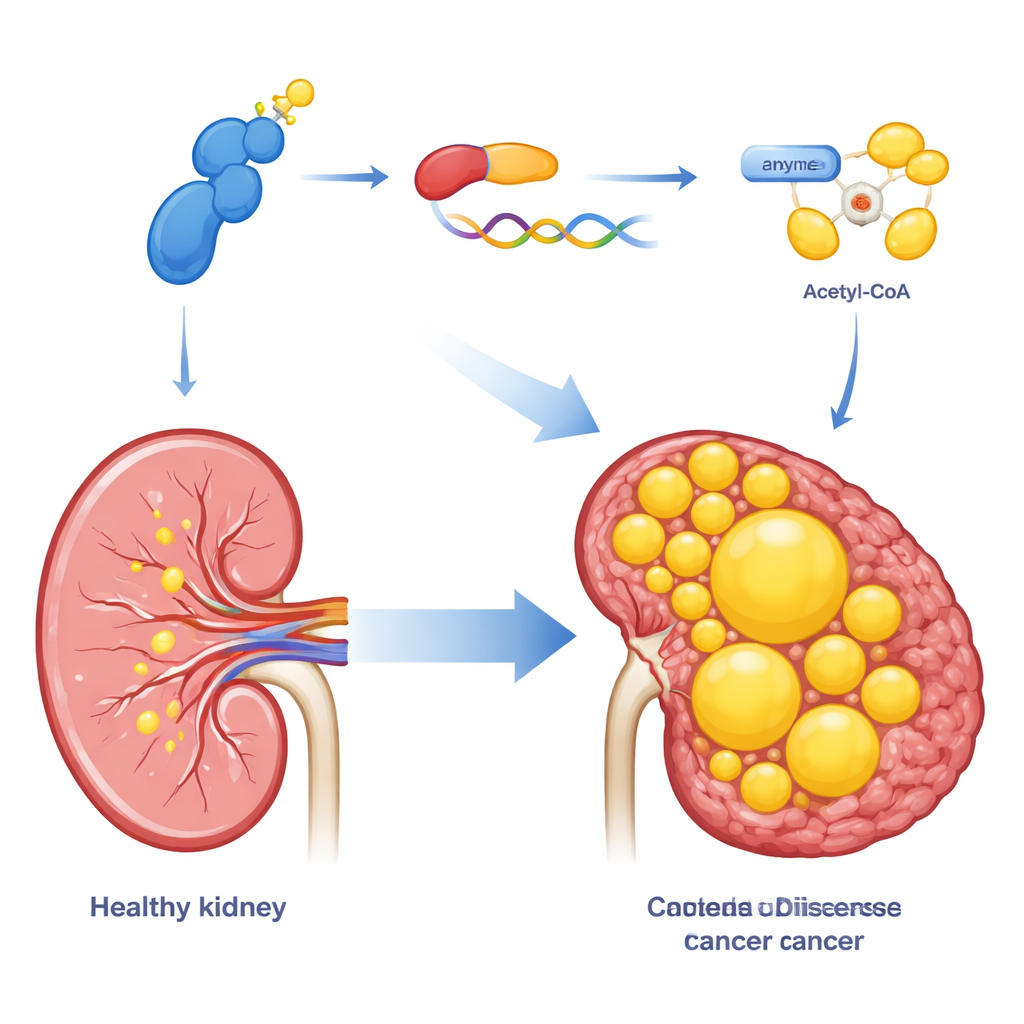
Un sistema a strati di messaggi dentro le cellule tumorali
Piuttosto che agire direttamente su ACLY come un semplice interruttore on‑off, CDK13 esercita il suo controllo attraverso un sistema a strati basato sull’RNA, la molecola che trasporta le istruzioni genetiche dal DNA alle fabbriche proteiche. Gli autori hanno scoperto che CDK13 si lega fisicamente e modifica chimicamente un altro enzima, METTL16, che marca messaggi RNA specifici con piccoli gruppi chimici chiamati gruppi metile. CDK13 aggiunge a METTL16 una fosforilazione in un sito preciso, aumentando l’attività di METTL16. A sua volta, METTL16 aggiunge ulteriori marche metiliche sull’RNA che codifica per ACLY. Queste marche non cambiano il codice genetico, ma alterano il modo in cui la cellula tratta quel messaggio. Una terza proteina, YTHDC2, riconosce l’RNA di ACLY marcato e lo protegge dalla degradazione, permettendo una maggiore produzione di proteina ACLY nel tempo. Questa cascata — CDK13 che attiva METTL16, METTL16 che marca l’RNA di ACLY e YTHDC2 che custodisce quel messaggio marcato — crea un circuito potente che spinge la sintesi lipidica. 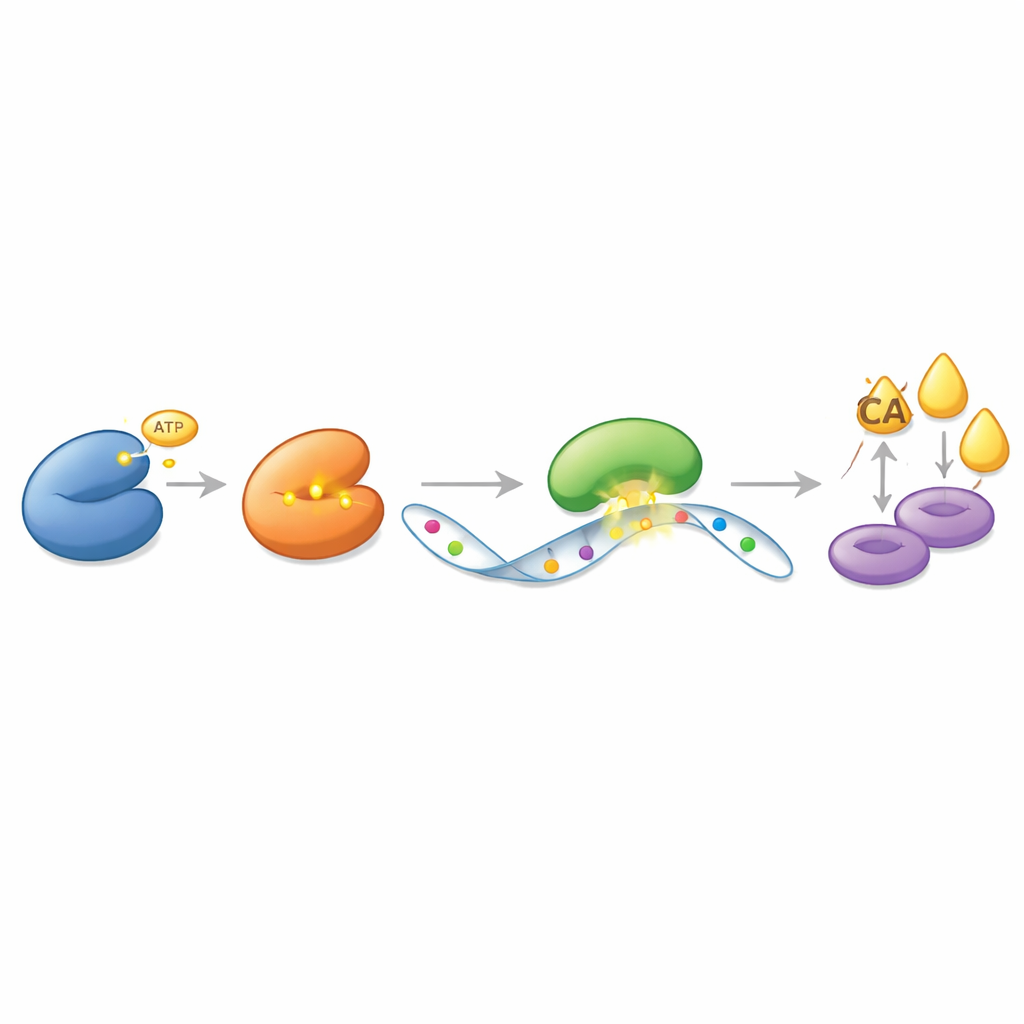
Testare la catena in cellule, topi e campioni di pazienti
La solidità del lavoro risiede nella meticolosità con cui gli autori hanno testato questa catena di eventi. In cellule tumorali renali coltivate, l’interruzione di qualsiasi componente della via CDK13–METTL16–ACLY riduceva le goccioline lipidiche e rallentava la proliferazione. In topi impiantati con cellule umane di carcinoma renale, bloccare CDK13 o ACLY singolarmente riduceva la crescita tumorale e la riserva di grasso al loro interno, mentre bloccarli insieme aveva un effetto ancora più marcato. Il team ha anche usato un composto a piccola molecola, 1NM‑PP1, che inibisce l’attività di CDK13. Questo agente simile a un farmaco ha ridotto il segnale attivante su METTL16, abbassato i livelli di ACLY e soppresso la crescita tumorale, specialmente se combinato con la deplezione di METTL16. Nei dati dei pazienti, CDK13, METTL16 e ACLY tendevano a salire e scendere insieme, rafforzando l’idea che quest’asse sia attivo nei tumori reali, non solo nei modelli di laboratorio.
Cosa potrebbe significare per i trattamenti futuri
Per chi non è specialista, il messaggio principale è che questo studio mette in luce un nuovo manopola di controllo per la “fabbrica del grasso” all’interno dei tumori renali a cellule chiare. Invece di mirare soltanto agli enzimi che sintetizzano i lipidi, i ricercatori rivelano una catena di comando di livello superiore che stabilizza le istruzioni per quegli enzimi. Interrompendo l’asse CDK13–METTL16–ACLY, potrebbe essere possibile privare i tumori dei lipidi di cui hanno bisogno per crescere e diffondersi, risparmiando maggiormente le cellule normali. Pur essendo ancora lavoro preclinico e 1NM‑PP1 non essendo attualmente un farmaco per il carcinoma renale, i risultati indicano nuove strategie che associano inibitori di chinasi a farmaci che mirano agli enzimi che modificano l’RNA, offrendo un modo più preciso per trattare questa forma di carcinoma renale guidata dal metabolismo.
Citazione: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Parole chiave: carcinoma renale a cellule chiare, metabolismo lipidico, CDK13, metilazione dell'RNA, ACLY