Clear Sky Science · it
Il fattore regolatore dell’interferone 5 partecipa alla patogenesi dell’enfisema tramite NLRP3 e cellule che esprimono Ly6C
Perché questo studio sui polmoni è importante
La broncopneumopatia cronica ostruttiva (BPCO) e l’enfisema privano milioni di persone del respiro, spesso molti anni dopo che hanno smesso di fumare. I farmaci attuali possono aiutare ad aprire le vie aeree, ma fanno poco per placare l’infiammazione persistente che continua a consumare il tessuto polmonare. Questo studio mette in luce un «capobanda» molecolare di quel danno, suggerendo un nuovo modo per proteggere i delicati alveoli e rallentare il declino della funzione polmonare.
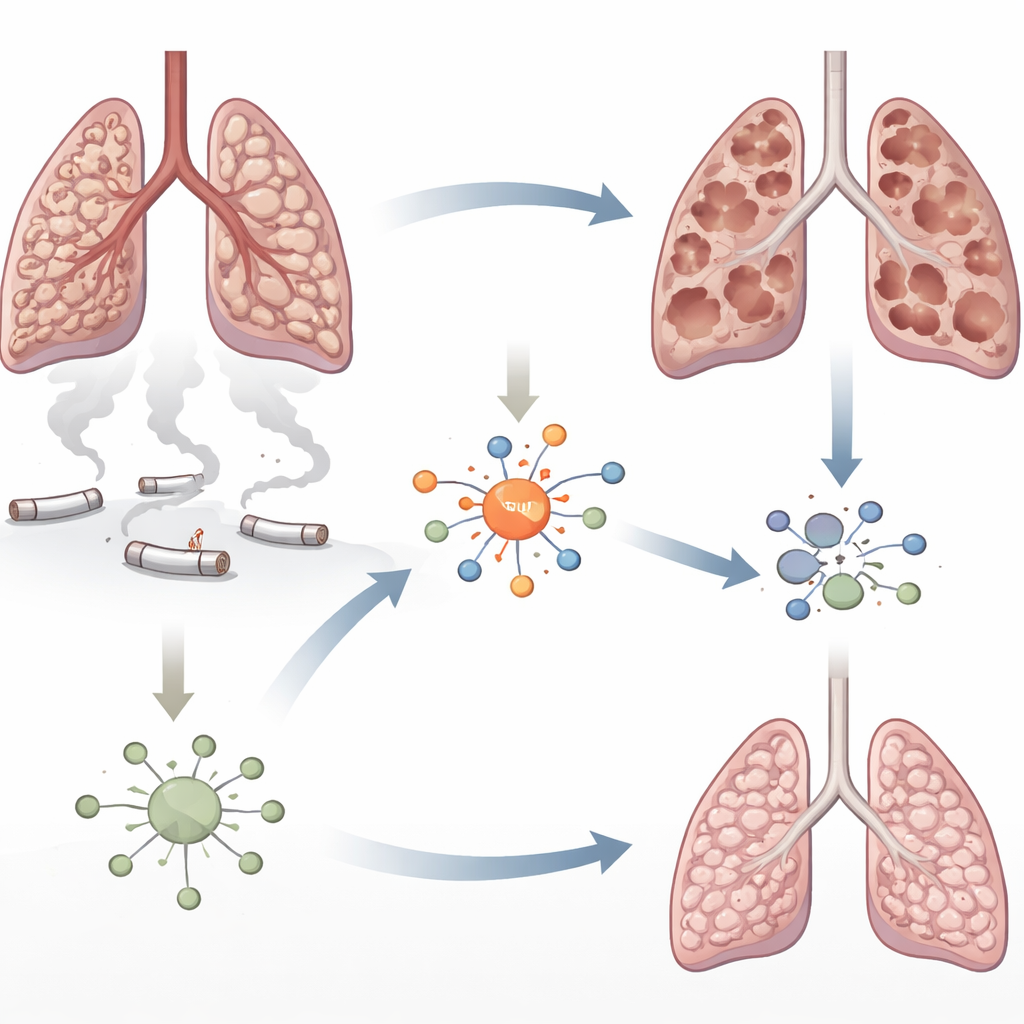
Uno sguardo più approfondito ai polmoni danneggiati dal fumo
L’enfisema è caratterizzato dalla progressiva distruzione dei piccoli alveoli che scambiano ossigeno e anidride carbonica. Il fumo di sigaretta bagna i polmoni con particelle tossiche che danneggiano le cellule e richiamano ondate di cellule immunitarie. Gli autori si sono concentrati su una proteina chiamata fattore regolatore dell’interferone 5 (IRF5), nota per guidare l’infiammazione nelle malattie autoimmuni ma poco studiata nella BPCO. Lavori precedenti avevano suggerito che i livelli di IRF5 aumentano nei polmoni esposti al fumo. In questo studio i ricercatori hanno voluto verificare se IRF5 sia semplicemente associata all’infiammazione o se contribuisca effettivamente alla distruzione del tessuto polmonare.
Spegnere un interruttore chiave nei topi
Per esplorare il ruolo di IRF5, il gruppo ha creato topi privi del gene che codifica questa proteina. Poi ha esposto animali normali e privi di IRF5 al fumo di sigaretta per diverse settimane e ha confrontato lo stato dei loro polmoni. Nei topi normali il fumo ha provocato chiari segni di enfisema: le pareti tra alveoli adiacenti sono andate perdute, lasciando ampi spazi iperinfiati. Al contrario, i topi privi di IRF5 sono risultati in gran parte protetti da questo danno strutturale, anche se il fumo ha comunque richiamato cellule immunitarie negli spazi aerei e aumentato molte molecole infiammatorie. Ciò indica che IRF5 è un collegamento cruciale tra l’esposizione al fumo e la distruzione dell’architettura polmonare.
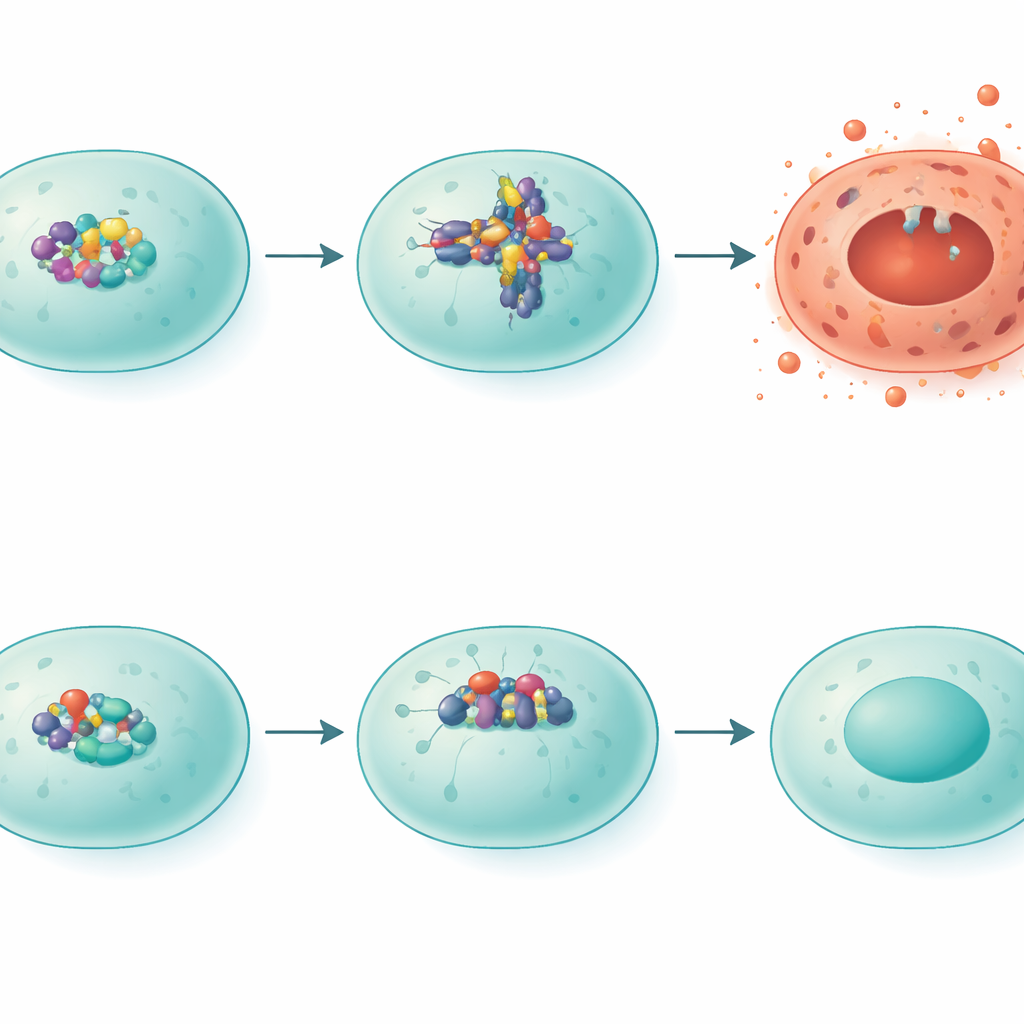
Come IRF5 spinge le cellule verso una morte infiammatoria
I ricercatori si sono poi concentrati su una particolare forma di morte cellulare violenta chiamata piroptosi, che apre buchi nelle membrane cellulari e riversa contenuti infiammatori nei tessuti circostanti. Al centro di questo processo c’è un complesso proteico noto come NLRP3. Nei topi normali esposti al fumo i livelli di NLRP3 sono aumentati, e i pattern di un’altra proteina, gasdermina D, corrispondevano a uno stato compatibile con la piroptosi. Nei topi privi di IRF5 i livelli di NLRP3 erano molto più bassi e la gasdermina D era tagliata in forme alternative associate a esiti meno distruttivi. Quando il team ha aumentato artificialmente IRF5 in cellule polmonari in laboratorio, i livelli di NLRP3 sono saliti, confermando che IRF5 agisce come un interruttore trascrizionale che attiva questa via dannosa.
Cellule immunitarie protettive entrano in scena
IRF5 ha anche rimodellato la composizione delle cellule immunitarie nel polmone. Nei topi privi di IRF5 è stato osservato un marcato aumento di un sottotipo di cellule derivanti dal sangue fortemente segnate da una molecola di superficie chiamata Ly6C. Queste cellule Ly6C‑alte includevano sia monociti sia cellule T e comparivano in numero maggiore dopo l’esposizione al fumo. Quando gli scienziati hanno purificato cellule Ly6C‑alte da topi privi di IRF5 e le hanno infuse in animali normali esposti al fumo, i riceventi hanno mostrato minore distruzione degli alveoli e livelli ridotti di NLRP3 nel polmone. Ulteriori esperimenti hanno rivelato che IRF5 sopprime direttamente l’attività del gene Ly6C, suggerendo che in presenza di IRF5 si producono o si mantengono meno di queste cellule potenzialmente protettive.
I polmoni umani confermano il segnale
Per verificare se questi risultati potessero avere rilevanza per le persone, gli autori hanno esaminato tessuto polmonare di pazienti sottoposti a intervento chirurgico per cancro polmonare. Hanno confrontato campioni di individui con buona capacità di scambio gassoso con quelli con enfisema rilevante. I livelli di proteina IRF5 erano sostanzialmente più alti nei polmoni del gruppo con enfisema. Pur non essendo uno studio sufficientemente ampio da collegare IRF5 con precisione alla gravità dei sintomi o alle riacutizzazioni, il quadro corrisponde ai risultati nei topi: più IRF5 nei polmoni malati, meno nei polmoni più sani.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, il lavoro dipinge IRF5 come un coordinatore centrale del danno polmonare indotto dal fumo. Potenzia un motore di morte cellulare centrato su NLRP3 e devia le cellule immunitarie lontano dalle popolazioni Ly6C‑alte che sembrano contribuire a preservare la struttura degli alveoli. Per i pazienti l’implicazione è semplice: un farmaco che attenui l’attività di IRF5 potrebbe, in teoria, ridurre le forme più distruttive di infiammazione senza spegnere del tutto il sistema immunitario. Sebbene terapie di questo tipo non esistano ancora per la BPCO, questo studio fornisce un chiaro bersaglio molecolare e un percorso biologicamente plausibile verso trattamenti che facciano più che dilatare le vie aeree ristrette: potrebbero proteggere il fragile impalcato del polmone.
Citazione: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Parole chiave: enfisema, BPCO, infiammazione, immunità polmonare, morte cellulare