Clear Sky Science · he
מקור המבנה הרביעוני בהתפתחות הסיביות של המוגלובין הסיקלתי: מחקר בדינמיקה מולקולרית
מדוע הסיפור הדמיוני הזה חשוב
מחלת תאי החרמש מתחילה משינוי זעיר בחלבון דם אחד, ובכל זאת מסוגלת לעצב מחדש את תאי הדם האדומים, לחסום כלי דם ולגרום לכאב כרוני. המחקר הזה בוחן באופן מדוקדק ובמונחים פיזיקליים כיצד השינוי הבודד הזה גורם למולקולת ההמוגלובין להצטבר לסיבים קשיחים בתוך התא. באמצעות הדמיות מחשב מתקדמות, המחברים מקשרים בין פרטים אטומיים לבעיות ברמת התא השלם, ומציעים רמזים חדשים כיצד תרופות עתידיות עשויות למנוע מהמוגלובין לחסום את זרם הדם.
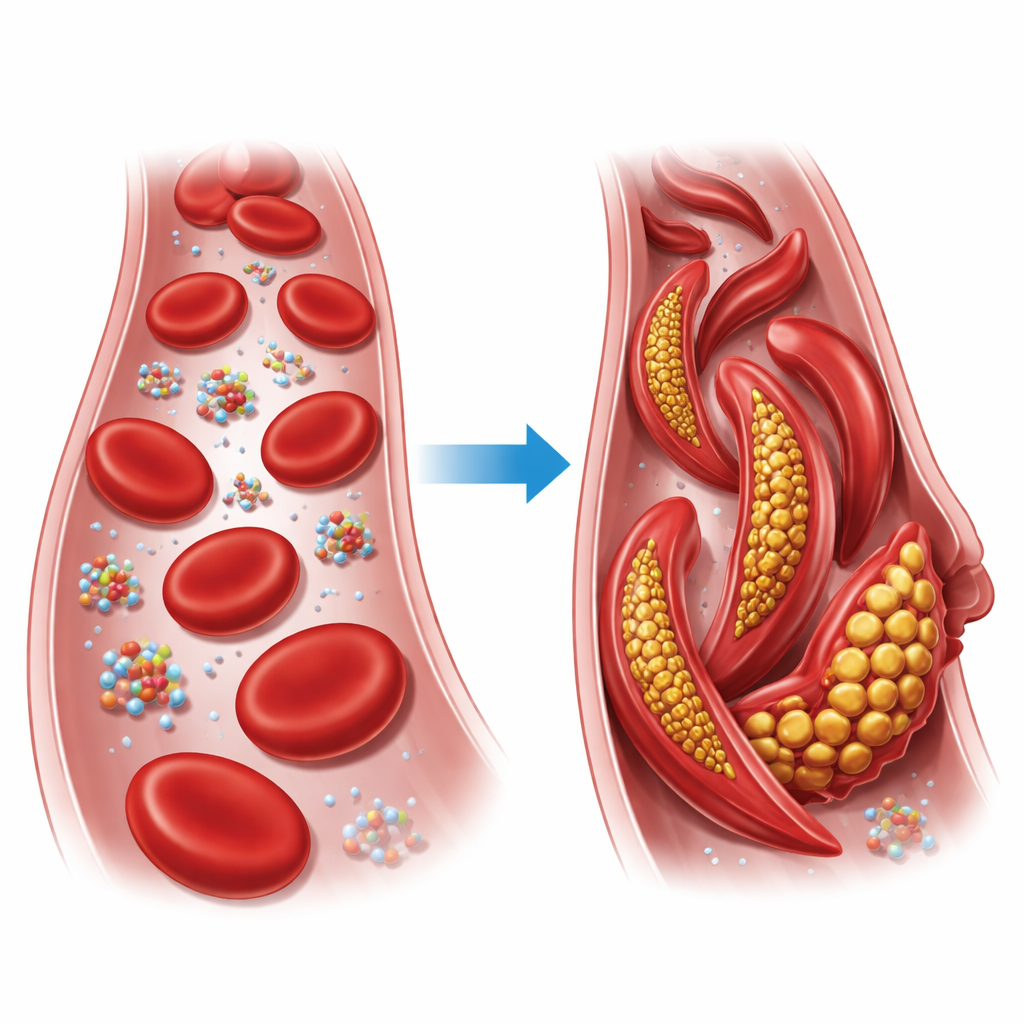
החלפה זעירה עם השלכות גדולות
המוגלובין הוא החלבון הנושא חמצן הממלא את תאי הדם האדומים שלנו. כל יחידת המוגלובין בנויה מארבע שרשרות שיכולות להתארגן בשתי צורות כלליות עיקריות, הידועות כמצב הרפוי (R) ומצב המתוח (T). באנמיית תאי חרמש, בלוק בנייה אחד בשרשרת אחת מוחלף: גלוטמט טעון מוחלף בוולין שומני במיקום שש בשרשרת הביטא. בתנאי חוסר חמצן, הגרסה המשובשת הזו, המכונה המוגלובין סיקלתי, נקשרת זו לזו ויוצרת סיבים ארוכים שמעוותים תאי דם אדומים עגולים לתצורות קשיחות בדמות חרמש, שעלולות לסתום כלי דם קטנים ולגרום לרקמות חוסר חמצן.
מעקב אחרי שינויי הצורה של המוגלובין
המחברים מתמקדים בדרך שבה יחידות המוגלובין שלמות מסתובבות ומתארגנות זו לצד זו בתוך הסיב. הם עוקבים אחרי שינוי צורה בקנה מידה גדול באמצעות זווית יחידה שמודדת כיצד שתי חצאי החלבון מסתובבות זו ביחס לזו. באמצעות הדמיות דינמיקה מולקולרית — ניסויים וירטואליים שחישובם מראה כיצד אטומים נעים במים ומלח לאורך זמן — הם דוחפים בעדינות את הזווית דרך טווח רחב ומחשבים כמה אנרגיה כל צורה דורשת. הם מגלים שגם המוגלובין הנורמלי וגם הסיקלתי יכולים לחקור רבות מהצורות הללו בטמפרטורת הגוף. המוגלובין הסיקלתי מראה העדפה זוויתית קלה, אך העדפות צורה אלה לבדן אינן מספיקות להסביר מדוע רק הצורה הסיקלית יוצרת סיבים יציבים.
מדוע הסיבים הסיקליים נדבקים ואלה הנורמליים מתפרקים
כדי להגיע לשורש היווצרות הסיב, המחקר מודד עד כמה יחידות המוגלובין שכנות נמשכות זו לזו לאורך הסיב וברוחבו. הצוות מחשב את אנרגיית הקוהזיה — הכוח הנטו שמחזיק את היחידות יחד — עבור רבות מהצורות הכוללות. עבור המוגלובין הסיקלתי, אנרגיית הקוהזיה נשארת שלילית (כלומר אטרקטיבית) לאורך טווח הצורות שנבדק, ולכן הסיבים נשארים יציבים ואינם נשברים בקלות. לעומת זאת, אצל המוגלובין הנורמלי, בחלק מהצורות אנרגיית הקוהזיה חיובית, מה שהופך סיבים בזוויות אלו לבלתי יציבים וקטופים להתפרקות ספונטנית. הבדל מרכזי הוא האופן שבו קבוצות הצד של הוולין המוטנטיות נשלחות אל תוך החלבונים השכנים: במוגלובין הסיקלתי, פלחי השומן האלה יוצרים מגעים יציבים הן לרוחב והן לאורך ציר הסיב, ותורמים ישירות לצמיחת הסיב.
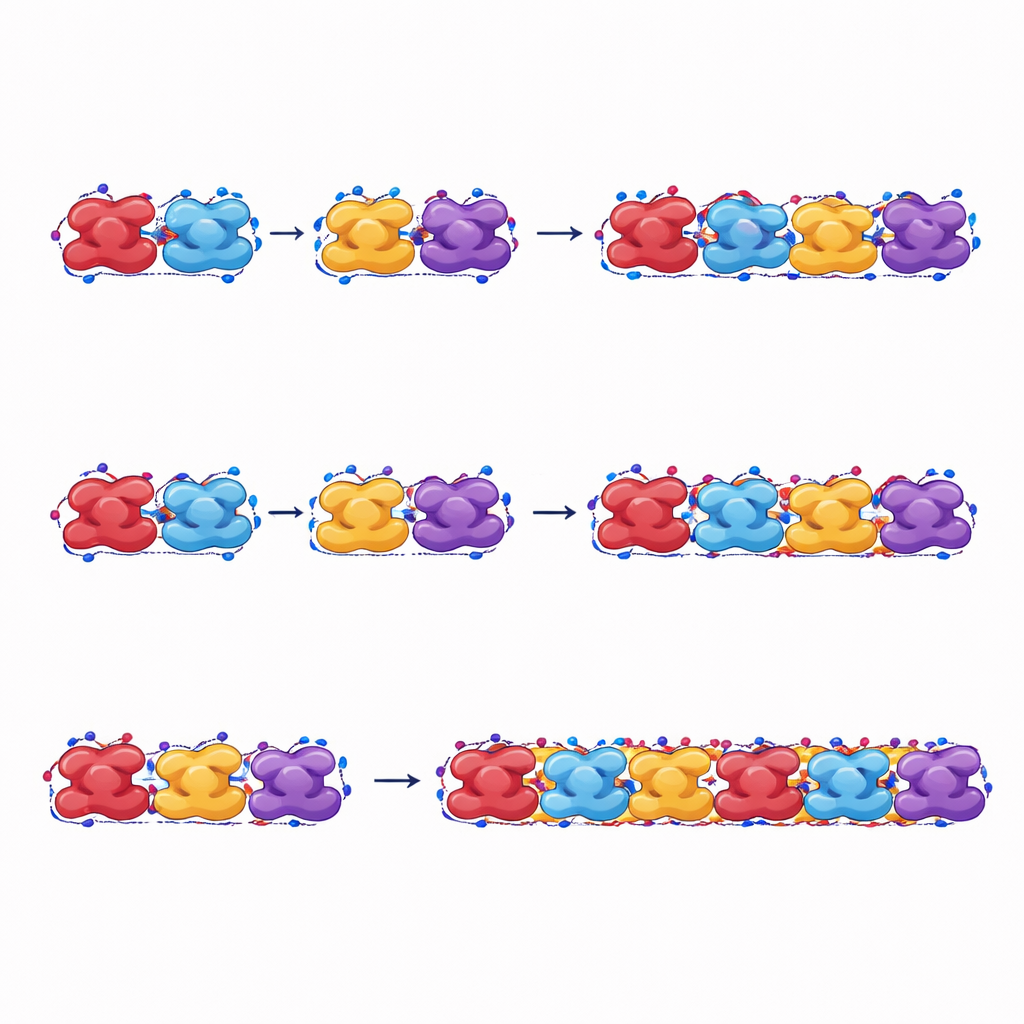
כיצד סיבים אלה נושאים עומס ומתפרקים
המחברים גם מתארכים את הסיבים המדומים שלהם כדי לדמות עומס מכני. כאשר מושכים לאורך אורכם, סיבים המורכבים ממוגלובין סיקלתי סובלים מכוחות ומתיחים גבוהים יותר וסופגים יותר אנרגיה לפני השבירה מאשר אלו המורכבים מהמוגלובין הנורמלי. אפילו הצורה הרפויה של הסיבים הסיקלתיים, שאינה הצורה שבה הסיבים מופיעים לראשונה, יכולה לשמר את השרשרת באמצעות שינויים פלסטיים בצורה, ועוזרת לשמור על שלמות הסיב לאחר היווצרותו. לעומת זאת, סיבי המוגלובין הנורמליים נפרדים בקלות רבה יותר בין יחידות שכנות וסופגים פחות אנרגיה לפני כישלון, מה שמאשר שהם פחות יציבים תחת מתח.
רמזים לטיפולים עתידיים וחומרים חדשים
בהתאם, ההדמיות מראות ששינוי חומצת אמינו יחיד משנה את אופן המפגש בין יחידות המוגלובין, מעקם את ההרכבה הכוללת לזוויות שמעדיפות משיכה חזקה, במיוחד במצב המתוח. שילוב זה של גיאומטריה ודביקות מאפשר למוגלובין הסיקלתי ליצור סיבים ארוכים וקשיחים שמתגוננים גם מתנועה תרמית וגם מתיחה מכנית, מה שמעוות בסופו של דבר את תאי הדם האדומים וסותם את זרימת הדם. על ידי הצבעת מאפיינים ספציפיים של הסידור הכולל של החלבון השולטים ביציבות הסיב, העבודה מרמזת כי תרופות אנטי‑סיקליות יעילות יכולות לפעול על ידי דחיפת ההמוגלובין לעבר צורות שבהן סיבים הופכים לאנרגטית בלתי־נכונים ופגיעים מבחינה מכנית — ולשחרר גודש מולקולרי קטלני אל תוך זרימת דם חופשית שוב.
ציטוט: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
מילות מפתח: אנמיית תאי חרמש, סיבי המוגלובין, הצטברות חלבונים, דינמיקה מולקולרית, הפרעות דם