Clear Sky Science · he
המוטציה APP E590D מגדילה יצירה של פפטידים Aβ ו‑Aη ומחמירה טאו-פתולוגיה
מדוע המוטציה החריגה הזו חשובה
מחלת אלצהיימר נתפסת בדרך כלל כתוצאה מהצטברות איטית של שני חלבונים מזיקים, אמילואיד וטאו, במוח. רוב האנשים מפתחים אלצהיימר ללא גורם בודד ברור, אך כמה משפחות נושאות שינויים גנטיים נדירים שיכולים להזיז את המאזן באופן דרמטי. המאמר הזה בוחן אחד כזה — שינוי לא שכיח בגֵן של חלבון המקור לאמילואיד (APP) — ומראה כיצד הוא יכול להגביר באופן קיצוני את יצירת חלקיקי חלבון רעילים ולהחמיר את התהליך של סבך הטאו. הבנה של המקרה החריג הזה מספקת רמזים שעשויים לחול בצורה רחבה יותר על הדרך שבה אלצהיימר מתחיל ואז מואץ.
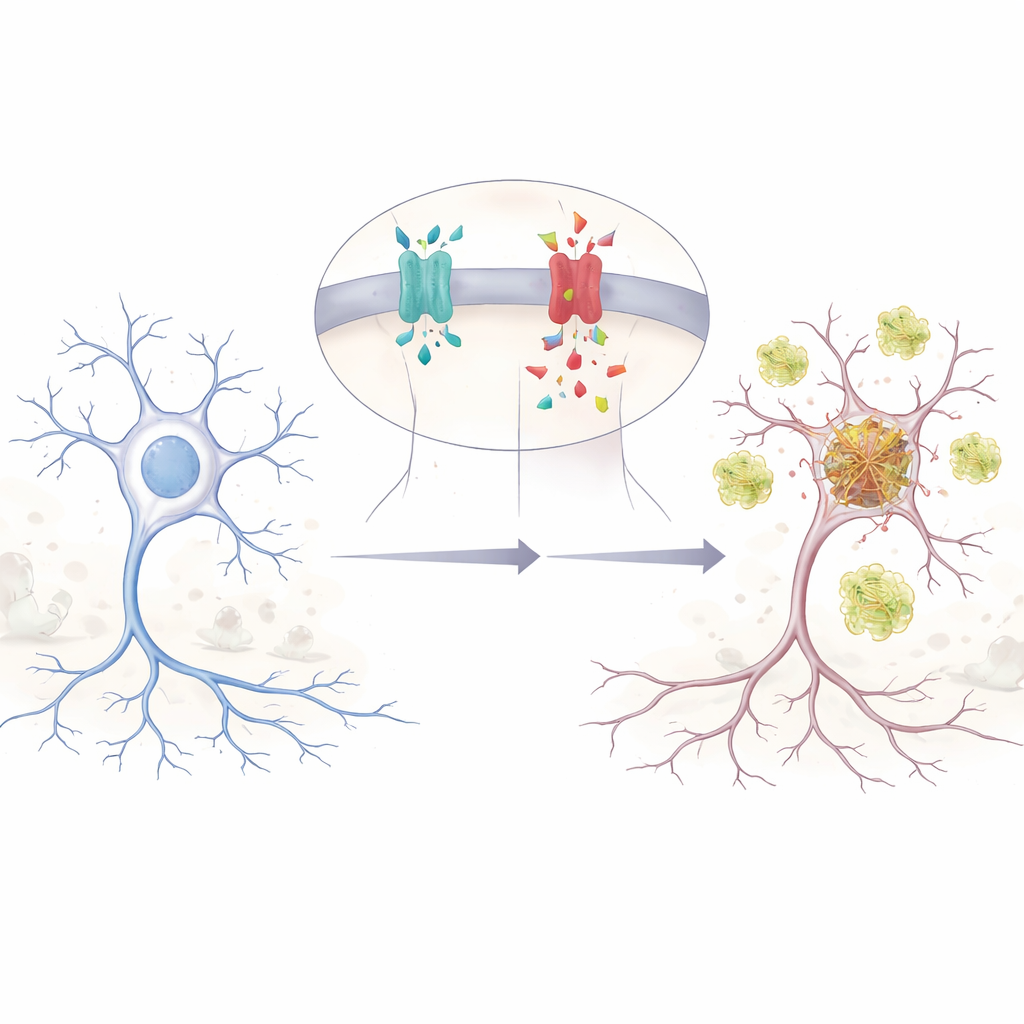
שינוי גנטי קטן עם השפעות גדולות
החוקרים מתמקדים בשינוי של אות אחת בגן APP, המכונה E590D בצורת ה‑APP הדומיננטית במוח. מוטציה זו דווחה רק בשני אנשים, שניהם עם אבחנה מאושרת של אלצהיימר בגילאים יחסית צעירים ותסמינים בלתי רגילים של בעיות זיכרון והתנהגות מוקדמות מאוד. מאחר שהיא כל כך נדירה, המדענים לא היו בטוחים אם היא אכן גורמת למחלה או פשוט קיימת במקרה. כדי לברר, הצוות שיחזר את המוטציה בתאים אנושיים ובנוירונים של עכבר, ואז עקב כיצד APP נחתך לחתיכותיו השונות. הם גילו ש‑APP המוטנטי מייצר הרבה יותר אמילואיד‑בטא (Aβ), הפפטיד הדביק שקשור לאלצהיימר מזה זמן רב, מאשר APP רגיל כאשר משווים רמות באופן הוגן.
שני פפטידים רעילים במקום אחד
ניתן לחתוך את APP בכמה דרכים, כמו לוג שנחתך בנקודות שונות. המסלול הקלאסי של אלצהיימר מייצר Aβ, אבל חיתוך אחר מייצר שבר פחות מוכר בשם Aη. עבודות קודמות הראו ש‑Aη יכול לפגוע בקשרים בין תאי העצב ולהחליש את יכולת המוח לחזק זיכרונות. בניסויים שלהם מצאו החוקרים שמוטציית E590D לא רק מגדילה את Aβ; היא גם מעלה משמעותית את Aη ואת שבר על־זרם שמזין את שני המסלולים. משמעות הדבר היא שהמוטציה מזיזה את עיבוד ה‑APP לעבר מכה כפולה של פפטידים מזיקים, שעלולה להפריע למעגלים המוחיים עוד לפני שניתן לצפות להופעת פלאקאמילואיד קלאסיים.
כיצד המוטציה מזרזת תנועה תאית
כדי להבין מדוע נוצרים יותר שברים רעילים, הצוות חקר היכן APP נמצא וכיצד הוא נע על פני שטח התא. חיתוכים רבים שיוצרים Aβ מתרחשים רק לאחר ש‑APP נמשך פנימה לתוך התא בתהליך שנקרא אנדוציטוזה. באמצעות הדמיה וטריקים ביוכימיים שמסמנים חלבונים על המשטח ואז עוקבים אחרי הכנסתן פנימה, הראו המדענים ש‑APP המוטנטי מצוי בכמות נמוכה יותר על פני התאים ונלקח פנימה מהר יותר לתאים מאשר APP רגיל. ברגע שמגיעים לאנדוזומים מוקדמים אלה, APP נפגש עם האנזימים שמייצרים Aβ, וההובלה המוטה נראית כנותנת לאותם אנזימים הזדמנות רבה יותר לפעול. במקביל, החיתוך באתר ה‑η על המשטח גם הוא מוגבר, מה שמסביר את העלייה ב‑Aη.
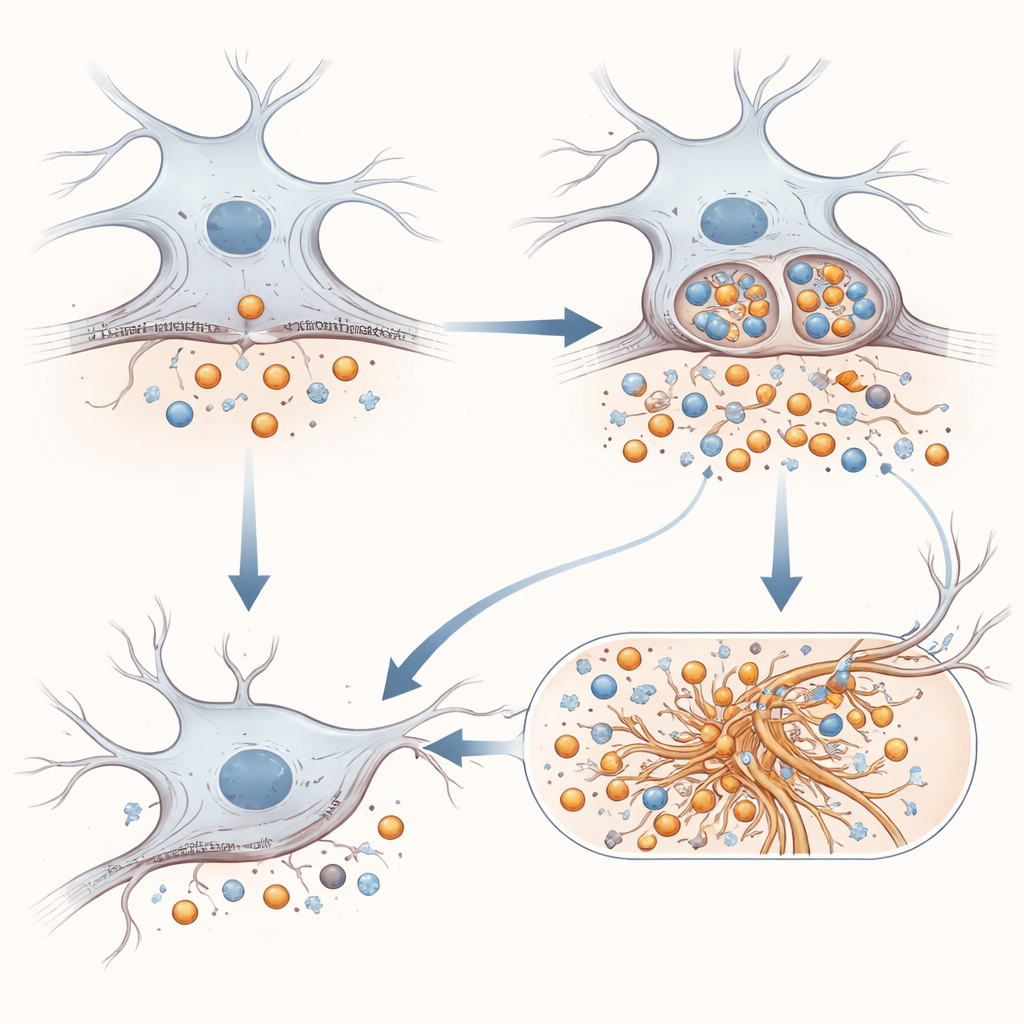
מחלקיקי חלבון עד לטאו הסבוך ודלקת מוחית
הסיפור אינו מסתיים בחתיכות הקשורות לאמילואיד. החוקרים בדקו האם APP המוטנטי ישפיע על טאו, החלבון המבני שיוצר סיבים מתולתלים בהרבה דמנציות. במודלים תאיים שמאירים כאשר זרעוני טאו גורמים להיווצרות גושים חדשים של טאו, נוכחות APP E590D הובילה לאגרגציה חזקה יותר מאשר APP רגיל או העדר APP. במודל עכבר שכבר נוטה לבעיות טאו, הזרקת וירוס שמבטא את APP המוטנטי להיפוקמפוס החריפה את סבכי הטאו והפעילה חזק יותר את האסטרוציטים והמיקרוגליה, תאי התמיכה והחיסון של המוח. מעניין כי חלקיקי אמילואיד מסיסים רגילים היו קשים לגילוי במוחות העכברים הללו, אך שבר ייחודי שמקורו ב‑APP הופיע רק כאשר המוטציה היתה נוכחת, דבר המצביע על עיבוד שונה ברקמה חיה.
מה המשמעות של זה להבנת אלצהיימר
לסיכום, הממצאים מראים שמוטציה נדירה זו ב‑APP אינה תופעה תמימה. היא דוחפת את APP לייצר יותר מפפטיד רעיל אחד, מאיצה את שלבי הקליטה פנימה שמעדיפים חיתוכים מזיקים, ומגבירה את סבכי הטאו ואת הדלקת במוח. עבור קהל לא־מומחה, המסר המרכזי הוא שביולוגיית אלצהיימר אינה מונעת על‑ידי שחקן בודד אלא על‑ידי רשת של שברי חלבון ומענים תאיים משולבים. חקר וריאנטים גנטיים רבי‑עוצמה אך בלתי שגרתיים כאלה מספק תמונה מגדילה של אותה רשת. במקרה זה, הדבר מצביע על כך שטיפולים עשויים להצטרך להתייחס הן לאמילואיד והן לפפטידים חלופיים שמקורם ב‑APP כמו Aη, וכן להשפעתם המשולבת על טאו, במקום להתמקד במסלול יחיד בבידוד.
ציטוט: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
מילות מפתח: מחלת אלצהיימר, חלבון מקור האמילואיד, קמטי טאו, דלקת עצבית, מוטציה גנטית