Clear Sky Science · he
פלטפורמה כמותית מהירה המשתמשת באורגנואידים צרברליים אנושיים מפורקים דו-ממדיים למידול דלקת עצבית במחלת אלצהיימר
מדוע זיהומים עלולים להיות חשובים לאובדן זיכרון
בדרך כלל מתארים את מחלת אלצהיימר כבנייה איטית של חלבונים דביקים במוח, אך ראיות גוברות מרמזות כי זיהומים עשויים לסייע בהפעלת התהליך הזה. המחקר הזה בוחן את הרעיון באמצעות מודלים זעירים של מוח אנושי שגודלו במעבדה ושואל שאלה פשוטה: האם וירוס דלקת שלפוחיות קרה נפוץ יכול להצית שינויים דמויי־אלצהיימר בתאי מוח אנושיים, והאם תרופה אנטי־ויראלית יכולה להפחית שינויים אלה?
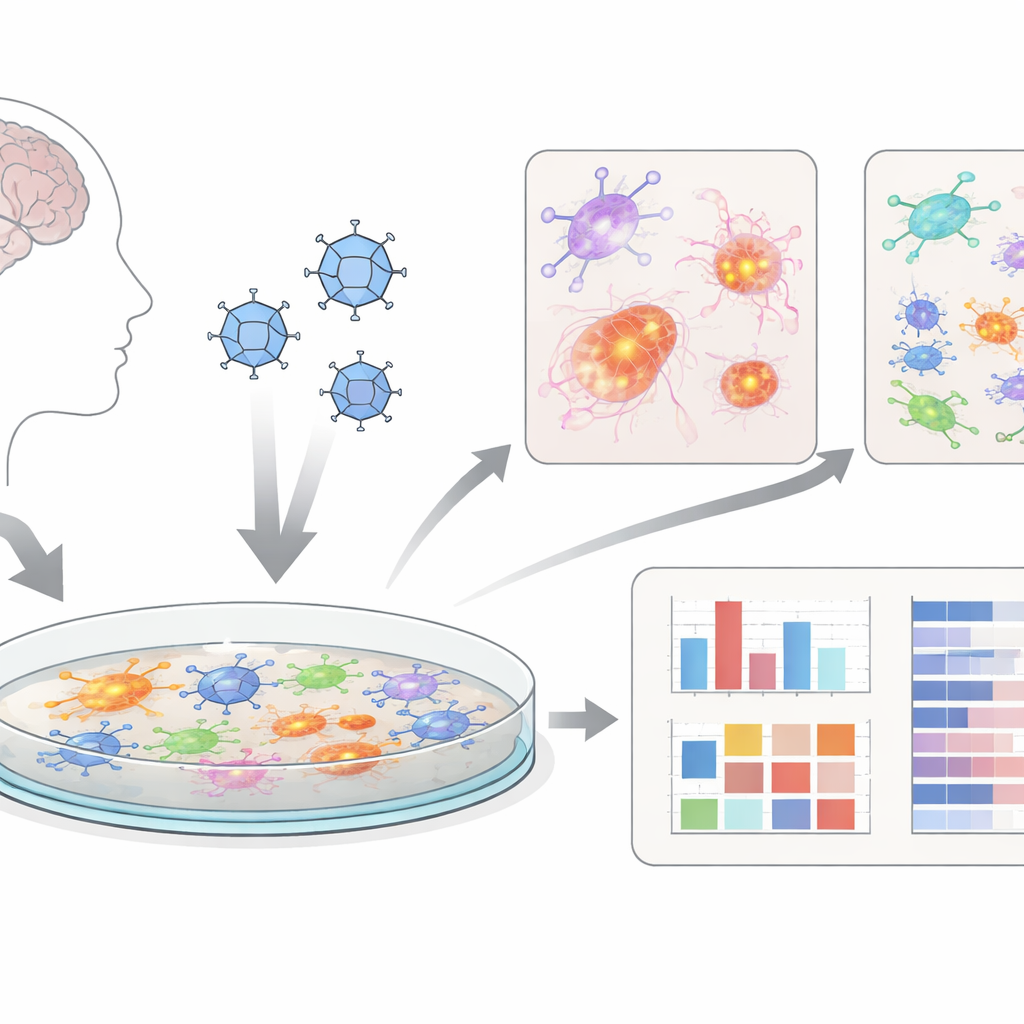
מיני־מוחות בצלחת
במקום לעבוד רק עם חיות, החוקרים השתמשו ב"אורגנואידים צרברליים" – צבירים של תאים הדומים למוח שגודלו מתאי גזע אנושיים. לאחר מכן הם פירקו בעדינות את האורגנואידים התלת־ממדיים לשכבות שטוחות של תאי מוח מעורבים, כולל נוירונים, תאי תמך שנקראים אסטרוציטים ותאים דמויי־חיסון שנקראים מיקרוגליה. תרביות דו־ממדיות אלה, שהם מכנים dcOrgs, קלות יותר לזיהום בצורה אחידה ולהערכה בהיקפים גדולים, כלומר ניתן לבדוק במקביל הרבה צלחות ותנאי תרופות. זה עושה את המערכת לאטרקטיבית ככלי סקרין של טיפולים חדשים.
וירוס שלפוחיות כגפרור
הקבוצה הדביקה dcOrgs בווירוס ההרפס סימפלקס 1 (HSV-1), הוירוס שאחראי לרוב שלפוחיות הקור וספק ארוך שלעיתים תורם לדמנציה אצל חלק מהאנשים. הם השוו תרביות מודבקות לבקרות שטופלו בדמה, לתרביות שקיבלו תרופה אנטי־ויראלית (אַסיקלוביר), לתרביות שנחשפו לוירוס שונה (שפעת A), ולוירוס שהושבת באמצעות קרינה על־סגולית. באמצעות ניתוח תאי אוטומטי וריצוף חד־תאי הם אישרו כי HSV-1 מדביק בעוצמה סוגים רבים של תאים בצלחת, בעוד שהוירוס המושבת והשפעת הפיקו דפוסים שונים והרבה יותר מתונים של שינוי.
שינויים דמויי־אלצהיימר בתוך ובין תאים
ב־dcOrgs מודבקים ב־HSV-1, תאים רבים הצטברו ברמות גבוהות של אותם צורות חלבון הנראות במוחות של חולי אלצהיימר: אגירה של בטא־עמילואיד מצופפת בתוך תאים וכמה גרסאות "מזורחנות" של טאו, חלבון מרכזי נוסף במחלה. הצטברויות אלה היו קשורות בחוזקה לתאים המכילים חלבוני וירוס והיו חזקות במיוחד בתאים גוססים. במקביל, פחות מקטע הבטא־עמילואיד הארוך (Aβ42) שוחרר לנוזל הסובב יחסית לצורות הקצרות יותר, שינוי שמשקף דפוסים הנמדדים בנוזל השדרתי של חולי אלצהיימר. גם האוכלוסיות התאית השתנו: מספר הנוירונים ירד, בעוד שאסטרוציטים ומיקרוגליה התרחבו, מה שהדהד את אובדן הנוירונים והדלקת הריאקטיבית הנראים ברקמות מוח של מטופלים.
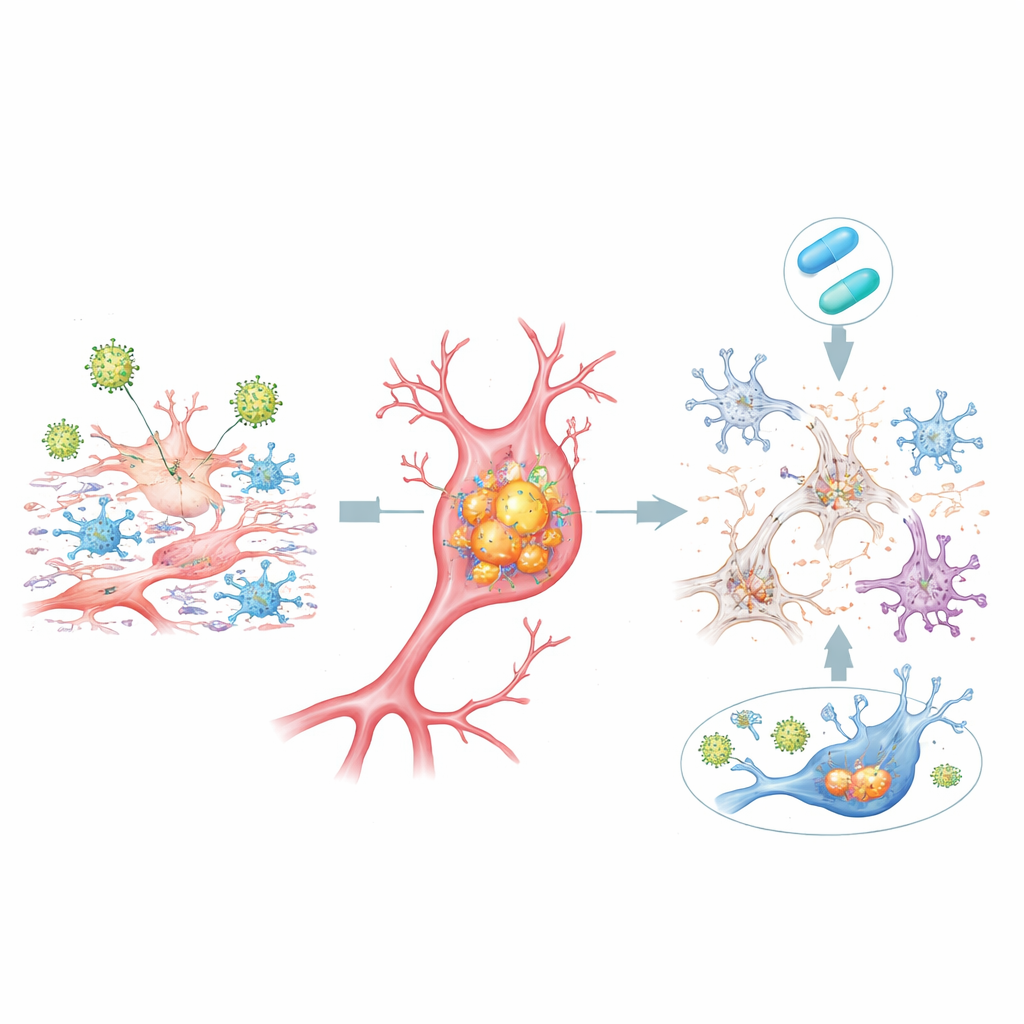
פעילות גנטית מקשרת את המודל לאלצהיימר האנושי
כאשר החוקרים בדקו פעילות גנים על פני כל הגנום, הם מצאו כי זיהום ב־HSV-1 ב־dcOrgs הדליק וכיבה רבים מהגנים שהיו מקושרים בעבר לסיכון לאלצהיימר במחקרים גנטיים רחבי היקף בבני אדם. שינויים אלה לא נראו בתרביות תאי גזע פשוטות או ב־dcOrgs מודבקים בשפעת, מה שמרמז על אינטראקציה ספציפית בין HSV-1 לסביבה המוחית המעורבת. ריצוף חד־תאי חשף שחלק משינויי הגנים המקושרים לאלצהיימר הגיעו מתאים שנחשפו לווירוס אך הכילו מעט או לא כלל חומר תורשתי של הווירוס בעצמן, מה שמרמז כי אותות מתאים מודבקים יכולים להפיץ תכניות דלקתיות מזיקות לשכנים.
מה טיפול אנטי־ויראלי יכול ומה לא יכול לתקן
הוספת התרופה האנטי־ויראלית אסיקלוביר זמן קצר לאחר החשיפה ל־HSV-1 הקטינה ביטוי גנים של הווירוס, הרגיעה תגובות דלקת רבות, הפחיתה את ההצטברות של בטא־עמילואיד וטאו רעילים בתוך תאים והשיבה חלקית את האיזון בין סוגי התאים השונים. לגבי חלק ניכר מהגנים המקושרים לאלצהיימר, רמות הפעילות שלהן חזרו לכיוון התקין. עם זאת, לא כל השינויים היו הפיכים: קבוצה משמעותית של גנים אנושיים נותרה ללא שינוי או אף הופרעה יותר על ידי הטיפול, במיוחד כאשר התרופה הייתה פחות יעילה בחסימת גנים ויראליים מאוחרים. זה מדגיש כי עצירת שכפול הווירוס עשויה לעזור, אבל לא בהכרח לבטל לחלוטין את המפל של האירועים הביולוגיים לאחר שהחל.
מה המשמעות להבנת אלצהיימר
ללא־מומחה, המסקנה היא שוירוס שלפוחיות אנושי, שפועל בתוך תערובת מציאותית של תאי מוח אנושיים, יכול במהירות לייצר הרבה סימנים היכר של מחלת אלצהיימר – מהצטברויות חלבון ונוירונים גוססים ועד דפוסים גנטיים שכבר נצפו בחולים. המערכת המבוססת על אורגנואידים שטוחים שנוצרת כאן מהירה, כמותית וקנה מידה, מה שהופך אותה לאתר בדיקה עוצמתי לתרופות אנטי־ויראליות וטיפולים אחרים שמטרתם להרגיע דלקת מוחית. אף על פי שזה אינו מוכיח שזיהומי הרפס גורמים לאלצהיימר אצל כל מטופל, זה מחזק את הטענה שבעבור תת־קבוצה של אנשים, זיהומים ויראליים כרוניים או מואצים עשויים להיות חלק חשוב בפאזל – ומטרת מניעה פוטנציאלית.
ציטוט: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
מילות מפתח: מחלת אלצהיימר, וירוס ההרפס סימפלקס, אורגנואידי מוח, דלקת בעצב, טיפול אנטי־ויראלי